
- •1.Основные понятия коллоидной химии; классификация, основные особенности, количественные характеристики дисперсных систем.
- •2. Диспергационные методы получения дисперсных систем
- •3. Конденсационные методы получения дисперсных систем
- •4. Закон Эйнштейна-Смолуховского, броуновское движение.
- •5. Первый и второй законы Фика, диффузия, движущая сила диффузии, связь коэффициента диффузии с размерами частиц
- •6. Гипсометрический закон Лапласа, диффузионно-седиментационное равновесие. Кривая седиментации для монодисперсных и полидисперсных систем.
- •7. Строение двойного электрического слоя (фи-потенциал и дзета-потенциал), теория Квинке-Гельмгольца-Перрена, теория Гуи-Чепмена, теория Штерна, строение мицеллы.
- •8. Рассеяние света. Опалесценция. Эффект Тиндаля.
- •9. Закон Бугера-Ламберта-Бера, оптические свойства коллоидных растворов, оптические методы анализа дисперсности.
- •10. Работа когезии. Связь поверхностной энергии с взаимодействиями между молекулами (атомами, ионами), правило Трутона, уравнение Дюпре. .
- •12. Закон Лапласа: общая форма, частные случаи, капиллярное поднятие жидкости, уравнение Жюрена.
- •13. Томсона (Кельвина), зависимость давления насыщенного пара от кривизны поверхности жидкости, капиллярная конденсация.
- •14. Закон Гиббса-Оствальда-Фрейндлиха, влияние дисперсности на растворимость твердых частиц, процессы изотермической перегонки в дисперсных системах.
- •15. Лиофильные коллоидные системы, методы получения. Самопроизвольное диспергирование макрофаз: критерий самопроизвольного диспергирования (по Ребиндеру-Щукину, примеры).
- •16. Мицеллообразование в водных растворах пав. Критическая концентрация мицеллообразования (ккм), основные методы определения ккм
- •17. Солюбилизация
- •18. Термодинамика мицеллообразования, диаграмма фазовых состояний, точка Крафта, жидкокристаллические системы.
- •19. Образование и строение обратных мицелл
- •20. Аэрозоли. Молекулярно-кинетические свойства. Седиментация
- •21. Термопреципитация
- •22. Фотофорез
- •23. Термофорез.
- •24. Коалесценция.
- •25. Быстрая и медленная коагуляция.
- •26. Концентрационная и нейтрализационная коагуляция
- •27. Изотермическая перегонка.
- •28. Пены, классификация и строение, разрушение пен и практическое применение.
- •29. Эффект Марангони.
- •30. Тиксотропия.
- •31. Флотация.
- •32. Эмульсии. Обращение фаз, разрушение эмульсий и практическое применение.
- •33. Правило Банкрофта
- •34. Правило Дюкло-Траубе
- •35. Правило Шульца-Гарди.
- •36.Критерий Эйлера-Корфа.
- •37. Теория длфо.
- •38. Слои Шиллера
- •39. Тактоиды
- •40. Биконтинуальные дисперсные системы
- •41. Кольца и слои Лизеганга
- •42. Пептизация.
- •43. Флокуляция
- •44. Гетерокоагуляция.
- •45. Адагуляция.
- •46. Аддитивность коагуляции.
- •47. Антагонизм коагуляции
- •48. Синергизм коагуляции
- •49. Коагуляционные структуры
- •50. Структуры с фазовыми контактами
- •51. Синерезис.
- •52. Конденсационные структуры
- •53. Кристаллизационные структуры
- •54. Когезия.
- •55. Адгезия
- •56. Физико-химические методы регулирования структурно-механических свойств дисперсных систем.
- •57. Смачивание.
- •58. Капиллярное давление
- •59. Закон Ньютона (трение)
- •60. Диссипация энергии
- •61. Застудневание
- •62.Ползучесть
- •63. Вязкость коллоидных растворов. Зависимость вязкости раствора от концентрации взвешенных частиц (уравнение Эйнштейна)
- •64.Аномалия вязкости коллоидных систем. Причины, которые вызывают аномалии вязкости
- •65. Как образуется снежинка
- •66. Хемосорбция и каталитическая сорбция, сходства и отличия, привести примеры
- •67. Почему “химические дожди” выпадают недалеко от источника загрязнения?
- •68. Адсорбция
- •69. Абсорция.
- •70. Хемосорбция.
- •71. Каталитическая сорбция
- •72. Обеспечивает вертикальную устойчивость облаков?
- •73. В чём сходство и различие газовой и жидкой дисперсионных сред?
- •74. Почему туман в вечернее время распространяется в приземном слое, не оседая на поверхность?
- •75. Почему снег выпадает иногда в виде “крупы”?
- •76. Почему иней в большей степени образуется на открытых участках, чем в лесу?
- •77. Адсорбция и адагуляция, сходства и отличия, привести примеры
- •78. Количественные характеристики дисперсных систем
- •78. Количественные характеристики дисперсных систем.
- •79. Классификация дисперсных систем по размеру частиц дисперсной фазы ( отличительные особенности частиц разных размеров)
- •80. Классификация дисперсных систем по фракционному составу частиц.
- •81. Классификация дисперсных систем по концентрации частиц.
- •82. Классификация дисперсных систем по характеру взаимодействий дисперсной фазы с дисперсной средой.
- •83. Классификация дисперсных систем по характеру распределения фаз.
- •84. Классификация дисперсных систем по агрегатному состоянию дисперсной фазы и дисперсной среды.
- •85. Классификация дисперсных частиц по размерам.
- •86. Классификация дисперсных частиц по форме
- •87. Классификация дисперсных частиц по строению.
- •88. Классификация дисперсных частиц по химическому составу.
- •89. Размерные эффекты, наблюдаемые в дисперсных системах.
- •90. Термодинамические свойства дисперсных частиц.
- •91. Механические свойства дисперсных частиц.
- •92. Магнитные свойства дисперсных частиц.
- •93. Каталитические свойства дисперсных частиц.
- •94. Энергетическое и силовое определение поверхностного натяжения.
- •95. Факторы, влияющие на поверхностное натяжение жидкостей.
- •96. Дисперсионная и полярная составляющая поверхностного натяжения жидкостей.
- •97. Метод избыточных величин Гиббса.
- •98. Капиллярное давление (определение, физический смысл, от чего зависит)
- •99. Несмачивание, полное смачивание, гидрофильность и гидрофобность.
- •100. Правило Антонова.
- •101. Эффект Марангони
- •102. Зависимость смачиваемости от свойств твердой поверхности
- •103. Смачивание нанокаплями
- •104. Адгезия, когезия, уравнение Дюпре.
- •105. Изотермическая перегонка
- •106. Перекристаллизация
- •107. Капиллярная конденсация
- •108. Закон Жюрена. (высота подъема жидкости в капиллярных трубках)
- •109. Измерение поверхностного натяжения методом капиллярного подъема.
- •110. Измерение поверхностного натяжения методом сидящей капли.
- •111. Измерение поверхностного натяжения методом максимального давления.
- •112.Измерение поверхностного натяжения методом пластинки Вильгельми.
- •113. Измерение поверхностного натяжения методом вращающейся капли.
- •114. Измерение поверхностной энергии твердых тел
- •115. Адсорбция пав на поверхности раздела жидких фаз.
- •116. Адсорбция пав из растворов на поверхности твердых тел.
- •117. Химическое модифицирование твердых тел.
- •118. Классификация пав по растворимости.
- •119. Классификация пав по диссоциации в воде.
- •120. Классификация пав по происхождению и по способности к образованию мицелл.
- •121. Классификация пав по физико-химическому воздействию на поверхность раздела между фазами.
- •122. Гидрофильно-липофильный баланс.
- •123. Критический параметр упаковки
- •125. Строение дэс
- •126. Влияние электролитов на дэс.
- •127. Электрофорез.
- •128. Электроосмос.
- •129. Потенциал течения.
- •130. Потенциал оседания.
- •131. Электрокапиллярные явления. (Электрокапилярная кривая, уравнение Липпмана)
61. Застудневание
Застудневание - студнеобразование, гелеобразование, желатинирование, желатинизация, превращение легко подвижной или вязкотекучей жидкости в твердообразное (т. е. лишённое текучести) тело, обладающее эластичностью, пластичностью, хрупкостью. З. характерно для растворов высокомолекулярных соединений и коллоидно-дисперсных систем. Оно обусловлено возникновением пространственной структурной сетки (каркаса), пронизывающей весь объём жидкости и лишающей её подвижности. В растворах полимеров такая сетка образуется из макромолекул, соединённых силами межмолекулярного взаимодействия или химическими связями , в коллоидных системах — из сцепленных частиц дисперсной фазы. З. может быть вызвано повышением или понижением температуры, увеличением концентрации растворённого или диспергированного вещества, изменением состава системы вследствие химического взаимодействия её компонентов или введения специальных реагентов. Иногда З. обратимо, т. е. с изменением условий система многократно может переходить из жидкого состояния в твердообразное и наоборот. Однако при глубоких химических или физических изменениях в системе З. происходит необратимо.
Примеры:Жидкий слой краски, лака, клея, фотографической эмульсии застудневает прежде, чем окончательно высохнуть. З. происходит при введении электролитов в каучуковый латекс, при отверждении синтетических смол в производстве пластмасс, при охлаждении растворов желатины и крахмального клейстера, при свёртывании крови и т.п.
62.Ползучесть
Ползучесть материалов — изменение с течением времени деформации твёрдого тела под воздействием постоянной нагрузки или механического напряжения. Ползучести в той или иной мере подвержены все твёрдые тела — как кристаллические, так и аморфные.
Ползучесть материалов экспериментально изучают прежде всего при простых напряженных состояниях: одноосных растяжении, сжатии, а также чистом сдвиге. Ползучесть при сложных напряженных состояниях изучают обычно на тонкостенных трубчатых образцах.
Стадии ползучести. Как общее время до разрушения, так и протяжённость каждой из стадий зависят от температуры и приложенной нагрузки. При температурах, составляющих 40 %-80 % температуры плавления металла (именно эти температуры представляют наибольший технический интерес), затухание ползучести на первой её стадии является результатом деформационного упрочнения (наклёпа). Так как ползучесть происходит при высокой температуре, то возможно также снятие наклёпа — так называемый возврат свойств материала. Когда скорости наклёпа и возврата становятся одинаковыми, наступает II стадия ползучести. Переход в III стадию связан с накоплением повреждения материала (поры, микротрещины), образование которых начинается уже на I и II стадиях.
63. Вязкость коллоидных растворов. Зависимость вязкости раствора от концентрации взвешенных частиц (уравнение Эйнштейна)
Вязкость жидкостей может сильно изменяться в присутствии растворенных или диспергированных компонентов. Вязкость большинства гидрофобных золей и суспензий при малых концентрациях почти не отличается от вязкости чистого растворителя, и такие растворы подчиняются законам Ньютона и Пуазейля. Однако по мере увеличения концентрации дисперсной фазы вязкость золя или суспензии даже в области подчинения законам Ньютона и Пуазейля становится больше вязкости чистого растворителя. Это объясняется тем, что частицы дисперсной фазы преграждают путь слоям движущейся жидкости, которой приходится обтекать частицы. Траектория течения жидкости искривляется, удлиняется и в единицу времени вытекает меньший объем жидкости. Этот эффект еще больше усиливается при удлиненной форме дисперсных частиц, которые могут вращаться вокруг своей поперечной оси (как пропеллер) под влиянием движущейся жидкости. Вращающаяся частица занимает больший кажущийся объем в системе, чем неподвижная, и это вызывает более резкое отличие вязкости коллоидного раствора от вязкости чистого растворителя.
А. Эйнштейн установил зависимость вязкости раствора от концентрации взвешенных частиц. При этом он исходил из допущений, что частицы дисперсной фазы удалены друг от друга, имеют одинаковые размер и форму и между ними отсутствует взаимодействие, а также что они велики
по сравнению с частицами растворителя. Тогда η = η0(1+ αϕ) , где η – вязкость раствора; η0 – вязкость растворителя; α – коэффициент, зависящий от формы частиц; ϕ – объемная доля дисперсной фазы.
Д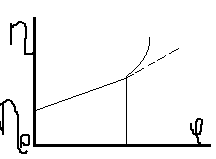 ля
сферических частиц α
=2.5, для удлиненных
α >2.5.
Величина ϕ
может быть
выражена отношением суммарного объема
всех частиц дисперсной фазы к общему
объему всей системы
ля
сферических частиц α
=2.5, для удлиненных
α >2.5.
Величина ϕ
может быть
выражена отношением суммарного объема
всех частиц дисперсной фазы к общему
объему всей системы
ϕ =V / (V +V ). Графически уравнение Эйнштейна выражается прямой в координатах η – ϕ(см. рис.). При превышении некоторой критической величины объемной доли ϕкр экспериментальные данные расходятся с теоретическими. Уравнение Эйнштейна применимо для золей и разбавленных суспензий, у которых частицы дисперсной фазы не взаимодействуют с дисперсионной средой (лиофобные системы).
