
- •§ 97. Сторонние силы. Электродвижущая сила и напряжение
- •§ 98. Закон Ома. Сопротивление проводников
- •§ 99. Работа и мощность тока. Закон Джоуля — Ленца
- •§ 100. Закон Ома для неоднородного участка цепи
- •§ 101. Правила Кирхгофа для разветвленных цепей
- •Глава 14 Магнитное поле § 109. Магнитное поле и его характеристики
- •§ 110. Закон Био - Савара - Лапласа и его применение к расчету магнитного поля
- •§ 111. Закон Ампера. Взаимодействие параллельных токов
- •§ 112. Магнитная постоянная. Единицы магнитной индукции и напряженности магнитного поля
- •§ 113. Магнитное поле движущегося заряда
- •§ 114. Действие магнитного поля на движущийся заряд
- •§ 115. Движение заряженных частиц в магнитном поле
- •§ 116. Ускорители заряженных частиц
- •§ 117. Эффект Холла
- •§ 118. Циркуляция вектора в магнитного поля в вакууме
- •§ 119. Магнитные поля соленоида и тороида
- •§ 120. Поток вектора магнитной индукции. Теорема Гаусса для поля в
- •§ 121. Работа по перемещению проводника и контура с током в магнитном поле
- •§ 123. Закон Фарадея и его вывод из закона сохранения энергии
- •§ 125. Вихревые токи (токи Фуко)
- •§ 126. Индуктивность контура. Самоиндукция
- •§ 127. Токи при размыкании и замыкании цепи
- •§ 128. Взаимная индукция
- •§ 129. Трансформаторы
- •§ 130. Энергия магнитного поля
- •Глава 16 Магнитные свойства вещества § 131. Магнитные моменты электронов и атомов
- •§ 133. Намагниченность. Магнитное поле в веществе
- •§ 134. Условия на границе раздeла двух магнетиков
- •§ 135. Ферромагнетики и их свойства
- •§ 136. Природа ферромагнетизма
- •§ 138. Ток смещения
- •§ 139. Уравнения Максвелла для электромагнитного поля
- •§ 141. Механические гармонические колебания
- •§ 142. Гармонический осциллятор. Пружинный, физический и математический маятники
- •§ 143. Свободные гармонические колебания в колебательном контуре
- •§ 144. Сложение гармонических колебаний одного направления и одинаковой частоты. Биения
- •§ 145. Сложение взаимно перпендикулярных колебаний
- •§ 146. Дифференциальное уравнение свободных затухающих колебаний (механических и электромагнитных) и его решение.
- •§ 147. Дифференциальное уравнение вынужденных колебаний (механических и электромагнитных) и его решение
- •§ 148. Амплитуда и фаза вынужденных колебаний (механических и электромагнитных). Резонанс
- •§ 149. Переменный ток
- •§ 150. Резонанс напряжений
- •§ 151. Резонанс токов
- •§ 152. Мощность, выделяемая в цепи переменного тока
- •§ 154. Уравнение бегущей волны. Фазовая скорость. Волновое уравнение
- •§ 155. Принцип суперпозиции. Групповая скорость
- •§ 156. Интерференция волн
- •§ 157. Стоячие волны
- •§ 158. Звуковые волны
- •§ 158. Эффект Доплера в акустике
- •§ 160. Ультразвук и его применение
- •§ 182. Дифференциальное уравнение электромагнитной волны
- •§ 163. Энергия электромагнитных волн. Импульс электромагнитного поля
- •§ 164. Излучение диполя. Применение электромагнитных волн
- •§ 166. Тонкие линзы. Изображение предметов с помощью линз
- •§ 167. Аберрации (погрешности) оптических систем
- •§ 168. Основные фотометрические величины и их единицы
- •§ 169. Элементы электронной оптики
- •Глава 22 Интерференция света § 170. Развитие представлений о природе света
- •§ 171. Когерентность и монохроматичность световых волн
- •§ 172. Интерференция света
- •§ 173. Методы наблюдения интерференции света
- •§ 174. Интерференции света в тонких пленках
- •§ 175. Применение интерференции света
- •Глава 23 Дифракция света § 176. Принцип Гюйгенса — Френеля
- •§ 177. Метод зон Френеля. Прямолинейноe распространение света
- •§ 178. Дифракция Френеля на круглом отверстии и диске
- •§ 179. Дифракция Фраунгофера на одной щели
- •§ 180. Дифракция Фраунгофера на дифракционной решетке
- •§ 181. Пространственная решетка. Рассеянии света
- •§ 182. Дифракция на пространственной решетке. Формула Вульфа — Брэггов
- •§ 183. Разрешающая способность оптических приборов
- •§ 184. Понятие о голографии
- •Глава 24 Взаимодействие электромагнитных волн с веществом § 185. Дисперсия света
- •§ 186. Электронная теория дисперсии света
- •§ 187. Поглощение (абсорбция) света
- •§ 188. Эффект Доплера
- •§ 189. Излучение Вавилова — Черенкова
- •Глава 25 Поляризация света § 190. Естественный и поляризованный свет
- •§ 191. Поляризация света при отражении и преломлении на границе двух диэлектриков
- •§ 192. Двойное лучепреломление
- •§ 193. Поляризационные призмы и поляроиды
- •§ 194. Анализ поляризованного света
- •§ 195. Искусственная оптическая анизотропия
- •§ 196. Вращение плоскости поляризации
- •Глава 26 Квантовая природа излучения § 197. Тепловое излучение и «го характеристики
- •§ 198. Закон Кирхгофа
- •§ 199. Законы Стефана — Больцмана и смещения Вина
- •§ 200. Формулы Рэлея — Джинса и Планка
- •§ 201. Оптическая пирометрия. Тепловые источники света
- •§ 202. Виды фотоэлектрического эффекта. Законы внешнего фотоэффекта
- •§ 203. Уравнение Эйнштейна для внешнего фотоэффекта. Экспериментальное подтверждение квантовых свойств света
- •§ 204. Применение фотоэффекта
- •§ 205. Масса и импульс фотона. Давление света
- •§ 206. Эффект Комптона и его элементарная теория
- •§ 207. Единство корпускулярных и волновых свойств электромагнитного излучения
- •§ 209. Линейчатый спектр атома водорода
- •§ 210. Постулаты Бора
- •§ 211. Опыты Франка и Герца
- •§ 212. Спектр атома водорода по Бору
- •§ 214. Некоторые свойства волн де Бройля
- •§ 215. Соотношение неопределенностей
- •§ 216. Волновая функция и ее статистический смысл
- •§ 217. Общее уравнение Шредингера. Уравнение Шредингера для стационарных состояний
- •§ 218. Принцип причинности в квантовой механике
- •§ 219. Движение свободной частицы
- •§ 220. Частица в одномерной прямоугольной «потенциальной яме» е бесконечно высокими «стенками»
- •§ 221. Прохождение частицы сквозь потенциальный барьер. Туннельный эффект
- •§ 222. Линейный гармонический осциллятор в квантовой механике
- •§ 225. Спин электрона. Спиновое квантовое число
- •§ 226. Принцип неразличимости тождественных частиц. Фермионы и бозоны
- •§ 227. Принцип Паули. Распределение электронов в атоме по состояниям
- •§ 228. Периодическая система элементов Менделеева
- •§ 229. Рентгеновские спектры
- •§ 230. Молекулы: химические связи, понятие об энергетических уровнях
- •§ 231. Молекулярные спектры. Комбинационное рассеяние света
- •§ 232. Поглощение. Спонтанное и вынужденное излучения
- •§ 233. Оптические квантовые генераторы (лазеры)
- •§ 235. Понятие о квантовой статистике Бозе — Эйнштейна и Ферми — Дирака
- •§ 236. Вырожденный электронный газ в металлах
- •§ 237. Понятие о квантовой теории теплоемкости. Фононы
- •§ 238. Выводы квантовой теории электропроводности металлов
- •§ 239. Сверхпроводимость. Понятие об эффекте Джозефсона
- •Глава 31 Элементы физики твердого тела § 240. Понятие о зонной теории твердых тел
- •§ 241. Металлы, диэлектрики и полупроводники по зонной теории
- •§ 242. Собственная проводимость полупроводников
- •§ 243. Примесная проводимость полупроводников
- •§ 244. Фотопроводимость полупроводников
- •§ 245. Люминесценция твердых тел
- •§ 247. Термоэлектрические явления и их применение
- •§ 248. Выпрямление на контакте металл — полупроводник
- •§ 249. Контакт электронного и дырочного полупроводников (р-п-переход)
- •§ 250. Полупроводниковые диоды и триоды (транзисторы)
- •§ 252. Дефект массы и энергия связи ядра
- •§ 253. Спин ядра и его магнитный момент
- •§ 254. Ядерные силы. Модели ядра
- •§ 255. Радиоактивное излучение и его виды
- •§ 256. Закон радиоактивного распада. Правила смещения
- •§ 257. Закономерности -распада
- •§ 259. Гамма-излучение и его свойства
- •§ 260. Резонансное поглощение g-излучения (эффект Мбссбауэра**)
- •§ 261. Методы наблюдения и регистрации радиоактивных излучений и частиц
- •§ 262. Ядерные реакции и их основные типы
- •§ 264. Открытие нейтрона. Ядерные реакции под действием нейтронов
- •§ 265. Реакция деления ядра
- •§ 266. Цепная реакция деления
- •§ 267. Понятие о ядерной энергетикe
- •§ 268. Реакция синтеза атомных ядер. Проблема управляемых термоядерных реакций
- •§ 270. Мюоны и их свойства
- •§ 271. Мезоны и их свойства
- •§ 273. Частицы и античастицы
- •§ 274. Гипероны. Странность и четность элементарных частиц
- •§ 275. Классификация элементарных частиц. Кварки
- •Заключение
- •Основные законы и формулы
§ 222. Линейный гармонический осциллятор в квантовой механике
Линейный гармонический осциллятор — система, совершающая одномерное движение под действием квазиупругой силы, — является моделью, используемой во многих задачах классической и квантовой теории (см. § 142). Пружинный, физический и математический маятники — примеры классических гармонических осцилляторов. Потенциальная энергия гармонического осциллятора (см. (141.5)) равна
![]() (222.1)
(222.1)
где 0 — собственная частота колебаний осциллятора, m— масса частицы. Зависимость (222.1) имеет вид параболы (рис. 300), т. е. «потенциальная яма» в данном случае является параболической.
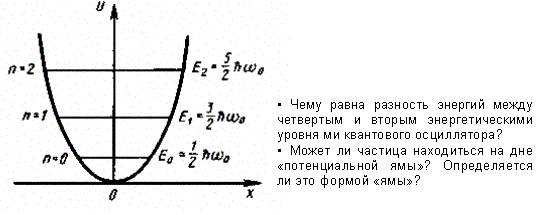
Рис. 300
Амплитуда малых колебаний классического осциллятора определяется его полной энергией Е (см. рис. 16). В точках с координатами ±хmax полная энергия Е равна потенциальной энергии. Поэтому с классической точки зрения частица не может выйти за пределы области (-хmax, + хmax). Такой выход означал бы, что ее потенциальная энергия больше полной, что абсурдно, так как приводит к выводу, что кинетическая энергия отрицательна. Таким образом, классический осциллятор находится в «потенциальной яме» с координатами —
- хmax x хmax «без права выхода» из нее.
Гармонический осциллятор в квантовой механике — квантовый осциллятор — описывается уравнением Шредингера (217.5), учитывающим выражение (222.1) для потенциальной энергии. Тогда стационарные состояния квантового осциллятора определяются уравнением Шредингера вида
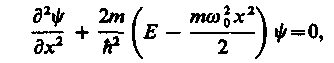 (222.2)
(222.2)
где Е — полная энергия осциллятора. В теории дифференциальных уравнений доказывается, что уравнение (222.2) решается только при собственных значениях энергии
![]() (222.3)
(222.3)
Формула (222.3) показывает, что энергия квантового осциллятора может иметь лишь декретом значения, т. е. квантуется. Энергия ограничена снизу отличным от нуля, как и для прямоугольной «ямы» с бесконечно высокими «стенками» (см. § 220), минимальным значением энергии E0 = 1/2ℏ0. Существование минимальной энергии — она называется энергией нулевых колебаний — является типичной для квантовых систем и представляет собой прямое следствие соотношения неопределенностей.
Наличие нулевых колебаний означает, что частица не может находиться на дне «потенциальной ямы», причем этот вывод не зависит от ее формы. В самом деле, «падение на дно ямы» связано с обращением в нуль импульса частицы, а вместе с тем и его неопределенности. Тогда неопределенность координаты становится сколь угодно большой, что противоречит, в свою очередь, пребыванию частицы в «потенциальной яме».
Вывод о наличии энергии нулевых колебаний квантового осциллятора противоречит выводам классической теории, согласно которой наименьшая энергия, которую может иметь осциллятор, равна нулю (соответствует покоящейся в положении равновесия частице). Например, классическая физика приводит к выводу, что при Т=0 энергия колебательного движения атомов кристалла должна обращаться в нуль. Следовательно, должно исчезать и рассеяние света, обусловленное колебаниями атомов. Однако эксперимент показывает, что интенсивность рассеяния света при понижении температуры не равна нулю, а стремится к некоторому предельному значению, указывающему на то, что при T0 колебания атомов в кристалле не прекращаются. Это является подтверждением наличия нулевых колебаний.
Из формулы (222.3) также следует, что уровни энергии линейного гармонического осциллятора расположены на одинаковых расстояниях друг от друга (рис. 300), а именно расстояние между соседними энергетическими уровнями равно ℏ0, причем минимальное значение энергии E0 = 1/2ℏ0.
Строгое решение задачи о квантовом осцилляторе приводит еще к одному значительному отличию от классического рассмотрения. Квантово-механический расчет показывает, что частицу можно обнаружить за пределами дозволенной области |х| < хmax (см. рис. 16), в то время как с классической точки зрения она не может выйти за пределы области (- хmax, + хmax). Таким образом, имеется отличная от нуля вероятность обнаружить частицу в той области, которая является классически запрещенной. Этот результат (без его вывода) демонстрируется на рис. 301, где приводится квантовая плотность вероятности w обнаружения осциллятора для состояния n = 1.

Рис. 301
Из рисунка следует, что для квантового осциллятора действительно плотность вероятности w имеет конечные значения за пределами классически дозволенной области |x| хmax т. е. имеется конечная (но небольшая) вероятность обнаружить частицу в области за пределами «потенциальной ямы». Существование отличных от нуля значений w за пределами «потенциальной ямы» объясняется возможностью прохождения микрочастиц сквозь потенциальный барьер (см. § 221).
Задачи
28.1. Свободная частица движется со скоростью u. Доказать, что выполняется соотношение vфазu = c2.
28.2. Электрон движется в атоме водорода по первой боровской орбите. Принимая, что допускаемая неопределенность скорости составляет 1% от ее числового значения, определить неопределенность координаты электрона. Применительно ли в данном случае для электрона понятие траектории? [х=33 нм; нет]
28.3.
-Функция
некоторой частицы имеет вид
![]() , где г — расстояние этой частицы от
силового центра, а
—
постоянная. Определить среднее расстояние
r
частицы от силового центра. [r=/2]
, где г — расстояние этой частицы от
силового центра, а
—
постоянная. Определить среднее расстояние
r
частицы от силового центра. [r=/2]
28.4. Записать уравнение Шредингера для стационарных состояний электрона, находящегося в атоме водорода.
28.5. Электрон находится в одномерной прямоугольной «потенциальной яме» шириной lс бесконечно высокими «стенками». Определить вероятность W обнаружения электрона в средней трети «ямы», если электрон находится в возбужденном состоянии (n=2). Пояснить физический смысл полученного результата, изобразив графически плотность вероятности обнаружения электрона в данном состоянии. [W=0,195]
28.6. Прямоугольный потенциальный барьер имеет ширину 0,1 нм. Определить в электрон-вольтах разность энергий U - E, при которой вероятность прохождения электрона сквозь барьер составит 0,99. [0,1 мэВ]
Глава 29
Элементы современной физики
атомов и молекул
§ 223. Атом водорода в квантовой механике
Решение задачи об энергетических уровнях электрона для атома водорода (а также водородоподобных систем: иона гелия Не"1", двукратно ионизованного лития Li+ + и др.) сводится к задаче о движении электрона в кулоновском поле ядра.
Потенциальная энергия взаимодействия электрона с ядром, обладающим зарядом Ze (для атома водорода Z= 1),
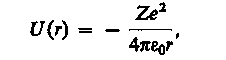
где r — расстояние между электроном и ядром. Графически функция U(r) изображена жирной кривой на рис. 302. U(r) с уменьшением г (при приближении электрона к ядру) неограниченно убывает.
Состояние электрона в атоме водорода описывается волновой функцией , удовлетворяющей стационарному уравнению Шредингера (217.5), учитывающему значение (223.1):
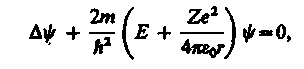 (223.2)
(223.2)
где m — масса электрона, Е — полная энергия электрона в атоме. Так как поле, в котором движется электрон, является центрально-симметричным, то для решения уравнения (223.2) обычно используют сферическую систему координат: r, , . Не вдаваясь в математическое решение этой задачи, ограничимся рассмотрением важнейших результатов, которые из него следуют, пояснив их физический смысл.
1. Энергия. В теории дифференциальных уравнении доказывается, что уравнения типа (223.2) имеют решения, удовлетворяющие требованиям однозначности, конечности и непрерывности волновой функции , только при собственных значениях энергии
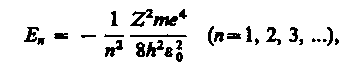 (223.3)
(223.3)
т. е. для дискретного набора отрицательных значений энергии.
Таким образом, как и в случае «потенциальной ямы» с бесконечно высокими «стенками» (см. § 220) и гармонического осциллятора (см. § 222), решение уравнения Шредингера для атома водорода приводит к появлению дискретных энергетических уровней. Возможные значения Е1, Е2, Е3,... показаны на рис. 302 в виде горизонтальных прямых. Самый нижний уровень El, отвечающий минимальной возможной энергии, — основной, все остальные (En > E1, n = 2, 3, ...) — возбужденные (см. § 212). При Е < 0 движение электрона является связанным — он находится внутри гиперболической «потенциальной ямы». Из рисунка следует, что по мере роста главного квантового числа n энергетические уровни располагаются теснее и при n = E = 0. При Е > 0 движение электрона является свободным; область непрерывного спектра Е > 0 (заштрихована на рис. 302) соответствует ионизованному атому. Энергия ионизации атома водорода равна
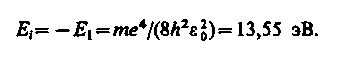
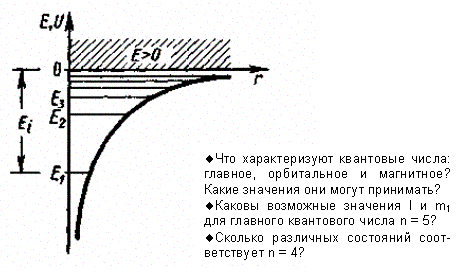
Рис. 302
Выражение (223.3) совпадает с формулой (212.3), полученной Бором для энергии атома водорода. Однако если Бору пришлось вводить дополнительные гипотезы (постулаты), то в квантовой механике дискретные значения энергии, являясь следствием самой теории, вытекают непосредственно из решения уравнения Шредингера.
2. Квантовые числа. В квантовой механике доказывается, что уравнению Шредингера (223.2) удовлетворяют собственные функции (r, в, <р), определяемые тремя квантовыми числами: главным л, орбитальным / и магнитным /и/.
Главное квантовое число л, согласно (223.3), определяет энергетические уровни электрона в атоме и может принимать любые целочисленные значения начиная с единицы:
![]()
Из решения уравнения Шредингера вытекает, что момент импульса (механический орбитальный момент) электрона квантуется, т. е. не может быть произвольным, а принимает дискретные значения, определяемые формулой
![]() (223.4)
(223.4)
где l — орбитальное квантовое число, которое при заданном л принимает значения
![]() (223.5)
(223.5)
т. е. всего n значений, и определяет момент импульса электрона в атоме.
Из решения уравнений Шредингера следует также, что вектор Ll момента импульса электрона может иметь лишь такие ориентации в пространстве, при которых его проекция Llx на направление z внешнего магнитного поля принимает квантованные значения, кратные n:
![]() (223.6)
(223.6)
где ml — магнитное квантовое число, которое при заданном l может принимать значения
![]() (223.7)
(223.7)
т. е. всего 2l+1 значений. Таким образом, магнитное квантовое число ml определяет проекцию момента импульса электрона на заданное направление, причем вектор момента импульса электрона в атоме может иметь в пространстве 2l+1 ориентации.
Наличие квантового числа ml должно привести в магнитном поле к расщеплению уровня с главным квантовым числом n на 2l+1 подуровней. Соответственно в спектре атома должно наблюдаться расщепление спектральных линий. Действительно, расщепление энергетических уровней в магнитном поле было обнаружено в 1896 г. голландским физиком П. Зееманом (1865—1945) и получило название эффекта Зеемана. Расщепление уровней энергии во внешнем электрическом поле, тоже доказанное экспериментально, называется эффектом Штарка*.
Хотя энергия электрона (223.3) и зависит только от главного квантового числа n, но каждому собственному значению Еn (кроме E1) соответствует несколько собственных функций nlml, отличающихся значениями l и ml. Следовательно, атом водорода может иметь одно и то же значение энергии, находясь в нескольких различных состояниях. Так как при данном n орбитальное квантовое число l может изменяться от 0 до n - 1 (см. (223.5)), а каждому значению l соответствует 2l+1 различных значений /и/ (223.7), то число различных состояний, соответствующих данному n, равно
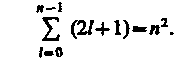 (223.8)
(223.8)
Квантовые числа и их значения являются следствием решений уравнений Шредингера и условий однозначности, непрерывности и конечности, налагаемых на волновую функцию . Кроме того, так как при движении электрона в атоме существенны волновые свойства электрона, то квантовал механика вообще отказывается от классического представления об электронных орбитах. Согласно квантовой механике, каждому энергетическому состоянию соответствует волновая функция, квадрат модуля которой определяет вероятность обнаружения электрона в единице объема.
Вероятность обнаружения электрона в различных частях атома различна. Электрон при своем движении как бы «размазан» по всему объему, образуя электронное облако, плотность (густота) которого характеризует вероятность нахождения электрона в раз личных точках объема атома. Квантовые числа n и l характеризуют размер и форму электронного облака, а квантовое число ml характеризует ориентацию электронного облака в пространстве.
В атомной физике, по аналогии со спектроскопией, состояние электрона, характеризующееся квантовыми числами l = 0, называют s-состоянием (электрон в этом состоянии называют s-электроном), l = 1 — p-состоянием, l = 2 — d-состоянием, l = 3 — f-состоянием и т. д. Значение главного квантового числа указывается перед условным обозначением орбитального квантового числа. Например, электроны в со стояниях с n = 2 и l = 0 и 1 обозначаются соответственно символами 2s и 2р.
На рис. 303 для примера приведено распределение электронной плотности (формы электронного облака) для состояний атома водорода при n=1 и n=2, определяемое |Ynlml |2. Как видно из рисунка, оно зависит от n, l и ml. Так, при l = 0 электронная плотность отлична от нуля в центре и не зависит от направления (сферически-симметрична), а для остальных состояний в центре равна нулю и зависит от направления.

Рис. 303
3. Спектр. Квантовые числа n, l и ml позволяют более полно описать спектр испускания (поглощения) атома водорода, полученный в теории Бора (см. рис. 294).
В квантовой механике вводятся правила отбора, ограничивающие число возможных переходов электронов в атоме, связанных с испусканием и поглощением света. Теоретически доказано и экспериментально подтверждено, что для дипольного излучения электрона, движущегося в центрально-симметричном поле ядра, могут осуществляться только такие переходы, для которых: 1) изменение орбитального квантового числа l удовлетворяет условию
![]() (223.9)
(223.9)
2) изменение магнитного квантового числа Am/ удовлетворяет условию
![]()
В оптических спектрах указанные правила отбора в основном выполняются. Однако в принципе могут наблюдаться и слабые «запрещенные» линии, например возникающие при переходах с l = 2. Появление этих линий объясняется тем, что строгая теория, запрещая дипольные переходы, разрешает переходы, соответствующие излучению более сложных систем зарядов, например квадруполей. Вероятность же квадрупольных переходов (переходы с Dl= 2) во много раз меньше вероятности дипольных переходов, поэтому «запрещенные» линии и являются слабыми.
Учитывая число возможных состояний, соответствующих данному л, и правило отбора (223.9), рассмотрим спектральные линии атома водорода (рис. 304): серии Лаймана соответствуют переходы
![]()
серии Бальмера —
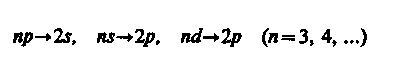
и т.д.
Переход электрона из основного состояния в возбужденное обусловлен увеличением энергии атома и может происходить только при сообщении атому энергии извне, например за счет поглощения атомом фотона. Так как поглощающий атом находится обычно в основном состоянии, то спектр атома водорода должен состоять из линий, соответствующих переходам 1snp (n=2, 3, ...), что находится в полном согласии с опытом.
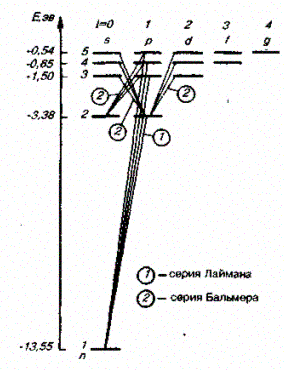
Рис. 304
§ 224. 1s-Состояние электрона в атоме водорода
1s-Состояние электрона в атоме водорода является сферически-симметричным, т. е. не зависит от углов и . Волновая функция ф электрона в этом состоянии определяется только расстоянием r электрона от ядра, т. е.
= Y100(r), где цифры в индексе соответственно указывают, что n = 1, l = 0 и ml = 0. Уравнению Шредингера для 1s-состояния электрона в атоме водорода удовлетворяет функция вида
![]() (224.1)
(224.1)
где, как можно показать, а = h240/(me2) — величина, совпадающая с первым боровским радиусом а (см. (212.2)) для атома водорода, С — некоторая постоянная, определяемая из условия нормировки вероятностей (216.3).
Благодаря сферической симметрии Y-функции вероятность обнаружения электрона на расстоянии r одинакова по всем направлениям. Поэтому элемент объема dV, отвечающий одинаковой плотности вероятности, обычно представляют в виде объема сферического слоя радиусом r и толщиной dr. dV = 4r2dr. Тогда, согласно условию нормировки вероятностей (216.3) с учетом (224.1),
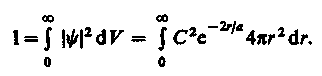
После интегрирования получим
![]() (224.2)
(224.2)
Подставив выражение (224.2) в формулу (224.1), определим нормированную волновую функцию, отвечающую 1s-состоянию электрона в атоме водорода:
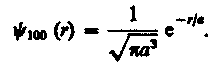 (224.3)
(224.3)
Вероятность обнаружить электрон в элементе объема (см. (216.2)) равна
![]()
Подставив в эту формулу волновую функцию (224.3), получим

Вычислим те расстояния rmax от ядра, на которых электрон может быть обнаружен с наибольшей вероятностью. Исследуя выражение dW/dr на максимум, получим, что rmax = а. Следовательно, электрон может быть обнаружен с наибольшей вероятностью на расстояниях, равных боровскому радиусу, т. е. имеется равная и наибольшая вероятность обнаружения электрона во всех точках, расположенных на сферах радиуса а с центром в ядре атома. Казалось бы, квантово-механический расчет дает полное согласие с теорией Бора. Однако, согласно квантовой механике, плотность вероятности лишь при r = а достигает максимума, оставаясь отличной от нуля во всем пространстве (рис. 305).
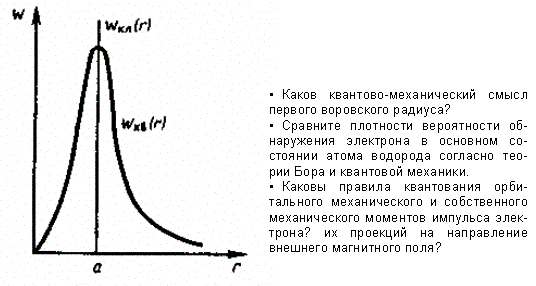
Рис. 305
Таким образом, в основном состоянии атома водорода наиболее вероятным расстоянием от электрона до ядра является расстояние, равное боровскому радиусу. В этом заключается квантово-механический смысл воровского радиуса.
