
- •Оглавление
- •1. Свойства препарата 4
- •2. Средства измерений, вспомогательные устройства, материалы, растворы………...6
- •2.1. Йодометрическое титрование 8
- •Введение
- •1 Свойства препарата
- •2 Средства измерений, вспомогательные устройства, материалы, растворы
- •2.1 Йодометрическое титрование
- •2.2 Спектрофотометрия
- •3 Йодометрический метод анализа
- •3.1 Сущность метода определения
- •3.2. Исходные данные для анализа
- •3.3 Экспериментальная часть
- •3.4 Математическая обработка результатов
- •4 Спектрофотометрический метод определения фурацилина
- •4.1 Сущность метода определения
- •4.2 Экспериментальная часть
- •5 Математическая обработка результатов двух методов
- •Заключение
- •Список используемой литературы
3.3 Экспериментальная часть
Количественное определение фурацилина ГФ рекомендует выполнять йодометрическим методом основанном на окислении препарата йодом в щелочной среде (для улучшения растворимости к смеси прибавляют хлорид натрия):
Фурацилин
при использовании разбавленных растворов
щелочей образует соль, окрашенную в
оранжево – красный цвет:
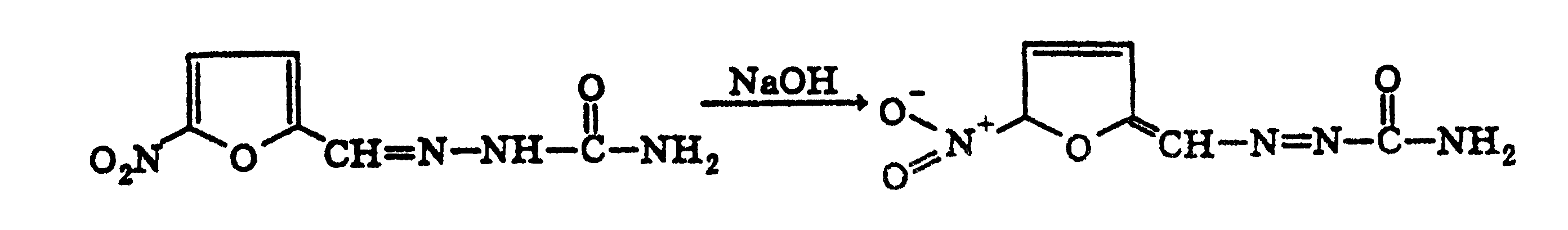 При
нагревании фурацилина в растворах
гидрооксидов щелочных металлов происходит
разрыв фуранового цикла и образуется
карбонат натрия, гидразин и аммиак.
Последний обнаруживают по изменению
окраски влажной лакмусовой бумаги:
При
нагревании фурацилина в растворах
гидрооксидов щелочных металлов происходит
разрыв фуранового цикла и образуется
карбонат натрия, гидразин и аммиак.
Последний обнаруживают по изменению
окраски влажной лакмусовой бумаги:
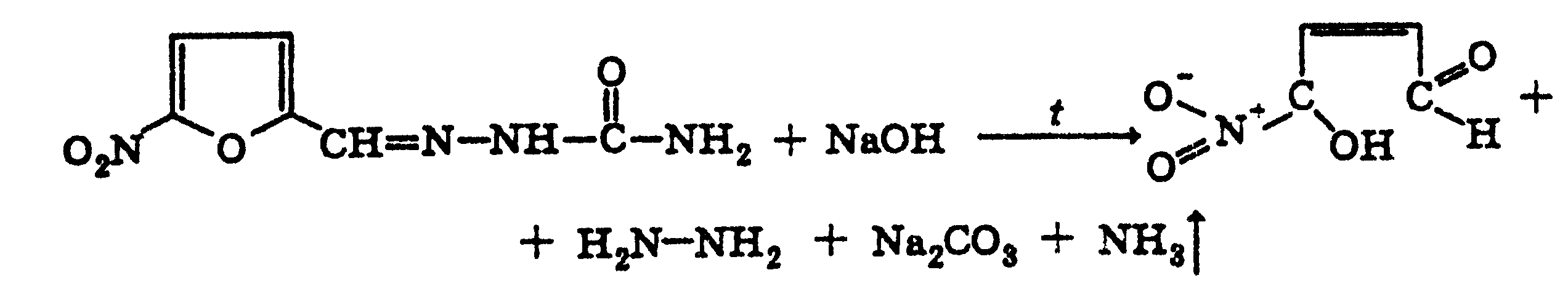
Раствор йода в щелочной среде образует гипойодид:

После окончания процесса окисления препарата раствор подкисляют и титруют выделившийся избыток титрованного раствора йода (обратное титрование):
 ,
,
1) Приготовление раствора
Для приготовления 0,01 н раствора (400 мл) используем 0,1 н раствора .
Необходимый объем 0,1 н раствора находим по формуле V1С1=V2С2,
где С1 - необходимая нормальность ;
V1 - необходимый объем ;
С2 - нормальность исходного раствора ;
V2 - объем раствора необходимый для приготовления заданного раствора;
 мл;
мл;
 мл.
мл.
2) Стандартизация раствора
В качестве первичного стандарта используем раствор K2Cr2O7 0,0525 н. В колбу для титрования наливаем 10 мл раствора H2SO4 2 н, затем 10 мл раствора KY, перемешиваем. Если раствор желтоватый, то добавляем Na2S2O3 по каплям до обесцвечивания. Затем добавляем 5,00 мл-пипеткой раствор K2Cr2O7.Закрываем часовым стеклом и ставим в темное место на 10 минут. Бюретку заполняем раствором Na2S2O3 до метки и титруем 3 раза. Перед титрованием смываем выделившийся на часовом стекле йод дистиллированной водой обратно в колбу.
;
 =0,0525
н ;
=0,0525
н ;
 =5,00
мл;
=5,00
мл;
Объемы раствора тиосульфата натрия Na2S2O3 пошедшие на титрования:
V1=22,00 мл ;
V2=22,10 мл ; Vср=22,20 мл
V3=22,50 мл ;
 н
н
3) Приготовление раствора
Для приготовления 0,01 н раствора (300 мл) используем 0,1 н раствор
Необходимый объем 0,1 н раствора находим по формуле V1С1=V2С2,
где С1 - необходимая нормальность ;
V1- необходимый объем ;
С2 - нормальность исходного раствора ;
V2 - объем раствора необходимый для приготовления заданного раствора;
 мл;
мл;
 мл.
мл.
4)Стандартизация раствора
В колбу для титрования вносим аликвотную часть 0,01н раствора йода (10,00мл). Титруем тиосульфатом натрия до исчезновения окраски. Титрование проводим три раза. Нормальность йода рассчитываем по формуле:
 ;
;
 =0,0118
н;
=0,0118
н;
 =10,00
мл;
=10,00
мл;
Объемы раствора тиосульфата натрия Na2S2O3 пошедшие на титрования:
V1=6,80 мл;
V2=6,80 мл; Vср=6,80 мл
V3=6,80 мл;
 н
н
5)Приготовление раствора фурацилина
Берем 0,8000 г (точная навеска) порошка растертых таблеток, количественно переносим в мерную колбу емкостью 100 мл, прибавляем 70 мл воды, растворяем при 70-80° на водяной бане до получения прозрачного раствора. Охлажденный раствор доводим водой до метки, хорошо перемешиваем.
Навеска: 0,8001 г.
6)Определение массы фурацилина в приготовленном растворе
К 5 мл 0,01 н раствора йода, помещенным в колбу емкостью 50 мл, прибавляем 0,5 мл едкого натра и 5 мл испытуемого раствора. Через 1-2 минуты к раствору прибавляем 2 мл разведенной серной кислоты, добавляем 2-3 капли раствора крахмала и выделившийся йод титруем из бюретки приготовленным раствором тиосульфата натрия .
Объемы, пошедшие на титрование исследуемого раствора:
V1=1,10 мл
V2=1,00 мл
V3=0,90 мл
Массу фурацилина в исследуемом растворе считаем по формуле:
 ;
;
 ;
;
 ;
;

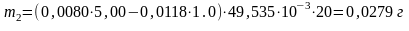

7) Определение массовой доли фурацилина
 ;
;



