
- •12. Выведите формулу для максимальной высоты подъема тела.
- •Движение под действием постоянной силы.
- •Проверка закона сохранения энергии.
- •Адиабатический процесс.
- •Вопросы для самоконтроля.
- •Распределение Максвелла.
- •Цикл Карно.
- •Лабораторная работа №1 Электрическое поле точечных зарядов.
- •Порядок выполнения работы:
- •Эксперимент 2 « Исследование поля диполя.»
- •Лабораторная работа № 2 Теорема Гаусса для расчета электрического поля в вакууме.
- •Порядок выполнения работы:
- •5. Постройте по данным таблицы график зависимости потока вектора напряженности ф от величины заряда .
- •4. По данным таблицы постройте график зависимости потока вектора напряженности ф от расстояния между зарядами.
- •Вывести, используя теорему Гаусса, формулу напряженности бесконечной равномерно заряженной плоскости.
- •Лабораторная работа № 3.
- •Движение заряженной частицы в электрическом поле.
- •Цель работы:
- •7. Выведите формулу для расчета движения заряженной частицы в однородном электрическом поле. Лабораторная работа № 4. Закон Ома для неоднородного участка цепи.
- •11. Можно ли определить сопротивление проводника в этой работе, используя транспортир? Почему?
Вопросы для самоконтроля.
Что называется параметрами состояния?
Какой газ называется идеальным?
Что называется изотермическим процессом? Напишите его формулу.
Что называется изобарным процессом? Напишите его формулу.
Что называется изохорным процессом? Напишите его формулу.
Какой процесс называется адиабатным? Приведите примеры.
Уравнение Пуассона. Коэффициент Пуассона.
Напишите формулу удельной теплоемкости при постоянном давлении.
Напишите формулу удельной теплоемкости при постоянном объеме.
Напишите формулу уравнения Клапейрона –Менделеева.
Что называется внутренней энергией? Как она определяется?
Как находится работа идеального газа?
Что называется степенями свободы?
Лабораторная работа № 5
Распределение Максвелла.
Цель работы:
Знакомство с компьютерной моделью, описывающей поведение молекул идеального газа.
Экспериментальное подтверждение распределения Максвелла молекул идеального газа по скоростям.
Экспериментальное определение массы молекул в данной модели.
Краткая теория:
Вероятностью получения некоторого результата измерения называется предел отношения количества измерений, давших этот результат, к полному числу измерений, когда оно стремится к бесконечности.
![]() -функция распределения
молекул газа по скоростям. Функция
показывает число молекул, скорости
которых лежат в единичном интервале.
Аналитически эту функцию определил
Максвелл:
-функция распределения
молекул газа по скоростям. Функция
показывает число молекул, скорости
которых лежат в единичном интервале.
Аналитически эту функцию определил
Максвелл:
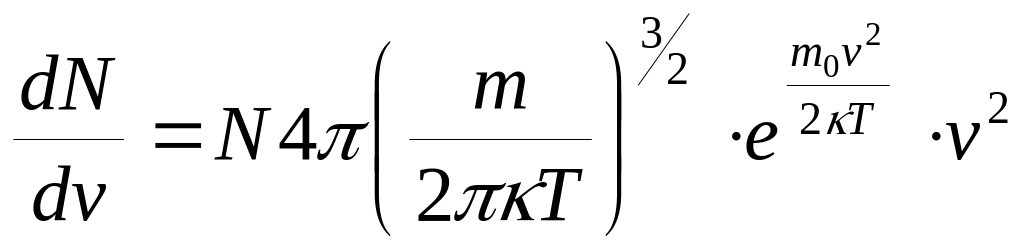
Средняя
скорость
![]()
Средняя
квадратичная скорость
![]()
Вероятнейшая
скорость
![]()
Функция распределения Максвелла дает следующую информацию о газе:
Максимум функции зависит от температуры.
С повышением температуры скорость химических реакций возрастает, при этом возрастает и число молекул, обладающих большими скоростями.
Распределение Максвелла равновесно, т.е. в естественных условиях сохраняется сколь угодно долго.
В равновесном состоянии каждой температуре соответствует своя функция распределения, и наоборот: каждому распределению соответствует своя температура.
Порядок измерений:
Откройте в разделе «Молекулярная физика и термодинамика» работу «Распределение Максвелла».
Установите температуру
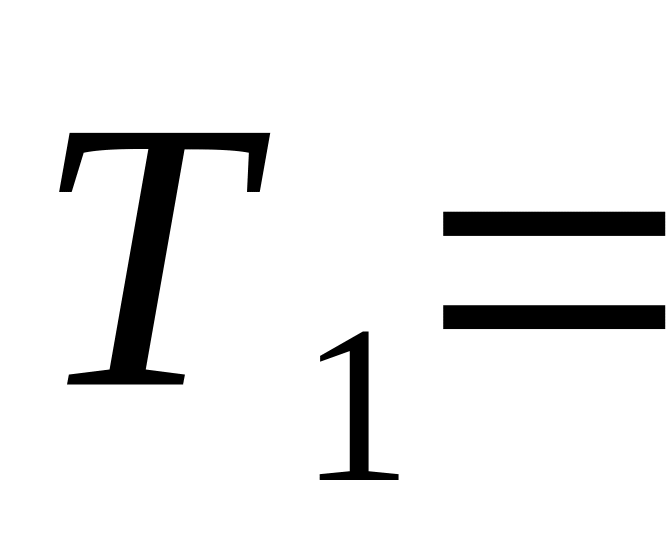 К для вашей бригады. Запишите значение
наивероятнейшей скорости, соответствующей
этой температуре.
К для вашей бригады. Запишите значение
наивероятнейшей скорости, соответствующей
этой температуре.
Установите минимальную скорость, указанную в таблице. Нажмите на «паузу» и подсчитайте на мгновенной фотографии количество молекул
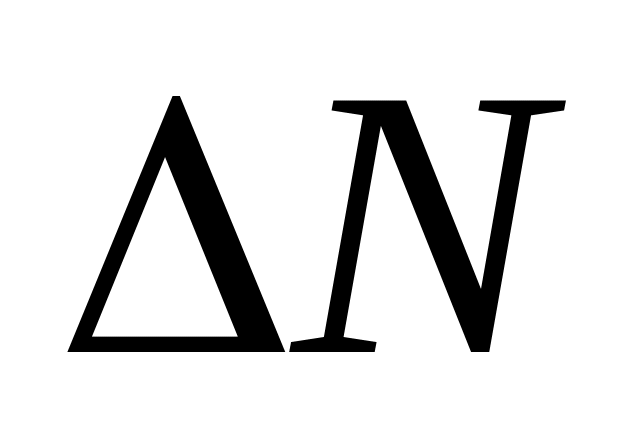 ,
скорости которых лежат в этом диапазоне
скоростей (они выделены зеленым цветом).
Результат занесите в таблицу.
,
скорости которых лежат в этом диапазоне
скоростей (они выделены зеленым цветом).
Результат занесите в таблицу.Нажмите кнопку «пуск» и через 10-20 секунд получите еще одну мгновенную фотографию.
Подсчитайте число молекул с заданной скоростью. Занесите в таблицу. Повторите измерения 5 раз.
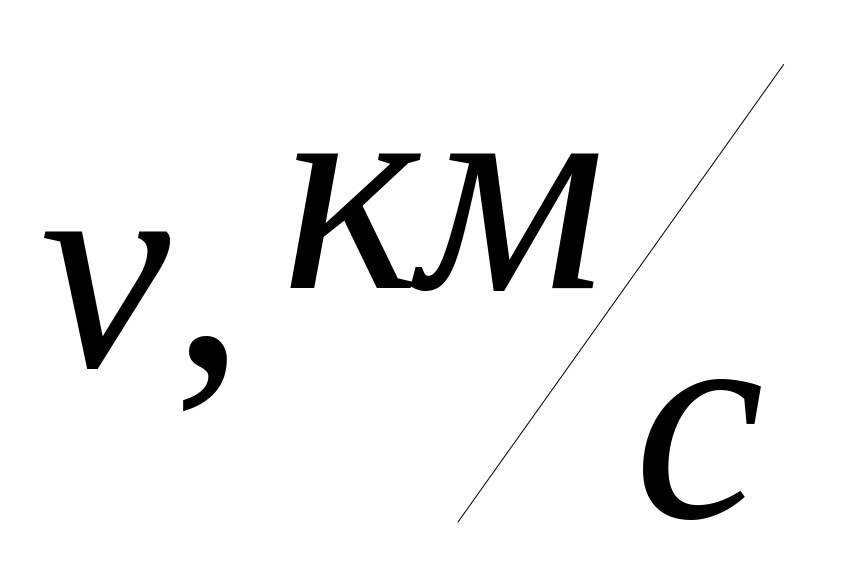
0,5
1,0
1,5
2,0
2,5
3,0
3.5
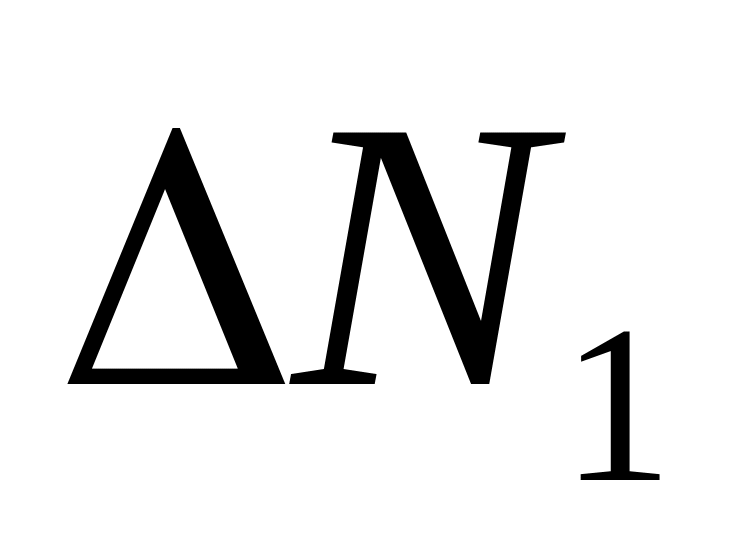
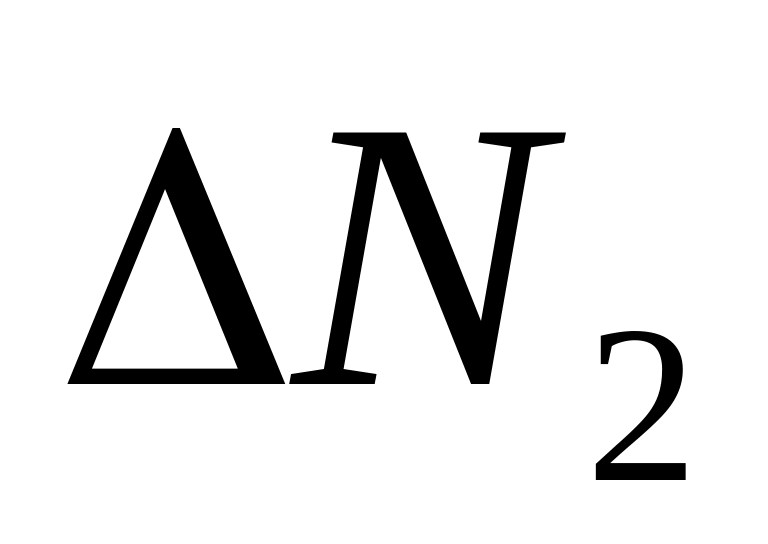
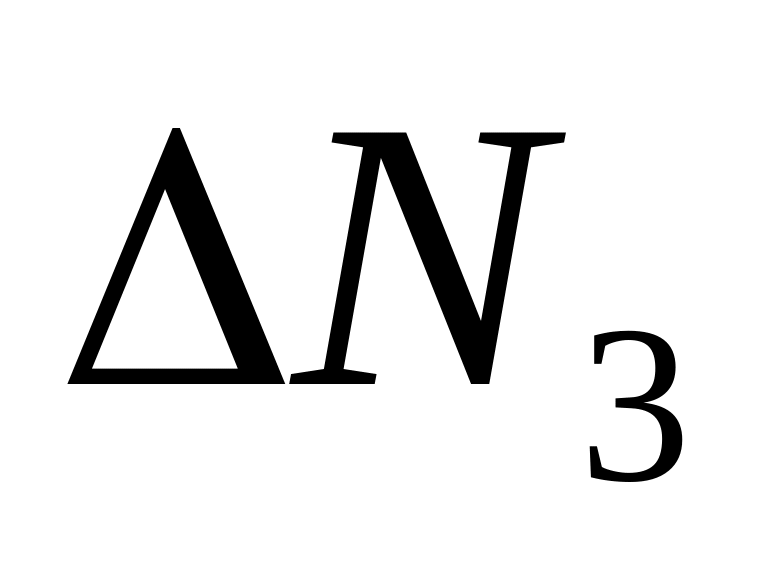
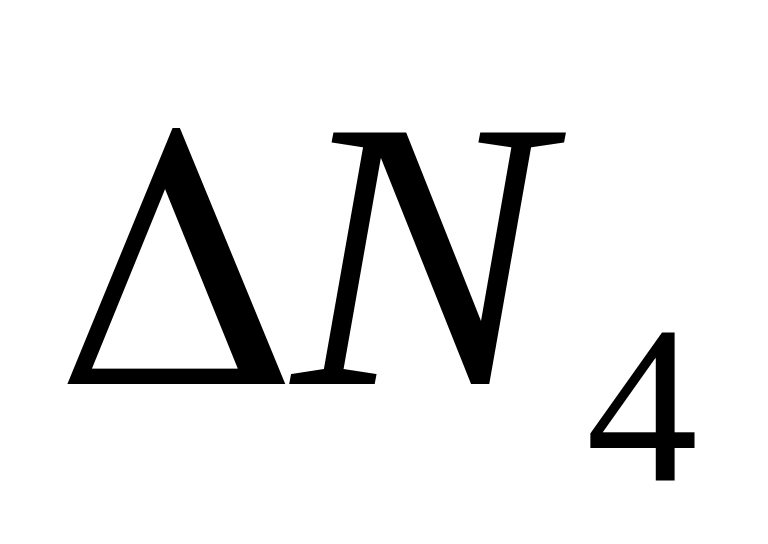
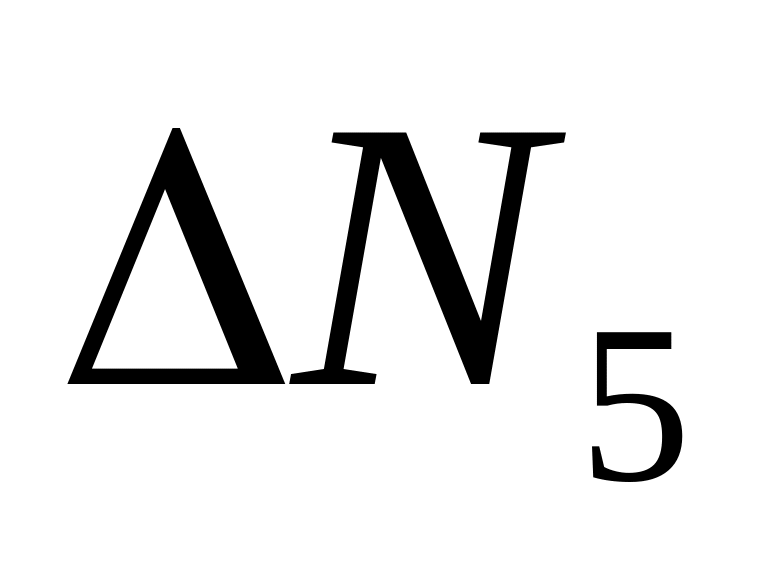
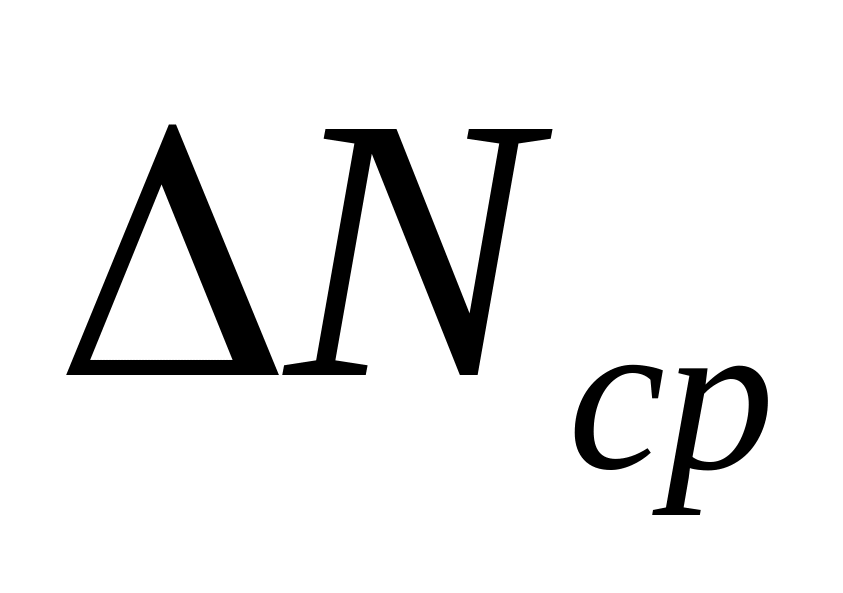
Изменяя скорость на значения, указанные в таблице, запишите количество молекул с заданными скоростями. Заполните всю таблицу.
Найдите средние значения
Установите второе значение температуры Т= К.
Выполните экспериментальное задание аналогично предыдущему, занося результаты в таблицу.
|
0,5 |
1,0 |
1,5 |
2,0 |
2,5 |
3,0 |
3.5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Постройте на одном рисунке графики зависимости
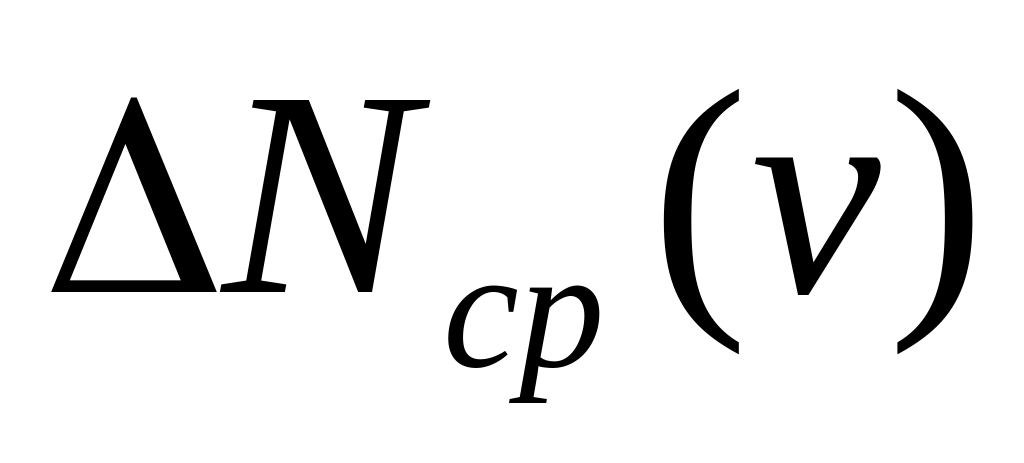 .
Используйте значение вероятнейшей
скорости, данное в работе. Можно
воспользоваться графиком с экрана
компьютера.
.
Используйте значение вероятнейшей
скорости, данное в работе. Можно
воспользоваться графиком с экрана
компьютера.
Для каждой температуры определите экспериментальное значение наивероятнейшей скорости.
![]() м/с,
м/с,
![]() м/с
м/с
Постройте график зависимости квадрата наивероятнейшей скорости от температуры.
По данному графику определите значение массы молекулы, используя формулу:
![]()
12. Подберите газ, масса молекулы которого достаточно близка к измеренной массе газа:
газ |
водород |
гелий |
неон |
азот |
кислород |
Масса
молекулы, |
3.32 |
6.64 |
33.2 |
46.5 |
53.12 |
13. Запишите ответ и проанализируйте графики. _________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Вопросы для самоконтроля
Что называется вероятностью состояния?
Как находится средняя скорость?
Как находится средняя квадратичная скорость?
Как находится вероятнейшая скорость?
В чем смысл распределения Максвелла?
Формула Больцмана.
Барометрическая формула.
Лабораторная работа № 6
