
- •1 Термодинамика. Основные понятия
- •1.2 Термодинамическая система и ее состояние
- •1.4 Тепловое равновесие. Нулевое начало термодинамики
- •1.5 Термометр и эмпирическая температура
- •1.6 Термические и калорические параметры состояния
- •1.8 Обратимые и необратимые процессы
- •1.10 Круговой процесс или цикл. Прямой и обратный цикл
- •2 Первое начало термодинамики
- •3 Газовые смеси
- •4 Второй закон термодинамики
- •5 Политропные процессы
1.4 Тепловое равновесие. Нулевое начало термодинамики
Пусть системы 1 и 2 в отдельности находятся в состоянии теплового равновесия с системой 3. Тогда, если их привести в состояние теплового контакта, то они будут находиться в равновесии друг с другом (рис. 1.1).
Рис. 1.1 К определению
нулевого начала термодинамики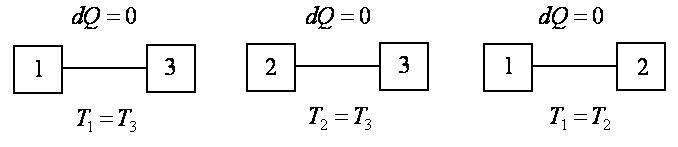
1.5 Термометр и эмпирическая температура
У всех систем, находящихся в тепловом равновесии, температура одинакова. Это свойство может быть использовано для создания приборов по измерению температуры. Обычно их называют термометрами, применение которых основано на том, что два соприкасающихся тела через некоторое время приходят в состояние теплового равновесия, то есть принимают одинаковую температуру.
Существует понятие термодинамической и эмпирической температуры. Эмпирическую температуру обозначают буквой t и ее единицей в системе СИ является градус Цельсия ( С). Термодинамической или абсолютной температурой называется температура, не зависящая от свойств применяемого термометрического вещества и определяемая на основе второго начала термодинамики. Впервые это было сделано Томсоном (лорд Кельвин) в 1848 г. и в его честь шкала абсолютной или термодинамической температуры получила название шкалы Кельвина. Известно, что ее можно воспроизвести с помощью идеального газового термометра. Единица измерения в термодинамической шкале Кельвина – К. Единицы эмпирической и термодинамической шкал температуры равны между собой 1 С =1 К. Термометр представляет собой термометрическое вещество, у которого некоторое свойство изменяется с изменением температуры по известной закономерности, желательно линейной. Это свойство называется термометрическим, например, давление или объем идеального газа, термо-ЭДС, электрическое сопротивление и так далее.
В газовом термометре в качестве термометрического свойства используется либо давление, либо объем.
Для жидкостного, например, ртутного термометра, эмпирическая температура может быть определена из зависимости:
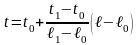 ,
,
если
зафиксированы две реперные (базовые)
точки, для которых измеренным длинам
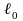 и
и
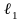 столба жидкости, соответствуют температуры
столба жидкости, соответствуют температуры
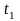 и
и
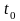 .
.
Связь между эмпирической и термодинамической температурами достаточно проста:
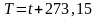 К.
К.
Кроме температуры
Цельсия в англосаксонских странах
пользуются температурной шкалой со
смещенной точкой отсчета – температурной
шкалой Фаренгейта, причем
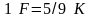 .
В этом случае температуры по Фаренгейту
и Цельсию связаны между собой соотношением:
.
В этом случае температуры по Фаренгейту
и Цельсию связаны между собой соотношением:
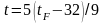 ,
,
где
t –
температура в эмпирической шкале, С;
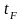 – температура по Фаренгейту, 1
F.
– температура по Фаренгейту, 1
F.
Согласно молекулярно-кинетической теории
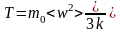 ,
(1.1)
,
(1.1)
где
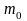 – масса молекулы, кг;
– масса молекулы, кг;
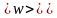 –
средняя квадратичная скорость молекулы,
м/с; k
– константа
Больцмана.
–
средняя квадратичная скорость молекулы,
м/с; k
– константа
Больцмана.
Уравнение (1.1) выведено на основании модели идеального газа, в котором молекулы движутся хаотически так, что температура есть величина пропорциональная средней кинетической энергии теплового движения молекул. Абсолютный ноль температуры должен соответствовать такому состоянию тела, при котором прекращается поступательное движение молекул идеального газа.
