
- •5) Размерная классификация дефектов
- •6)Классификация дефектов по характеру разупорядочения кристаллической решетки,
- •7)Сущность ассоциированных дефектов, a и f – центры
- •13. Законы Фика для диффузии примесных атомов
- •1 0) Примеры взаимодействия дефектов
- •16) Радиационные дефекты.
- •14) Эффекты Френкеля и Киркендала
- •18) Ближний и дальний порядок. Квазикристаллы
1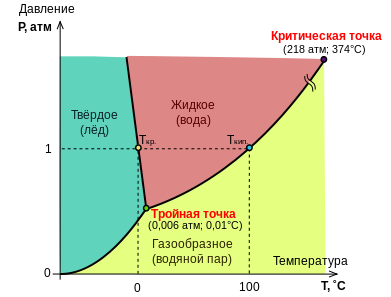 )
Химический компонент…Каждая
совокупность хим. веществ, мысленно
выделенная
из окру- жающей среды и рассматриваемая
как бы изолированно, назы- вается
химической
системой.
Вещества,
из которых состоит химическая система,
называют химическими
компонентами (любое вещество вступившее
в реакцию).
Системы могут быть одно- и многокомпонентными.
Каждый компонент может существовать в
том или ином агрегатном состоянии
(газообразное, жидкое, твердое), каждое
из которых в химии и материаловедении
называют фазой.
Системы,
состоящие из одной фазы, являются
полностью однородными и их называют
гомогенными в противоположность системам
гетерогенным (неоднородным) — состоящим
из более чем одной фазы. Такое определение
фазы является не пол- ным. Оно отражает
понятие фазы в общем, "агрегатном"
смысле. Но в одном и том же образце
твердого тела, напри- мер, в сплаве меди
с цинком могут находиться участки чис-
той меди, чистого цинка и участки
истинного сплава CuZn. Все три компонента
относятся к твердой фазе, но каждое из
них имеет разные химический состав,
кристаллическую. структуру и физические
свойства. Поэтому мы можем гово- рить о
фазах меди, цинка и латуни (CuZn). Таким
образом более полное определение фазы
формулируется как совокупность всех
гомогенных частей системы, отделенных
от других частей (от другой фазы)
поверхностью раздела, при переходе
через которую химический состав или(и)
структура и свойства изменяются скачком.
Классическое определение фазы: гомогенная
часть
гетерогенной системы, ограниченная
поверхностью раздела.
Фаза
вещества определяется температурой и
давлением, а ФАЗОВАЯ ДИАГРАММА показывает
связь между фазами при изменении
температуры и давления. Изменение во
внутренней ЭНЕРГИИ вещества вызывает
фазовый переход (изменение агрегатного
состояния), наблюдаемое, например, при
плавлении или кипении.
)
Химический компонент…Каждая
совокупность хим. веществ, мысленно
выделенная
из окру- жающей среды и рассматриваемая
как бы изолированно, назы- вается
химической
системой.
Вещества,
из которых состоит химическая система,
называют химическими
компонентами (любое вещество вступившее
в реакцию).
Системы могут быть одно- и многокомпонентными.
Каждый компонент может существовать в
том или ином агрегатном состоянии
(газообразное, жидкое, твердое), каждое
из которых в химии и материаловедении
называют фазой.
Системы,
состоящие из одной фазы, являются
полностью однородными и их называют
гомогенными в противоположность системам
гетерогенным (неоднородным) — состоящим
из более чем одной фазы. Такое определение
фазы является не пол- ным. Оно отражает
понятие фазы в общем, "агрегатном"
смысле. Но в одном и том же образце
твердого тела, напри- мер, в сплаве меди
с цинком могут находиться участки чис-
той меди, чистого цинка и участки
истинного сплава CuZn. Все три компонента
относятся к твердой фазе, но каждое из
них имеет разные химический состав,
кристаллическую. структуру и физические
свойства. Поэтому мы можем гово- рить о
фазах меди, цинка и латуни (CuZn). Таким
образом более полное определение фазы
формулируется как совокупность всех
гомогенных частей системы, отделенных
от других частей (от другой фазы)
поверхностью раздела, при переходе
через которую химический состав или(и)
структура и свойства изменяются скачком.
Классическое определение фазы: гомогенная
часть
гетерогенной системы, ограниченная
поверхностью раздела.
Фаза
вещества определяется температурой и
давлением, а ФАЗОВАЯ ДИАГРАММА показывает
связь между фазами при изменении
температуры и давления. Изменение во
внутренней ЭНЕРГИИ вещества вызывает
фазовый переход (изменение агрегатного
состояния), наблюдаемое, например, при
плавлении или кипении.
2) Отличие… Хими́ческая реа́кция— превращение одного или нескольких исходных веществ (реагентов) в отличающиеся от них по химическому составу или строению вещества (продукты реакции). В отличие от ядерных реакций, при химических реакциях ядра атомов не меняются, в частности не изменяется их общее число, изотопный состав химических элементов, при этом происходит перераспределение электронов и ядер и образуются новые химические вещества. Фа́зовый перехо́д (фазовое превращение) в термодинамике — переход вещества из одной термодинамической фазы в другую при изменении внешних условий. С точки зрения движения системы по фазовой диаграмме при изменении её интенсивных параметров (температуры, давления и т. п.), фазовый переход происходит, когда система пересекает линию, разделяющую две фазы. Поскольку разные термодинамические фазы описываются различными уравнениями состояния, всегда можно найти величину, которая скачкообразно меняется при фазовом переходе. Поскольку разделение на термодинамические фазы — более мелкая классификация состояний, чем разделение по агрегатным состояниям вещества, то далеко не каждый фазовый переход сопровождается сменой агрегатного состояния. Однако любая смена агрегатного состояния есть фазовый переход. Превращения с изменением состава называют химическими реакциями, а без изменения состава — фазовыми превращениями. Наиболее характерным количественным параметром, определяющим химическую реакцию, является ее скорость.
3) Физико-химический анализ — комплекс методов анализа физико-химических систем путем построения и геометрического анализа диаграмм состояния и диаграмм состав-свойство. Этот метод позволяет обнаружить существование соединений (например, медистого золота CuAu), существование которых невозможно подтвердить другими методами анализа.
Два основные принципа ФХА. а. были сформулированы Н.С. Курнаковым. Согласно принципу соответствия, (1)каждой совокупности фаз, находящихся в данной системе в равновесии в соответствии с фаз правилом, на диаграмме отвечает определенный геом. образ. На основании этого принципа Н.С. Курнаков определил ФХА. как геометрический метод исследования химический превращений. Второй основной принцип ФХА., называют принципом непрерывности, формулируется следующей образом: (2)при непрерывном изменении параметров, определяющих состояние системы, свойства отдельных ее фаз изменяются непрерывно. Св-ва же системы в целом изменяются также непрерывно, но при условии, что не возникают новые фазы и не исчезают старые; если же число фаз меняется, то изменяются и свойства системы, причем, как правило, скачкообразно. Третий принцип ФХА был предложен Я.Г. Горощенко. Он утверждает, что (3)любой набор компонентов, независимо от их числа и физических-химический свойств, может составить систему (принцип совместимости). Из него следует, что диаграмма любой системы содержит все элементы частных систем (подсистем), из которых она составлена. В общей системе элементы трансляции частных систем совмещаются с геометрическая образами на химический диаграмме, возникающими как отображение процессов, протекающих с участием всех компонентов общей системы. В современном ФХА. число используемых свойств системы составляет много десятков. В принципе можно применять любое свойство, которое может быть измерено или вычислено. Например, при решении теоретич. вопросов, в частности при выводе различные типов диаграмм, используют к.-л. термодинамическое потенциал, который не может быть измерен непосредственно. При выборе свойства необходимо учитывать как возможную точность определения его значений, так и его чувствительность к происходящим в системе химический превращениям. Например, плотность вещества может быть определена с большой точностью, но она малочувствительна к образованию химический соединение, тогда как твердость чутко реагирует на химический взаимодействие в системе, однако мала точность ее определения. Для ФХА. характерно параллельное исследование и сопоставление результатов определения несколько свойств, например электропроводности, твердости. Фазовые диаграммы состояний являются неотъемлемой частью любого обсуждения свойств материалов в тех случаях, когда речь идет о взаимодействии различных материалов. Особенно фазовые диаграммы состояния важны в микроэлектронике, т.к. для изготовления выводов и пассивирующих слоев там приходится использовать большой набор различных материалов. В производстве интегральных микросхем в тесном контакте с различными металлами находится кремний, особое внимание уделим тем фазовым диаграммам, в которых в качестве одной из компонент фигурирует именно кремний.
5) Размерная классификация дефектов
Прежде всего следует различать макро- и микродефекты. Первые легко видны в микроскоп. Примеры таких макродефектов — поры, трещины и раковины в металлических отливках, посторонние включения примесных скоплений, видимые грани- цы отдельных кристаллитов — зерен поликристалла. К микродефектам или дефектам, рассматриваемым на атом- ном уровне, относят такие, у которых хотя бы один из трех его размеров (дг, j, z) сравним с периодом решетки а = 0,2-5- 0,5 нм. кристаллической. Любое нарушение внутрикристаллического поля и есть дефект.
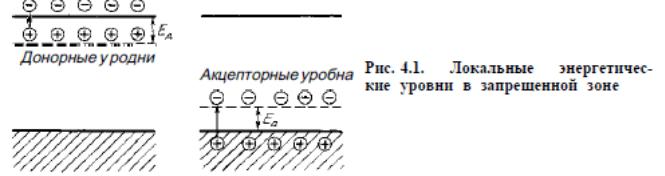
Если дефектов в кристалле немного, то они находятся назначительных расстояниях один от другого, т.е. дефекты решетки кристалла в этом случае локализованы. По- этому изменяются энергетические состояния только тех электронов, которые находятся в этой области, что приводит к образованию локальных энергетических состояний, на- кладывающихся на идеальную зонную структуру твердого те- ла. Число таких локальных состояний либо равно числу де- фектов, либо превышает его, Важной чертой, присущей дефектам, является связь ло- кальных состояний — энергетических уровней с электронами. В металлах, зонная структура которых не имеет за- прещенной зоны, электронные уровни примесных атомов могут попадать в заполненную или свободную часть валентной зоны. И в ме- таллах наиболее вероятным является ионизированное состоя- ние дефектов, свободных от электронов. Иначе обстоит дело в полупроводниках и диэлектриках, Дефекты, способные при ненарушенных валентных связях в кристалле отдавать электроны в зону проводимости, называ- ют донорами, а полупроводники, содержащие доноры, называ- ют полупроводниками с электронной электропроводностью, или полупроводниками л-типа. Если при нагревании кристалла электроны из валентной зоны могут переходить на уровни дефектов, то в валентной зоне возникает дырочная электропроводность. Дефекты, способные воспринимать электроны из валентной зоны, называют акцепторами, а полупроводник, содержащий акцепторы, называют или полупроводником с дырочной электропроводностью, или полупроводником p-типа.
а) точечные (нульмерные) дефекты, у которых х < а, у < а и z < а; б) линейные (одномерные) дефекты, которые малы (< а) в двух направлениях и сколь угодно протяженные в третьем направлении в пространстве (»а); в) плоские (<двумерные) дефекты, которые малы в одном направлении. Объемные (трехмерные) дефекты в этой классификации не рассматриваются, так как относятся практически уже к макродефектам. В эту размерную классификацию необходимо еще включить так называемые ассоциированные дефекты, представляющие собой ассоциации в единый дефект нескольких одинаковых или разных дефектов, например, дивакансии V2 или ионные пары примесных атомов А++В~—АВ,
6)Классификация дефектов по характеру разупорядочения кристаллической решетки,
Наиболее важными при-
мерами собственного разупорядочения являются электронные
и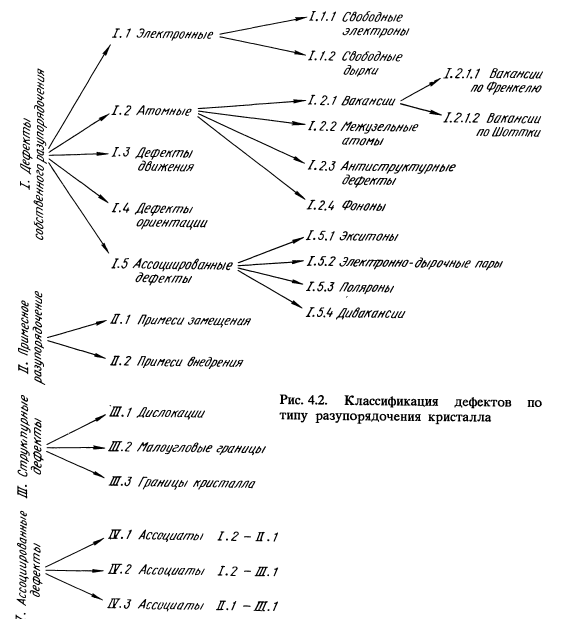 атомные дефекты. Они — прямые участники
разных превращений в твердых телах —
диффузии, распада твердых раство- ров
и др. Однако известны и другие дефекты
собственного разупо- рядочения, например,
дефекты
движения,
представляющие собой группу атомов,
которые вращаются не в фазе с основной
массой атомных групп кристалла.
атомные дефекты. Они — прямые участники
разных превращений в твердых телах —
диффузии, распада твердых раство- ров
и др. Однако известны и другие дефекты
собственного разупо- рядочения, например,
дефекты
движения,
представляющие собой группу атомов,
которые вращаются не в фазе с основной
массой атомных групп кристалла.
АТОМНЫЕ 1)вакансии-узлы, из которых удалился атом. Физическая природа образования вакансий связана с тепловыми колебаниями атомов кристалла. После перехода атома из узла в межузлие возможен, конечно, и обратный переход - рекомбинация, т.е. возврат атома в свободный узел. Но есть и другая возможность — диффузия атома из ближайшего к вакансии межузлия в более удаленные. Таким образом возникают пары вакансия — межузельный атом, называемые френкелевскими. Сами вакансии этого типа называют вакансиями по Френкелю. Если вакансия, диффундируя по кристаллу, выйдет на по- верхность, то в нее способен перескочить атом из более глубокого атомного слоя. В освободившуюся вакансию перейдет атом из следующего слоя и в результате в кристалле окажутся вакансии без межузельных атомов. Вакансии такого типа получили название вакансий по Шоттки1. Аналогичная ситуация возникает и при выходе на поверхность кристалла из глубины межузельного атома. С увеличением температуры количество вакансий должно возрастать. Если выдержать кристалл некоторое время при высокой температуре, т.е. образовать в нем большое количество вакансий, а затем быстро его охладить (такой режим называют закалкой), то повышенное количество вакансий заморозится и кристалл будет содержать повышенное неравновесное количество вакансий. Процесс исчезновения замороженных вакансий при нагревании с выдержкой во времени называют отжигом. Образование точечных дефектов может зависеть не только от температуры, но и от давления. 2) Межузельные атомы-Антиструктурные образуются в случае попадания некоторого количества атомов А в "чужую" подрешетку В кристаллического соединения АВ. Такой вид дефектов более вероятен в металлических сплавах и в сложных полупроводниковых соединениях типа А В , в которых доля ионнои связи незначительна. В более ионных кристаллах слишком велики энергетические барьеры для замещения одноименно заряженных с ним свобод- ных вакансий в противоположной подрешетке. Эти барьеры обусловлены электростатическими силами отталкивания. Вообще, установлено, что антиструктурные дефекты возникают в соединениях с близкими размерами атомов в различных подрешетках кристалла. Фононы кванты колебательного движения атомов кристалла. Корпускулярные свойства волн проявляются в существовании наименьшей порции (кванта) колебаний атомов кристалла с данной частотой. При таком подходе изменение энергии колебаний (волны) на одну такую порцию — квант колебаний рассматривается как появление или исчезновение особой квазичастицы — фонона, имеющего энергию Е = hω и движущегося со скоростью звука. Фононы обладают и импульсом р = hq. Более строго, вектор р не импульс, а лишь квазиимпульс. Экситоны (электрон и дырка, удерживаемые в виде единого нейтрального центра). Экситон в какой-то мере аналогичен атому водорода в воз- бужденном (предыонизационном) состоянии, в котором элек- трон и протон еще остаются связанными. Экситон может иметь большое время жизни, в течение которого он может диффундировать в кристалле на значительные расстояния. Кроме экситонов могут существовать электронно-дырочные пары, отличающиеся от экситонов тем, что электроны и дыр- ки, составляющие пару, находятся в основных, а не в возбужденных энергетических состояниях.
…
Примесное разупорядочение Чужеродные примесные атомы с матрицей основного кристалла могут образовывать либо твердые растворы замещения, либо твердые растворы внедрения. В первом случае примесные атомы находятся в узлах кристаллической решетки, во втором — в межузлиях. Та или другая ситуация за- висит в основном от двух факторов: геометрического и электрохимического. Формулировка геометрического фактора: растворы замещения образуют лишь те атомы, радиусы которых отличаются от радиусов матричных атомов не более чем на 15 %. Электрохимический фактор: Для образования растворов замещения необходимо, чтобы атомы примеси и матрицы были электрохимически подобны, т.е. находились бы не слишком далеко в ряду напряжений, хорошо известном в химии. Если атомы примеси и матрицы-растворителя далеко от- стоят в ряду напряжений, то один из них будет слишком электроположителен, а другой электроотрицателен, что при- ведет скорее к образованию химического соединения, а не к твердому раствору. Количественной характерисгикой электрохимического фактора является разность электроотрицательностей примесного и матричного атомов. Для образования растворов замещения необходимо, чтобы эта разность была мала. Правило Хэгга: Отношение радиуса внедряющегося атома к радиусу атома матрицы должно быть меньше чем 0,59, т.е. разница в атомных диаметрах должна быть > 41 % диаметра большего из атомов. Таким образом, если отношение гП/гм, где гп — радиус примесного атома, гм — радиус матричного атома, заключено в пределах 0 < гп/гм < 0,59, то примесь образует раствор внедрения, а если 0,85 < гп/гм < 1,15, то — раствор замещения. Область же 0,59 < r n / rM < 0,85 вообще не благоприятна для образования твердых растворов
