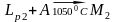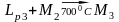- •1 Построение диаграммы состояния а-в-с
- •1.1 Анализ граничных двойных систем
- •1.2 Анализ фазовых равновесий в трехкомпонентной системе с промежуточными одной конгруэнтно плавящейся и тремя инконгруэнтно плавящимися фазами
- •2 Составление структурной схемы фазовых равновесий в тройной системе а-в-с
- •3 Проекция поверхностей ликвидуса. Нанесение изотерм на поверхности ликвидуса в трёхкомпонентной системе
- •4 Построение изотермических разрезов
- •4.1 Построение изотермического разреза при комнатной температуре без растворимости в твердом состоянии
- •4.2 Построение изотермического разреза при комнатной температуре с растворимостью компонентов друг в друге и в промежуточных фазах
- •5 Построение политермических разрезов
- •5.1 Политермический разрез I – b
- •5.2 Политермический разрез II – II
- •6 Фазовые превращения в сплавах
- •6.1 Сплав 1 (42%а, 3%в, 55%с)
- •6.2 Сплав 2 (47%а, 46%в, 7%с)
- •Список используемой литературы:
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ
ГОСУДАРСТВЕННОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
«МАТИ» - РОССИЙСКИЙ ГОСУДАРСТВЕННЫЙ ТЕХНОЛОГИЧЕСКИЙ УНИВЕРСИТЕТ имени К.Э. ЦИОЛКОВСКОГО
Кафедра «Материаловедение и технология обработки материалов»
РАССЧЁТНО-ГРАФИЧЕСКАЯ РАБОТА
по дисциплине «Современные проблемы науки в области материаловедения и технологии материалов и покрытий»
на тему: «Анализ фазовых равновесий в трехкомпонентной системе с промежуточными конгруэнтно плавящимся и тремя инконгруэнтно плавящимися фазами».
Вариант №
Выполнил: Егенмамедов Х.О.
Группа: 4МТМ – 5ДМ – 093
Проверил: Осинцев О.Е.
Москва, 2012г.
СОДЕРЖАНИЕ:
Задание……………………………………………..……………………………
1. |
Построение диаграммы состояния тройной системы А–В–С…………...
|
|
2. |
Составление структурной схемы фазовых равновесий в трёхкомпонентной системе………………………………………………... |
|
3. |
Проекция поверхностей ликвидуса. Нанесение изотерм на поверхности ликвидуса в трёхкомпонентной системе…………………. |
|
4.
5.
6.
|
Построение изотермических разрезов………………………………….. 4.1. Построение изотермического разреза при комнатной температуре без растворимости в твёрдом состоянии………….….. 4.2. Построение изотермического разреза при комнатной температуре с растворимостью компонентов друг в друге и в промежуточных фазах ………………………………….…………… 4.3. Построение изотермического разреза при Т=640ºС………………… Построение политермических разрезов………………………………….. 5.1. Политермический разрез I–А …………………………………,...…… 5.2. Политермический разрез II–II………………………………………... Фазовые превращения в сплавах………………...………………………... 6.1. Сплав 1 (42%А, 3%В, 55%С)…………………………………… 6.2. Сплав 2 (47%А, 46%В, 7%С)………… ……………………………. |
|
|
Список используемой литературы………………………………………... |
|
1 Построение диаграммы состояния а-в-с
Построение диаграммы состояния системы А-В-С начинаем с анализа граничных двойных систем.
1.1 Анализ граничных двойных систем
Согласно заданию, в двойных системах существуют следующие фазы:
Система А-В:
L – жидкий раствор компонентов А и В друг в друге;
А – однокомпонентная твердая фаза;
В – однокомпонентная твердая фаза;
М1 – промежуточная инконгруэнтно плавящаяся фаза постоянного состава;
Система В-С:
L – жидкий раствор компонентов В и С друг в друге;
В – однокомпонентная твердая фаза;
С – однокомпонентная твердая фаза;
S1 – промежуточная конгруэнтно плавящаяся фаза постоянного состава;
Система А-С:
L – жидкий раствор компонентов А и С друг в друге;
А – однокомпонентная твердая фаза;
С – однокомпонентная твердая фаза;
М2 – промежуточная инконгруэнтно плавящаяся фаза постоянного состава;
М3 – промежуточная инконгруэнтно плавящаяся фаза постоянного состава;
По этим данным строим диаграммы состояния систем А-В, В-С и А-С во всех возможных вариантах последовательности нонвариантных реакций, изображенных на рис. 1. Для каждой граничной двойной системы выбираем один вариант:
- для системы А-В – из двух возможных вариантов выбираем вариант “а”;
- для системы В-С – единственно возможный вариант “в” ;
- для системы А-С – из трех возможных вариантов выбираем вариант “е”.
В двойных системах существуют следующие нонвариантные равновесия:
В системе А-В:
- перитектическая
реакция
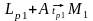 ;
;
- эвтектическая
реакция
 .
.
В системе В-С:
- эвтектическая
реакция
 .
.
- эвтектическая
реакция
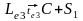 .
.
В системе А-С:
- перитектическая
реакция
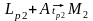 ;
;
- перитектическая
реакция
 ;
;
- эвтектическая
реакция
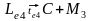 .
.
1.2 Анализ фазовых равновесий в трехкомпонентной системе с промежуточными одной конгруэнтно плавящейся и тремя инконгруэнтно плавящимися фазами
В тройной системе А–В–С существуют 8 фаз:
L – жидкий раствор компонентов А, В, С друг в друге;
А – однокомпонентная твёрдая фаза;
В – однокомпонентная твёрдая фаза;
С – однокомпонентная твёрдая фаза;
S1 – промежуточная конгруэнтно плавящаяся фаза постоянного состава в системе B-C. Состав: 50%A, 50%B.
М1 – промежуточная инконгруэнтно плавящаяся фаза постоянного состава в системе А–В. Состав: 40%А, 60%В.
М2 – промежуточная инконгруэнтно плавящаяся фаза постоянного состава в системе C-A. Состав: 90%C, 10%A.
М3 – промежуточная инконгруэнтно плавящаяся фаза постоянного состава в системе C-A. Состав: 50%C, 50%A.
Растворимость компонентов друг в друге в твердом состоянии пренебрежительно мала, поэтому ее не учитываем. На стороны концентрационного треугольника наносим точки, отвечающие составам промежуточных фаз (S1, M1, M2, M3), перитектических (р1, р2, р3) и эвтектических (е1, е2, е3, е4) нонвариантных точек в двойных системах.
По правилу фаз Гиббса трехфазные нонвариантные равновесия для двойных систем являются для тройных систем моновариантными (с = f–k +1 = =3–3+1 = 1) , поэтому из нонвариантных точек двойных систем (р1, р2, р3, е1, е2, е3, е4) будут выходить моновариантные линии, отвечающие трехфазным равновесиям в тройной системе. Моновариантные линии будут пересекаться в точках, которые будут нонвариантными для тройной системы. Эти точки будут определять состав жидкой фазы, участвующей в четырехфазных нонвариантных равновесиях.
При вычерчивании проекции тройной системы необходимо помнить:
четырехфазные реакции совместимы в одной трехфазной системе, если между ними имеется одно общее трехфазное равновесие с одинаковым набором фаз для двух соседних четырехфазных равновесий;
если нонвариантное равновесие перитектическое, то к точке нонвариантного равновесия подходят 2 моновариантные линии, а выходит из нее одна, а если нонвариантное равновесие эвтектическое, то в точке нонвариантного равновесия сходятся 3 моновариантные линии;
конгруэнтно плавящиеся фазы и твердые растворы на основе компонентов всегда находятся в области проекции ликвидуса этих фаз; инконгруэнтно плавящиеся фазы всегда лежат вне проекции ликвидуса этих фаз;
центром кривизны моновариантных линий является более тугоплавкий компонент;
четырехфазным перитектическим равновесиям на плоскости концентрационного треугольника отвечают четырехугольники, а эвтектическим равновесиям − треугольники, указывающие состав участвующих в равновесии фаз;
метастабильные продолжения моновариантных линий ликвидуса должны проходить между двумя другими линиями ликвидуса фаз, участвующих в нонвариантном превращении.
Учитывая всё выше сказанное, был выбран вариант системы, в которой имеются следующие 5 четырёхфазных нонвариантных превращения:
Перитектические:
LP1+A
 М1+M2,
этому превращению отвечает четырехугольник
P1M1AM2;
М1+M2,
этому превращению отвечает четырехугольник
P1M1AM2;
LP2+М1
 S1+М2,
этому превращению отвечает четырехугольник
P2S1М1M2;
S1+М2,
этому превращению отвечает четырехугольник
P2S1М1M2;LP3+B
 S1+M1,
этому превращению отвечает четырехугольник
P3S1
BМ1;
S1+M1,
этому превращению отвечает четырехугольник
P3S1
BМ1;LP4+M2 S1+M3, этому превращению отвечает четырехугольник P4S1M2M3;
Эвтектическое:
LE1→С+S1+M3, этому превращению отвечает треугольник CS1M3;
Диаграммы состояния граничных двойных систем А-В, В-С и А-С представлены на рис. 2,3,4 соответственно.
Составы промежуточных фаз и нонвариантных точек и температуры нонвариантных равновесий в системе А–В–С представлены в таблице 1.
Проекция диаграммы состояния А-В-С на плоскость концентрационного треугольника представлена на рис. 5, рис. 6.
Проверка соответствия законам термодинамики положения нонвариантных точек на проекции в системе А-В-С: каждая перитектическая точка находится вне конодного треугольника, построенного на составах твёрдых фаз, а эвтектическая точка находится внутри конодного треугольника.
Таблица 1. Химический состав фаз, участвующих в реакциях.
Система, реакция
|
Химический состав фаз, % |
||||||||||||||
I |
II |
III |
IV |
||||||||||||
A |
B |
C |
A |
B |
C |
A |
B |
C |
A |
B |
C |
||||
Система ABC |
|||||||||||||||
LP1+A М1+M2 |
54 |
23 |
23 |
100 |
0 |
0 |
40 |
60 |
0 |
90 |
0 |
10 |
|||
LP2+М1 S1+М2 |
26 |
28 |
46 |
40 |
60 |
0 |
0 |
50 |
50 |
90 |
0 |
10 |
|||
LP3+B S1+M1 |
18 |
45 |
37 |
0 |
100 |
0 |
0 |
50 |
50 |
40 |
60 |
0 |
|||
LP4+M2 S1+M3 |
24 |
20 |
56 |
90 |
0 |
10 |
0 |
50 |
50 |
50 |
0 |
50 |
|||
Cистема А-В
|
35 |
65 |
- |
100 |
0 |
- |
40 |
60 |
- |
- |
- |
- |
|||
|
27 |
73 |
- |
0 |
100 |
- |
40 |
60 |
- |
- |
- |
- |
|||
Система В-С
|
- |
60 |
40 |
- |
100 |
0 |
- |
50 |
50 |
- |
- |
- |
|||
|
- |
27 |
73 |
- |
0 |
100 |
- |
50 |
50 |
- |
- |
- |
|||
Система А-С
|
80 |
- |
20 |
100 |
- |
0 |
10 |
- |
90 |
- |
- |
- |
|||
|
40 |
- |
60 |
10 |
- |
90 |
50 |
- |
50 |
- |
- |
- |
|||
|
82 |
- |
18 |
0 |
- |
100 |
50 |
- |
50 |
- |
- |
- |
|||
Примечание: цифры I-IV порядковый номер фазы.