
Синдром ломкой хромосомы х и особенности ээг при этом синдроме.
. Синдром FXS является наиболее часто встречаемой наследуемой формой умственной отсталости (после синдрома Дауна). Интерес к этому сцепленному с полом заболеванию значительно возрос в последнее время. Это связано с его широкой распространенностью, возможностью предотвратить рождение больных детей с помощью пренатальной диагностики и, главное, появившейся в самое последнее время надеждой на терапию. В 1969 году была выявлена цитогенетическая аномалия Х хромосомы в виде ломкости ее дистального фрагмента (Lubs,1969) у больных с сцепленной с полом умственной отсталости, а в 1991 году группой ученых был выделен ген FMR1, мутация в котором и вызывает это заболевание. Мутация в гене умственной отсталости с ломкой хромосомой Х (FMR1) , является причиной двух заболеваний: синдрома ломкой хромосомы Х (FXS), который возникает при полной мутации FMR1 (количество повторов в промоторе более 200), и синдрома тремора и атаксии ассоциированного с ломкой хромосомой Х (FXS /АТ) у части индивидуумов с премутацией (количестве повторов от 55 до 200) (Hagerman et al,2004). Обычно при полной мутации происходит метилирование промотора и транскрипция гена FMR1 практически прекращается. Дефицит белка FMR1 (FMRР) приводит к нарушению функционирования многих генов и проявляется определенным физическим и поведенческим фенотипом, который включает: большие уши, удлиненное лицо, гиперэластичность кожи, макроорхизм( очевиден после пубертата), умственную отсталость (УО) и эпилептические приступы, гиперактивность и дефицит внимания (СДВГ), высокий уровень тревожности и аутистические проявления. Частота встречаемости с полной мутацией и УО составляет 1: 4 000 мужчин и 1: 6 000 женщин. Белок, который отсутствует при этом синдроме является РНК связывающим и транспортным белком, регулирующим трансляцию многих посредников, важных для синаптической пластичности. В норме этот белок (FMRP) ингибирует трансляцию этих посредников и, следовательно, его отсутствие приводит к их увеличению. FMRP является ингибитором метаботоропного глютаматергического рецептора, отвечающего за долговременную депрессию. Отсутствие белка приводит к ее увеличению и ослаблению синаптических контактов и даже синаптической элиминации, что и приводит к описанному выше поведенческому фенотипу. Использование антагонистов глютаматергического рецептора приводит к восстановлению синаптических шипиков, способности к обучению и улучшению поведения на животных моделях. В 2008 году опубликованы первые результаты применения такого рода антагонистов на больных с синдромом ломкой хромосомы Х (Hagerman и др.,2008). Было доказано улучшение поведения и когнитивных функций у этих больных в результате терапии, но эффект был краткосрочным и в настоящее время этот препарат не используется. В настоящее время идет испытание ряда препаратов, которые улучшают функционирование мозга при этой патологии за счет активации активности ГАМК-эргической системы.
Другой причиной аутизма при нарушении функционирования гена FMR-1 является премутация ФРАХ, но механизм здесь иной и связан с токсичностью РНК. Нейроны с премутацией более чувствительны к воздействиям среды и окислительному стрессу, приводящему к гибели клеток. Поведенческий фенотип при этом заболевании включает у детей трудности школьного обучения, синдром гиперактивности с дефицитом внимания, расстройства аутистического спектра и высокий уровень тревожности. Только что проведенное исследование этой группы ученых частоты встречаемости этого синдрома показало наличие его у каждого 250-го в общей популяции новорожденных, взятых безвыборочно.
ЭЭГ детей с синдромом умственной отсталости, сцепленной с ломкой хромосомой Х имеет специфические особенности, которые выделяют его из общей группы детей с аутизмом и умственной отсталостью.
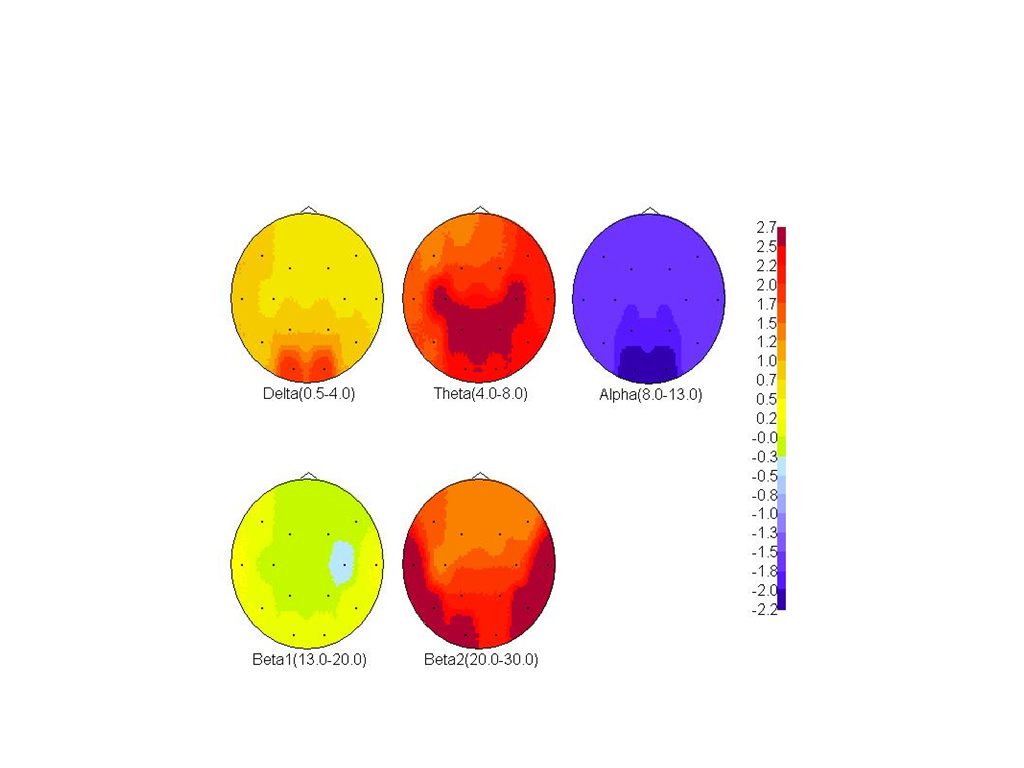
У подавляющего большинства больных с синдромом FXS регистрируется определенный паттерн в виде доминирования высокоамплитудного (до 150 мкВ) тета-ритма с частотой 5-8 Гц в теменно-центральных и лобно-центральных зонах коры. Этот ритм сохраняется при зрительном внимании и депрессируется при моторных пробах. На этом основании этот ритм можно расценить как медленный сенсомоторный ритм (МСР), исходя из его локализации и функциональной реактивности. Альфа-ритм у больных с этим синдромом , как правило, не регистрируется, альфа-активность представлена отдельными колебаниями, ее индекс не превышает 10-15%. Отмечается повышенный уровень бета-активности, преимущественно бета- 2 диапазона частот. Сравнение с возрастной нормой показывает достоверное увеличение тета-активности в теменно-центральных зонах коры, бета-2 активности и дефицит альфа-ритма (Рис. 9 ).
Рис. 9. Карты значений относительной мощности в стандартных диапазонах частот при сравнении с помощью Z-статистики ЭЭГ- записей группы пациентов с FXS в состоянии спокойного бодрствования с закрытыми глазами с возрастной нормой. Цветная шкала показывает величину стандартного отклонения (синий цвет – ниже нормы, красный- выше нормы, цифры показывают величину стандартного отклонения.).
После наступления периода полового созревания происходят существенные изменения в характере ЭЭГ- к 20 годам высокамплитудный тета-ритм, как правило, элиминируется и тип ЭЭГ из гиперсинхронного превращается в низкоамплитудный с отсутствием альфа ритма.
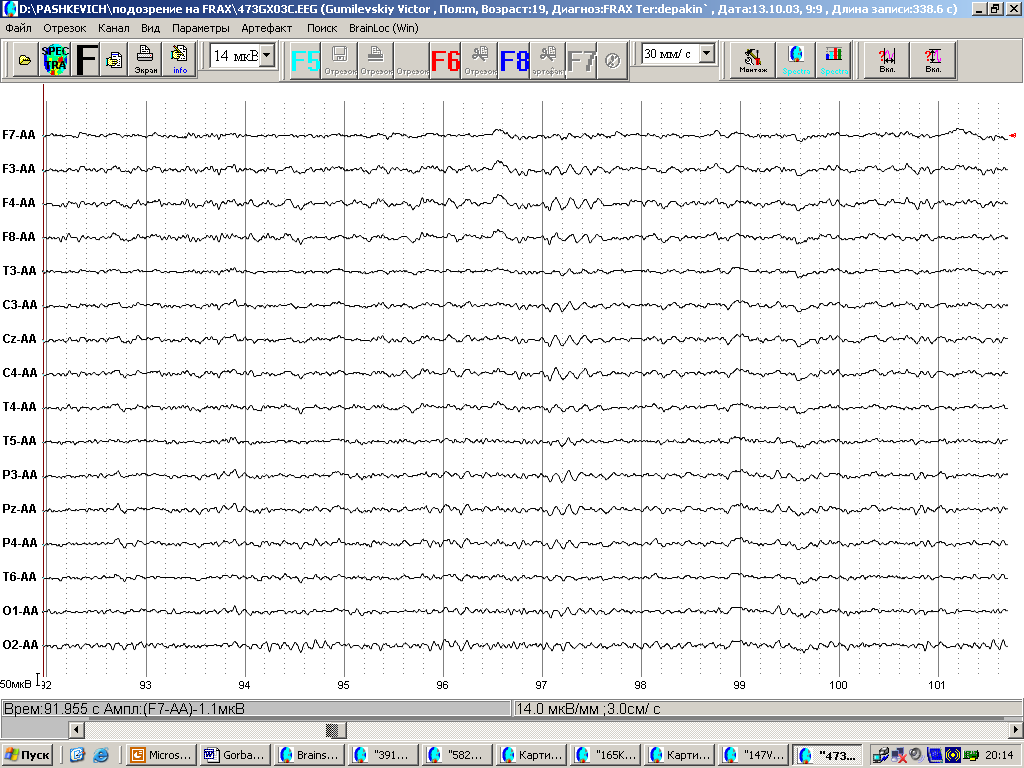
Рис. 10. ЭЭГ пациента с синдромом FXS в возрасте 19 лет. Низкоамплитудная ЭЭГ с отдельными вспышками ритмической тета-активности в лобно-центральных зонах коры
У больных с премутацией наличие тета-активности было характерно, в основном, для дошкольного возраста. У женщин- носительниц мутации наблюдалась отчетливая корреляция выраженности тета ритма с уровнем когнитивных нарушений. При нормальном IQ регистрировался организованный тип ЭЭГ, при умеренно выраженной УО наряду с альфа-ритмом регистрировалась тета-активность, при IQ ниже 70 в ЭЭГ доминировал тета-ритм на фоне значительной редукции альфа-активности. Т.о..выявление у индивида характерного для синдрома FXS фенотипа в сочетании с упомянутой ЭЭГ-активностью, является достаточным поводом для назначения цитогенетического исследования. Наличие подобного паттерна при СДВГ и мягкой деменции не позволяет исключить у этих пациентов синдром FXА/Т, что требует проведения генетических исследований. В связи с широким распространением нарушения функционирования гена FMR1 необходимо пересмотреть диагностическую тактику, широко использовать ЭЭГ для диагностики, наладить тестирование и провести скрининг.
