
- •1.Боевые свойства ов. Средства применения ob. Маркировка химических боеприпасов вероятного противника.
- •Боевые свойства
- •1.2 Токсичность
- •Классификация отравляющих веществ
- •2. Физические, химические и токсические свойства фов
- •2.1 Вещество gb - Зарин
- •2.2 Вещество gd - Зоман
- •2.3 Вещество VX
- •2.4 Другие вещества нервно - паралитического действия
- •Диизопропилфторфосфат
- •Алкилфторфосфонаты
- •2.5 Защита и дегазация фов. Защита от gb (зарин)
- •Защита от gd (зоман)
- •Защита от VX
- •3. Физические, химические и токсические свойства ов кожно-нарывного действия. Общая характеристика
- •3.1 Вещество hd – иприт
- •3.2 Другие вещества кожно-нарывного действия.
- •Вещество l – Люизит
- •Вещества hn-1. Hn-2, hn-3 - Азотистые иприты.
- •3.3. Защита и дегазация ов кожно-нарывного действия. Защита от hd (иприт).
- •4. Физические, химические и токсические свойства ов общеядовитого действия и защита от них.
- •4.1 Вещество ас - синильная кислота
- •4.2 Вещество ск
- •4.3 Другие вещества общеядовитого действия
- •Мышьяковистый водород AsH3 Мол. Масса 77,95
- •Фосфористый водород рн3 Мол. Масса 34
- •Окись углерода
- •Защита от ас
- •5. Физические, химические и токсические свойства ов удушающего действия и защита от них.
- •5.1 Вещество cg - фосген.
- •5.2. Другие вещества удушающего действия
- •Дифосген
- •Фториды хлора и серы
- •5.3. Защита от cg.
- •6. Характеристика раздражающих веществ (иритантов).
- •6.1 Вещество cs
- •6.2. Вещество cr
- •6.3. Другие вещества раздражающего действия Вещество ps
- •Вещество cn
- •Вещество dm
- •Арсины раздражающего действия
- •Природные раздражающие вещества и их синтетические аналоги
- •7. Характеристика психотропных веществ (инкапаситантов).
- •7.1 Вещество bz
- •7.2 Вещество lsd
- •7.3 Другие инкапаситанты
- •8. Бинарные системы химического оружия
- •8.1. Общая характеристика
- •8.2. Требования к реакциям в бинарных боеприпасах
- •8.3. Компоненты снаряжения gb-2 и gd-2
- •8.4. Компоненты снаряжения VX-2
- •8.5. Оценка бинарных систем химического оружия
- •9. Токсины
- •9.1. Общая характеристика
- •9.2. Классификация токсинов
- •9.3. Особенности строения и свойств токсинов
- •9.4. Ботулинические токсины и вещество хr
- •9.5. Стафилококковые энтеротоксины и вещество pg
- •9.6. Оценка токсинов
Диизопропилфторфосфат
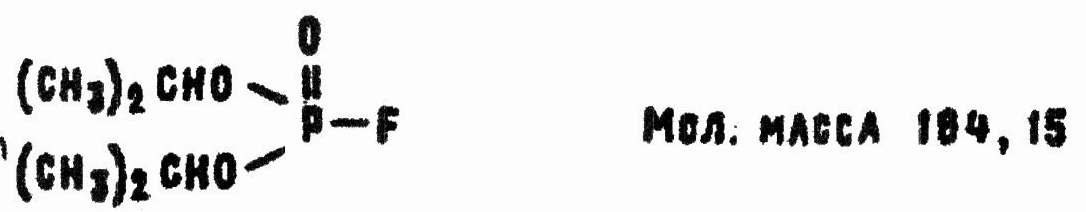
Химические названия: фторангидрид диизопропилового эфира фосфорной кислоты; диизопропиловый эфир фторфосфорной кислоты; диизопропилфторфосфат; диизопропоксифосфорилфторид.
Условные названия и шифры: ДФФ; DFP (Великобритания); PF-3 (США).
Диизопропилфторфосфат впервые получен в 1938 г. Г. Шрадером (Германия). Независимо от него в 1941 г. при изучении органических соединений фтора соединение получил Б. Сондерс (Великобритания). На конференции в Лондоне в декабре 1941 г. он сделал первое сообщение о токсических свойствах ДФФ, которое наметило перспективу использования его в военных целях. В настоящее время ДФФ потерял значение как самостоятельное ОВ, но нельзя исключать возможности применения его в тактических смесях. Известна, например, смесь с содержанием 87% ДФФ и 13% иприта, замерзающая при температуре минус 36 °С.
По характеру токсического действия ДФФ не отличается от вещества GB, уступая ему только в степени токсичности. Миоз наступает через 5 мин пребывания в атмосфере с концентрацией ДФФ 0,008 мг/л и продолжается до 7 сут, причем не ослабевает в течение первых 3 сут. Относительная токсичность ДФФ при ингаляции LCτ50 3 мг·мин/л. Средняя смертельная токсодоза при кожной резорбции LD50 200 мг/кг.
Диизопропилфторфосфат представляет собой бесцветную прозрачную жидкость со слабым фруктовым запахом, плотность жидкости при температуре 20 °С 1,0611 г/см3, относительная плотность пара по воздуху 6,4. ДФФ хорошо растворяется в органических растворителях, растворимость его в воде при температуре 20 °С — 1,5%. Температура кипения ДФФ 183 °С, давление насыщенного пара 0,57 мм рт. ст. при температуре 20 °С, максимальная концентрация Сmax20 5,6 мг/л. Соединение замерзает при температуре минус 82 °С.
Диизопропилфторфосфат — сравнительно стабильное, хорошо хранящееся соединение, химические свойства которого определяются наличием фторангидридной и эфирных функциональных групп. Поведение его в химических реакциях аналогично GB, различие состоит только в скоростях превращений. ДФФ медленно гидролизуется водой с разрывом связи фтор — фосфор:
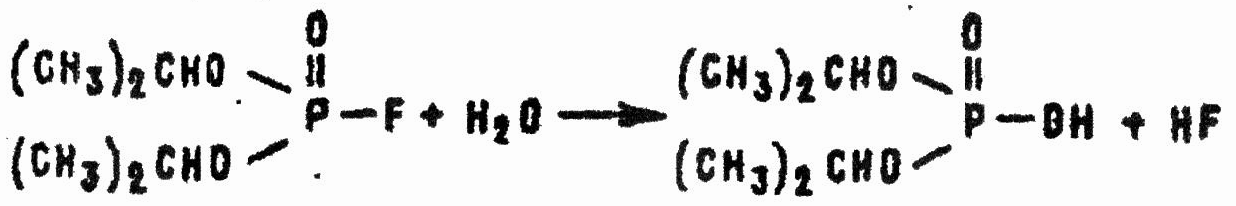
При температуре 15 °С гидролиз 1% раствора ДФФ в воде завершается за 3 сут. В избытке щелочи при температуре 17 °С и перемешивании ДФФ полностью гидролизуется за 30 мин (за это же время без перемешивания успевает прореагировать только 16% вещества), при температуре 25 °С — за 15 мин.
Амитон
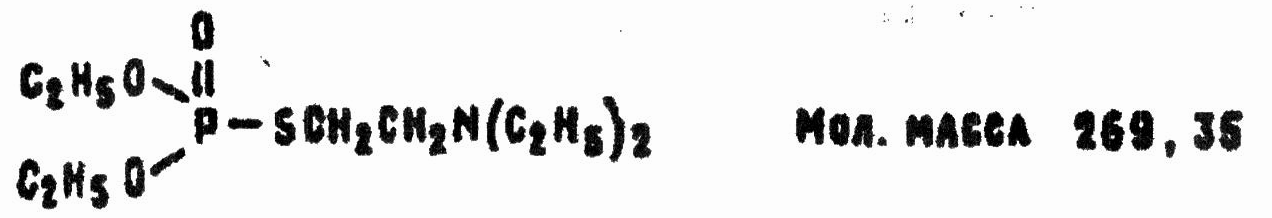
Химические названия: О,O-диэтиловый S-2-(N,N-диатиламино)-этиловый эфир тиолфосфорной кислоты; О, О-диэтил-S-(β-диэтиламиноэтил)-тиофосфат.
Условные названия и шифры: VG (США); амитон, тетрам, инферно, метрамак.
Амитон впервые описан в 1955 г. Р. Гошем и Дж. Ньюманом (Великобритания). По характеру и механизму физиологического действия аналогичен веществу VX, а по токсичности сравним с GB: среднесмертельные токсодозы LD50 при подкожном и внутрибрюшинном введении мышам для амитона равны соответственн 0.235 мг/кг и 0,5 мг/кг, а для GB — 0,2 мг/кг и 0,45 мг/кг.
Амитон является системным инсектицидом и акарицидом, однако из-за своей высокой токсичности для теплокровных животных находит ограниченное применение сельском хозяйстве. Он представляет собой бесцветную жидкость с расчетной температурой кипения около 300 °С. Хорошо растворяется в воде и смешивается органическими растворителями. Амитон медленно гидролизуется водой с разрывом связи фосфор — сера. Он образует твердые аммониевые соли с кислотами и некоторым галоидными алкилами, не уступающими по токсичности исходному основанию. Британская химическая компания «Империэл Кемикл Индастриз» (ICI) выпускает его виде кислого оксалата (соли со щавелевой кислотой), характеризующегося температурой плавления 100—101°С и токсодозой LD50 2 мг/кг (крысы, перорально). Для разложения амитона пригодны те же средства, что и для обезвреживания VX.
