
- •1.Боевые свойства ов. Средства применения ob. Маркировка химических боеприпасов вероятного противника.
- •Боевые свойства
- •1.2 Токсичность
- •Классификация отравляющих веществ
- •2. Физические, химические и токсические свойства фов
- •2.1 Вещество gb - Зарин
- •2.2 Вещество gd - Зоман
- •2.3 Вещество VX
- •2.4 Другие вещества нервно - паралитического действия
- •Диизопропилфторфосфат
- •Алкилфторфосфонаты
- •2.5 Защита и дегазация фов. Защита от gb (зарин)
- •Защита от gd (зоман)
- •Защита от VX
- •3. Физические, химические и токсические свойства ов кожно-нарывного действия. Общая характеристика
- •3.1 Вещество hd – иприт
- •3.2 Другие вещества кожно-нарывного действия.
- •Вещество l – Люизит
- •Вещества hn-1. Hn-2, hn-3 - Азотистые иприты.
- •3.3. Защита и дегазация ов кожно-нарывного действия. Защита от hd (иприт).
- •4. Физические, химические и токсические свойства ов общеядовитого действия и защита от них.
- •4.1 Вещество ас - синильная кислота
- •4.2 Вещество ск
- •4.3 Другие вещества общеядовитого действия
- •Мышьяковистый водород AsH3 Мол. Масса 77,95
- •Фосфористый водород рн3 Мол. Масса 34
- •Окись углерода
- •Защита от ас
- •5. Физические, химические и токсические свойства ов удушающего действия и защита от них.
- •5.1 Вещество cg - фосген.
- •5.2. Другие вещества удушающего действия
- •Дифосген
- •Фториды хлора и серы
- •5.3. Защита от cg.
- •6. Характеристика раздражающих веществ (иритантов).
- •6.1 Вещество cs
- •6.2. Вещество cr
- •6.3. Другие вещества раздражающего действия Вещество ps
- •Вещество cn
- •Вещество dm
- •Арсины раздражающего действия
- •Природные раздражающие вещества и их синтетические аналоги
- •7. Характеристика психотропных веществ (инкапаситантов).
- •7.1 Вещество bz
- •7.2 Вещество lsd
- •7.3 Другие инкапаситанты
- •8. Бинарные системы химического оружия
- •8.1. Общая характеристика
- •8.2. Требования к реакциям в бинарных боеприпасах
- •8.3. Компоненты снаряжения gb-2 и gd-2
- •8.4. Компоненты снаряжения VX-2
- •8.5. Оценка бинарных систем химического оружия
- •9. Токсины
- •9.1. Общая характеристика
- •9.2. Классификация токсинов
- •9.3. Особенности строения и свойств токсинов
- •9.4. Ботулинические токсины и вещество хr
- •9.5. Стафилококковые энтеротоксины и вещество pg
- •9.6. Оценка токсинов
2.2 Вещество gd - Зоман
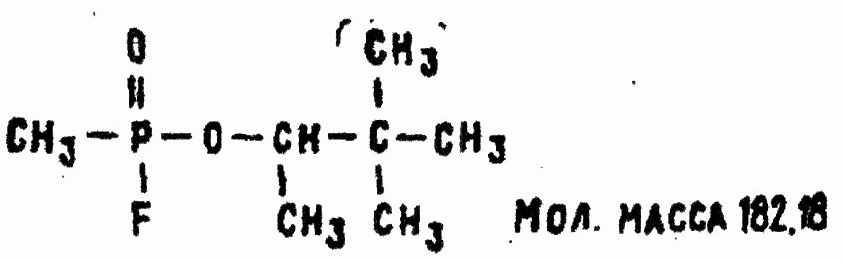
Химические названия: фторангидрид пинаколилового эфира метилфосфоновой кислоты; пинаколиловый эфир метилфторфосфоновой кислоты; фторангидрид 1,2,2-триметилпропилового эфира метилфосфоновой кислоты; пинаколилметилфторфосфонат; O-(втор-неогексил) метилфторфосфонат; O-(3,3 диметал-втор-бутил)-метилфторфосфонат.
Условные названия и шифры: зоман, GD (США), трилон (Германия).
Вещество GD впервые получено в конце 1944 г. Р. Куном в Германии. В Шпандау сразу же начал интенсивно осуществляться комплекс всесторонних исследований этого соединения, включающий разработку технологии его промышленного производства, средств и способов применения, токсикологические испытания. К моменту окончания второй мировой войны крупнотоннажное производство пинаколилметилфторфосфоната, получившего военный шифр «зоман», не бьло налажено, однако, по зарубежным данным, Германия имела около 20 т этого ОВ.
Первые публикации о зомане в открытой печати относятся к 1947 г. В США отравляющее вещество вызвало значительный интерес в связи с его высокой токсичностью, превосходящей токсичность зарина, и физико-химическими характеристиками, позволяющими применять его с помощью боеприпасов с неконтактными взрывателями.
Несмотря на то, что в армии США и других стран НАТО в настоящее время нет химических боеприпасов в снаряжении пинаколиловым эфиром метилфторфосфоновой кислоты, он рассматривается в качестве быстродействующего боевого ОВ смертельного действия, предназначенного для уничтожения живой силы противника путем заражения атмосферы паром и тонкодисперсным аэрозолем, а также для сковывания ее действий вследствие заражения местности и расположенных на ней объектов капельно-жидким веществом.
Предусмотрена кодировка боеприпасов с пинаколил-мстилфторфосфонатом тремя зелеными кольцами и маркировка надписью «GD GAS».
Токсические свойства
По характеру физиологического действия вещество GD аналогично GB, однако более токсично. Граница безопасных концентраций ОВ в воздухе находится ниже 5·10-7 мг/л, отравления слабой степени возникают уже при пребывании в зараженной атмосфере с концентрацией 2·10-5 мг/л в течение 15 мин. Величина Cτ, при которой наступает миоз, сопровождающийся затруднением дыхания, слюнотечением и потливостью, составляет 5·10-4 мг·мин/л. В тех случаях, когда экспозиция превышает 2 мин, эти признаки поражения могут сохраняться в течение нескольких суток.
Относительная токсичность GD при ингаляции LCτ50 0,03 мг·мин/л. Значения LCτ50 при поступлении парообразного ОВ через кожу находятся в пределах 7,5 - 10 мг·мин/л. Кожно-резорбтивная токсодоза LD50 1,4 мг/кг.
Кумулятивные свойства GD выражены сильнее, чем при отравлениях веществом GB.
Физические свойства
Пинаколилметилфторфосфонат в чистом виде представляет собой бесцветную прозрачную жидкость с плотностью 1,0131 г/см3. Технический продукт может иметь окраску от соломенно-желтой до коричневой и обладать камфарным запахом. Плотность пара по воздуху 6,33. GD ограниченно растворяется в воде: около 1% при температуре 0 °С и не более 1,5% при температуре 20 °С. Тем не менее вода опасно заражается и оказывается непригодной к употреблению. В органических растворителях вещество легко растворимо.
Пинаколиловый эфир метилфторфосфоновой кислоты не перегоняется при атмосферном давлении, вычисленная температура его кипения около 190 °С. Давление насыщенного пара около 0,3 мм рт. ст. при температуре 20 °С. Максимальная концентрация Сmax20 3 мг/л, что позволяет ожидать создания в атмосфере такой концентрации пара GD, которая способна вызвать смертельные поражения при пребывании в зараженной атмосфере в течение 1 мин.
Вещество GD способно к переохлаждению, при температуре минус 80 °С оно превращается в твердую стекловидную массу. Низкая температура затвердевания позволяет применять GD в любое время года.
Пористые материалы впитывают GD больше, чем GB. Это обусловливает необходимость предварительной десорбции ОВ с одежды и пористых поверхностей перед входом в герметичные убежища, транспортные средства и технику.
Химические свойства
Фторангидрид пинаколилового эфира метилфосфоновой кислоты по структуре аналогичен изопропилметилфторфосфонату, поэтому реакции, в которые вступает GB, свойственны и веществу GD. Различие между ними состоит лишь в том, что у GD более разветвленная и объемистая эфирная группа. Она и накладывает свой отпечаток в основном на скорость реакций.
Положительный индукционный эффект пинаколиловой группы выше соответствующего эффекта у изопропильной группы вещества GB. В одном направлении с ним действует и эффект сопряжения р-электронов эфирного кислорода с π-связью фосфора с фосфонильным кислородом. Это приводит к «выравниванию» связей между атомом фосфора и обоими кислородными атомами и, как следствие, — к некоторой компенсации дефицита электронной плотности на фосфоре и более слабой выраженности электрофильного характера данного реакционного центра у вещества GD по сравнению с веществом GB.
Пинаколиловая группа создает, кроме того, пространственные затруднения для подхода нуклеофильных реагентов к атому фосфора. Таким образом, в целом веществе GD взаимодействует с нуклеофильными реагентами заметно медленнее, чем GB, не более склонно по сравнению с ним к реакциям с электрофильными реагентами.
Гидролиз GD происходит по одинаковой с GB схеме с образованием нетоксичного пинаколилового эфира метилфосфоновой кислоты или соответствующих солей этой кислоты:
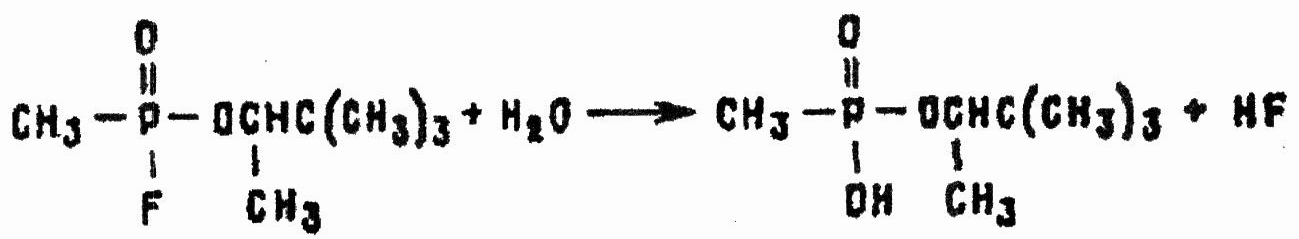
Скорость реакции зависит от концентрации водородных ионов. В водных растворах пинаколилметилфторфосфонат наиболее стабилен в слабокислой среде ее значениями рН = 4-6. В этих условиях при температуре 30 °С он успевает прогидролизоваться наполовину более чем за 10 сут. Для полного разложения GD в воде при температуре 18 °С и концентрации около 100 мг/л требуется 2,5 мес.
Влияние рН водных растворов GD на скорость его гидролиза при одинаковой концентрации можно проиллюстрировать следующими примерами. В нейтральной среде (рН = 7) GD гидролизуется на 50% за 82,5 ч при температуре 20 °С и за 41 ч при З0 °С. При рН = 2 и температуре 30 °С это время снижается до 6,5 ч. Особенно сильно возрастает скорость разложения ОВ в щелочной среде: если при температуре 20 °С и рН = 7,8 гидролиз GD наполовину продолжается около 1 сут, то при рН = 10 — всего 12 мин. Поэтому для дегазации GD можно рекомендовать щелочные растворы с достаточно высокой концентрацией гидроксильных ионов (рН не ниже 10). Концентрированные водные растворы щелочей и аммиака отщепляют не только атом фтора, но и эфирную группу:
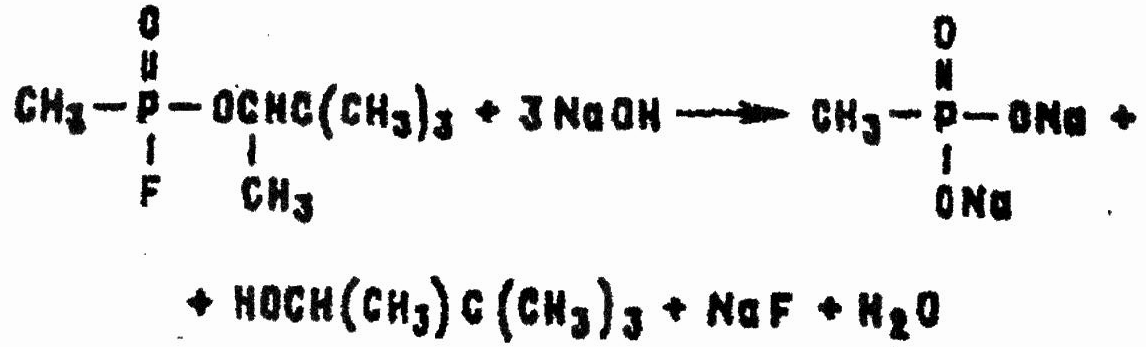
Взаимодействие GD с аммиаком и аминами, с гипохлоритами, с оксимами и гидроксамовыми кислотами в водных растворах также происходит медленнее, чем GB.
Это, как и невысокую растворимость ОВ в воде, необходимо принимать во внимание при выборе дегазирующих веществ, особенно при низких температурах.
В спиртовых растворах щелочей, а еще лучше алкоголятов и фенолятов щелочных металлов GD легко превращается в нетоксичные средние эфиры метилфосфоновой кислоты, например:
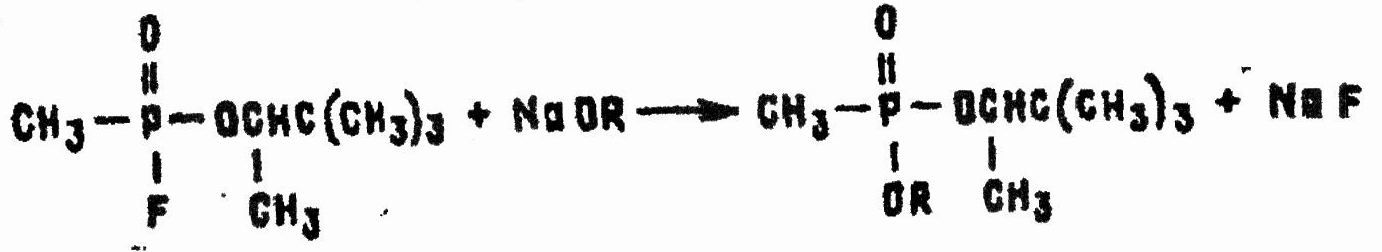
Эти реакции можно использовать для уничтожения GD на кожных покровах и поверхностях мелких предметов.
Пинаколилметилфторфосфонат хорошо хранится, хотя при длительном содержании в металлических емкостях требует внесения стабилизирующих добавок. Термическая устойчивость его сравнима с GB: заметный пиролиз наступает при нагревании выше температуры 150 °С. Продуктами пиролиза являются монофторангидрид метилфосфоновой кислоты, олигомерный метилфосфоновый ангидрид и непредельные углеводороды. Кратковременное термическое воздействие при взрыве боеприпасов соединение переносит без существенного разложения.
