
- •1.Боевые свойства ов. Средства применения ob. Маркировка химических боеприпасов вероятного противника.
- •Боевые свойства
- •1.2 Токсичность
- •Классификация отравляющих веществ
- •2. Физические, химические и токсические свойства фов
- •2.1 Вещество gb - Зарин
- •2.2 Вещество gd - Зоман
- •2.3 Вещество VX
- •2.4 Другие вещества нервно - паралитического действия
- •Диизопропилфторфосфат
- •Алкилфторфосфонаты
- •2.5 Защита и дегазация фов. Защита от gb (зарин)
- •Защита от gd (зоман)
- •Защита от VX
- •3. Физические, химические и токсические свойства ов кожно-нарывного действия. Общая характеристика
- •3.1 Вещество hd – иприт
- •3.2 Другие вещества кожно-нарывного действия.
- •Вещество l – Люизит
- •Вещества hn-1. Hn-2, hn-3 - Азотистые иприты.
- •3.3. Защита и дегазация ов кожно-нарывного действия. Защита от hd (иприт).
- •4. Физические, химические и токсические свойства ов общеядовитого действия и защита от них.
- •4.1 Вещество ас - синильная кислота
- •4.2 Вещество ск
- •4.3 Другие вещества общеядовитого действия
- •Мышьяковистый водород AsH3 Мол. Масса 77,95
- •Фосфористый водород рн3 Мол. Масса 34
- •Окись углерода
- •Защита от ас
- •5. Физические, химические и токсические свойства ов удушающего действия и защита от них.
- •5.1 Вещество cg - фосген.
- •5.2. Другие вещества удушающего действия
- •Дифосген
- •Фториды хлора и серы
- •5.3. Защита от cg.
- •6. Характеристика раздражающих веществ (иритантов).
- •6.1 Вещество cs
- •6.2. Вещество cr
- •6.3. Другие вещества раздражающего действия Вещество ps
- •Вещество cn
- •Вещество dm
- •Арсины раздражающего действия
- •Природные раздражающие вещества и их синтетические аналоги
- •7. Характеристика психотропных веществ (инкапаситантов).
- •7.1 Вещество bz
- •7.2 Вещество lsd
- •7.3 Другие инкапаситанты
- •8. Бинарные системы химического оружия
- •8.1. Общая характеристика
- •8.2. Требования к реакциям в бинарных боеприпасах
- •8.3. Компоненты снаряжения gb-2 и gd-2
- •8.4. Компоненты снаряжения VX-2
- •8.5. Оценка бинарных систем химического оружия
- •9. Токсины
- •9.1. Общая характеристика
- •9.2. Классификация токсинов
- •9.3. Особенности строения и свойств токсинов
- •9.4. Ботулинические токсины и вещество хr
- •9.5. Стафилококковые энтеротоксины и вещество pg
- •9.6. Оценка токсинов
8.3. Компоненты снаряжения gb-2 и gd-2
Одним из компонентов снаряжения GB-2 является дифторангидрид метилфосфоновой кислоты (DF), другим — смесь изопропилового спирта (IP) с акцептором фтористого водорода (KZ), представляющим собой амин или одну из кислот Льюиса, например растворимый в спиртах галогенид бора. Образование GB в бинарных боеприпасах описывается уравнением:
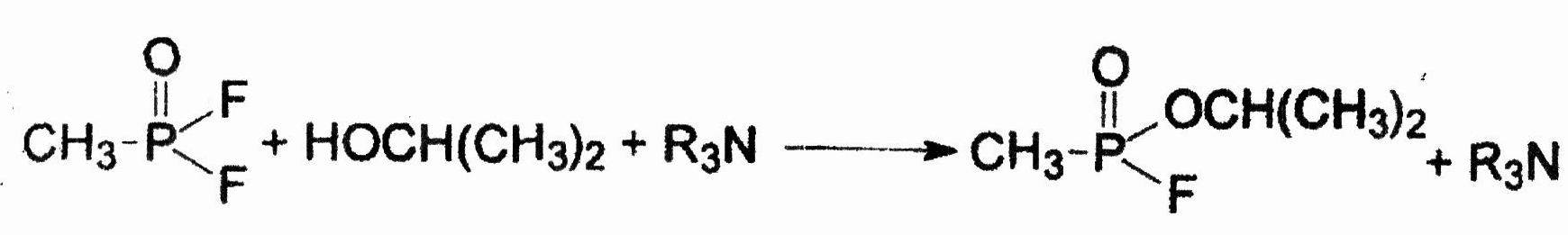
Дифторангидрид метилфосфоновой кислоты находит ограниченное применение в промышленности, главным образом в производстве некоторых пестицидов. Это бесцветная, прозрачная жидкость, не имеющая запаха, с плотностью при температуре 20 °С 1,367 г/см3. Соединение смешивается с инертными органическими растворителями, температура кипения 99 °С, максимальная концентрация пара при температуре 20 °С 153,6 мг/л. Температура начала кристаллизации минус 37 °С. Дифторангидрид метилфосфоновой кислоты относительно токсичен для теплокровных животных: LCτ50 5мг·мин/л (собаки), LD50 20 мг/кг (мыши, полкожно).
Дифторангидрид метилфосфоновой кислоты вступает во все реакции нуклеофильного замещения, присущие галоидангидридам кислот: гидролизуется водой, водными растворами щелочей, реагирует со спиртами, аммиаком и аминами. Вода авнительно легко замещает только один атом фтора с образованием метил-орфосфоновой кислоты:
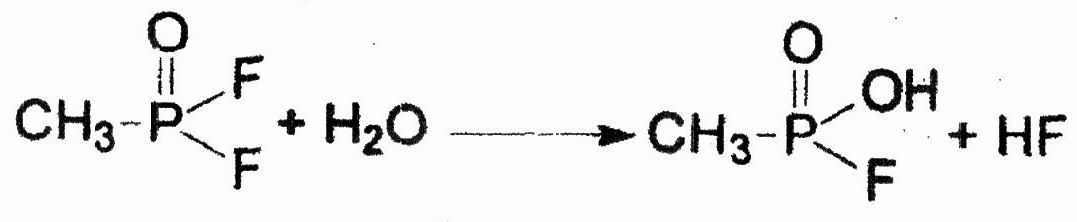
Для замещения второго атома фтора требуется кипячение разбавленных растворов DF со щелочью. Аналогично происходит реакция DF со спиртами:
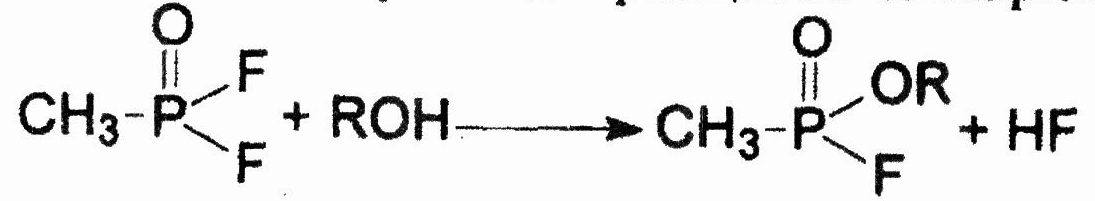
Реакция ускоряется в присутствии фтористого водорода, ее катализируют е вещества кислого характера.
Наиболее распространенным способом получения ОР является замещение хлора на фтор в дихлорангидриде метилфосфоновой кислоты:
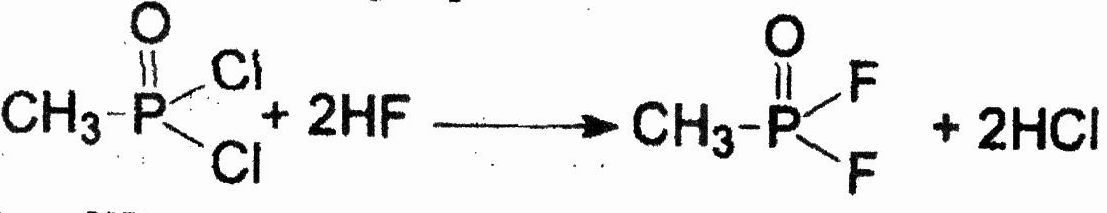
При пропускании HF через дихлорангидрид при температуре 70 - 100 °С выход DF близок к количественному.
Изопропиловый спирт применяется в промышленности в качестве межуточного продукта синтеза ацетона дегидрированием или неполным ислением.
Изопропиловый спирт — бесцветная, прозрачная жидкость со специфическим, характерным запахом, плотность 0,7851 г/смЗ при температуре 20 °С. Он в любых соотношениях смешивается с водой и органическими растворителями, образуя с водой азеотропную смесь (12,6% воды) с температурой кипения 80,3 °С. Температура кипения изопропанола 82,4 °С, температура плавления минус 89,5 °С. Изопропанол обладает слабым раздражающим действием на слизистые оболочки глаз и верхних дыхательных путей: LD50 5740 мг/кг (крысы, перорально). Смертельное отравление человека, сопровождающееся отеком легких, наступает при приеме внутрь не менее 0,4 л спирта.
Изопропиловый спирт обладает всеми свойствами алифатических спиртов: образует простые и сложные эфиры, вступает в реакции замещения гидроксильной группы на галоид, взаимодействует с реактивами Гриньяра. Он конденсируется с ароматическими соединениями в присутствии серной кислоты с образованием соответствующих изопропилпроизводных (изопропил-бензола, изопропилтолуола и т. п.).
Промышленные синтезы изопропанола основаны на гидратации пропилена. Известны два варианта этого процесса — так называемые сернокислотная и прямая гидратации пропилена.
При сернокислотной гидратации пропилен реагирует при температуре 25—50 °С и давлении 0,5—1 Па с 80—90% серной кислотой, при этом образуются изопропил- и диизопропилсульфаты:
CH3CH=CH2 + H2SO4 (CH3)2CHOSO2OH
2CH3CH=CH2 + H2SO4 (CH3)2CHOSO2OCH(CH3)2
Последние гидролизуют путем нагревания с водой.
Прямую гидратацию пропилена осуществляют в присутствии жидких или твердых катализаторов.
В присутствии жидкого катализатора (разбавленной серной кислоты) пропилен нагревают при температуре 200 °С и давлении 1,5 Па. В случае использования твердого катализатора парообразный пропилен пропускают над поверхностью контакта, представляющего собой смесь окиси вольфрама с активатором и окисью цинка, нанесенную на силикагель.
В качестве исходного сырья применяют либо пропилен-пропановую фракцию газов крекинга, либо пропиленовую фракцию газов после пиролиза нефти. Приведенными способами получают изопропанол с содержанием от 12 до 20% воды. Обезвоживание осуществляют методом азеотропной сушки в системе бензол — изопропанол — вода.
В случае синтеза в бинарных боеприпасах вещества GD вместо изопропанола в контейнер с веществом KZ помещают пинаколиновый спирт:
(СН3)3СН(СН3)ОН
В промышленности он находит применение в качестве промежуточного продукта синтеза средств борьбы с грызунами — вредителями сельскохозяйственных культур, некоторых парфюмерных и фармацевтических веществ.
Пинаколиновый спирт представляет собой бесцветную, прозрачную жидкость со слабым камфарным запахом, плотность 0,8187 при температуре 20 °С. Растворимость спирта в воде около 0,2% при температуре 20 °С, в органических растворителях — хорошая. С водой образует азеотропную смесь (31,4% воды), кипящую при температуре 90,7 °С. Температура кипения пинаколинового спирта 121 °С, максимальная концентрация пара 47 мг/л при температуре 20 °С, температура плавления 4 — 5,5 °С. Физиологическая активность и химические свойства мало отличаются от активности и свойств изопропанола.
