
- •1.Боевые свойства ов. Средства применения ob. Маркировка химических боеприпасов вероятного противника.
- •Боевые свойства
- •1.2 Токсичность
- •Классификация отравляющих веществ
- •2. Физические, химические и токсические свойства фов
- •2.1 Вещество gb - Зарин
- •2.2 Вещество gd - Зоман
- •2.3 Вещество VX
- •2.4 Другие вещества нервно - паралитического действия
- •Диизопропилфторфосфат
- •Алкилфторфосфонаты
- •2.5 Защита и дегазация фов. Защита от gb (зарин)
- •Защита от gd (зоман)
- •Защита от VX
- •3. Физические, химические и токсические свойства ов кожно-нарывного действия. Общая характеристика
- •3.1 Вещество hd – иприт
- •3.2 Другие вещества кожно-нарывного действия.
- •Вещество l – Люизит
- •Вещества hn-1. Hn-2, hn-3 - Азотистые иприты.
- •3.3. Защита и дегазация ов кожно-нарывного действия. Защита от hd (иприт).
- •4. Физические, химические и токсические свойства ов общеядовитого действия и защита от них.
- •4.1 Вещество ас - синильная кислота
- •4.2 Вещество ск
- •4.3 Другие вещества общеядовитого действия
- •Мышьяковистый водород AsH3 Мол. Масса 77,95
- •Фосфористый водород рн3 Мол. Масса 34
- •Окись углерода
- •Защита от ас
- •5. Физические, химические и токсические свойства ов удушающего действия и защита от них.
- •5.1 Вещество cg - фосген.
- •5.2. Другие вещества удушающего действия
- •Дифосген
- •Фториды хлора и серы
- •5.3. Защита от cg.
- •6. Характеристика раздражающих веществ (иритантов).
- •6.1 Вещество cs
- •6.2. Вещество cr
- •6.3. Другие вещества раздражающего действия Вещество ps
- •Вещество cn
- •Вещество dm
- •Арсины раздражающего действия
- •Природные раздражающие вещества и их синтетические аналоги
- •7. Характеристика психотропных веществ (инкапаситантов).
- •7.1 Вещество bz
- •7.2 Вещество lsd
- •7.3 Другие инкапаситанты
- •8. Бинарные системы химического оружия
- •8.1. Общая характеристика
- •8.2. Требования к реакциям в бинарных боеприпасах
- •8.3. Компоненты снаряжения gb-2 и gd-2
- •8.4. Компоненты снаряжения VX-2
- •8.5. Оценка бинарных систем химического оружия
- •9. Токсины
- •9.1. Общая характеристика
- •9.2. Классификация токсинов
- •9.3. Особенности строения и свойств токсинов
- •9.4. Ботулинические токсины и вещество хr
- •9.5. Стафилококковые энтеротоксины и вещество pg
- •9.6. Оценка токсинов
4.2 Вещество ск
Химические названия: хлорангидрид циановой кислоты; хлорциан; хлористый циан, шифр в армии США—СК.
Хлорциан является важным продуктом промышленного органического синтеза. Его тример, хлористый цианур, используется как исходное вещество для получения гербицидов и красителей триазинового ряда.
В период первой мировой войны хлорциан применялся французскими войсками в виде смеси с треххлористым мышьяком под названием «витрит». В годы второй мировой войны в США СК рассматривали как вещество, способное преодолеть шихту фильтрующего противогаза.
В настоящее время он не состоит на вооружении иностранных армий, однако, учитывая наличие производственных мощностей, нельзя исключать возможность его применения как самостоятельно, так и в смеси с АС.
Хлорциан — быстродействующее ОВ, обладающее общеядовитым действием и вызывающее раздражение слизистых оболочек глаз и верхних дыхательных путей. В организме он генерирует циан-ионы, поэтому признаки общего отравления хлорцианом такие же, как и синильной кислотой. Являясь галоидангидридом циановой кислоты, хлорциан ацилирует, кроме того, нуклеофильные функциональные группы рецепторов чувствительных окончаний слизистых оболочек, вызывая их раздражение.
Раздражающее действие пара СК на глаза и органы дыхания проявляется без периода скрытого действия. Начальная раздражающая концентрация 0,002 мг/л, непереносимая, вызывающая обильное слезотечение и спазм век — 0,06 мг/л. Концентрация 0,4 мг/л при экспозиции 10 мин может вызвать смертельный исход. Относительная токсичность при ингаляции LCτ50 11 мг·мин/л, при этом смерть наступает в течение 1—15 мин. Кумулятивными свойствами СК не обладает.
Хлорциан — бесцветный газ с плотностью по воздуху 2,1. Плотность жидкого вещества при температуре 4 °С 1,218 г/см3; ограниченно растворим в воде (7% при температуре 20 °С) и хорошо — в органических растворителях, в том числе в таких отравляющих веществах, как иприт, синильная кислота, хлорпикрин; температура кипения 12,6 °С, давление насыщенного пара 1002 мм рт. ст., Сmax20 3300 мг/л; температура замерзания минус 6,5 °С; хорошо сорбируется пористыми материалами.
Как хлорангидрид циановой кислоты, хлорциан способен к реакциям нуклеофильного замещения атома хлора на различные группировки. Кроме того, он обладает окислительными свойствами и способностью к некоторым специфическим реакциям.
Влагой воздуха СК не гидролизуется. Вода медленно разлагает его на соляную и неустойчивую циановую кислоты:
![]()
В избытке воды циановая кислота разлагается на двуокись углерода и аммиак, который образует с соляной кислотой хлористый аммоний:
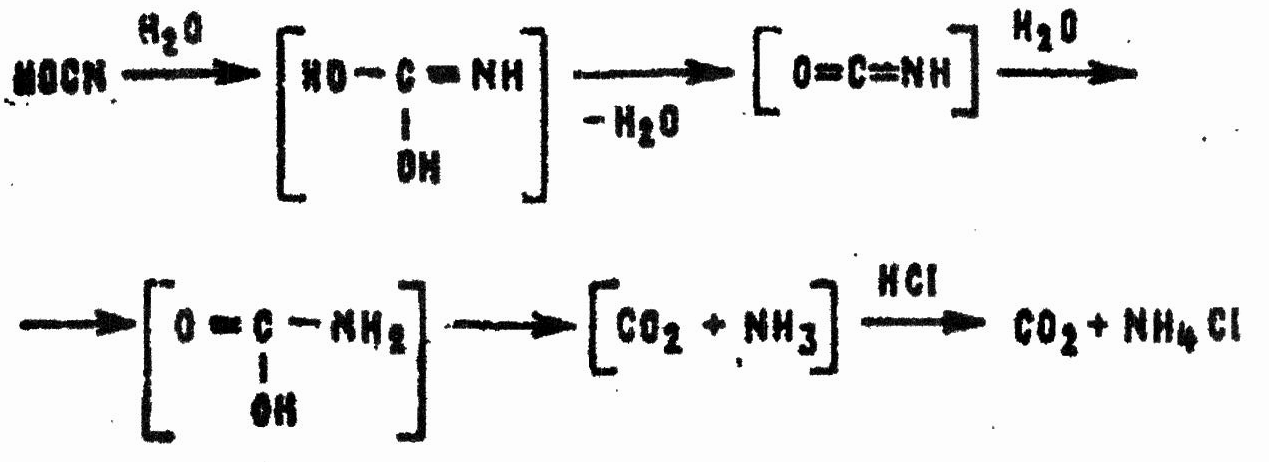
При кипячении в воде гидролиз СК происходит очень быстро. Концентрированные кислоты ускоряют процесс. Еще больше ускоряется гидролиз разбавленными щелочами, а концентрированные щелочи уже при комнатной температуре быстро превращают СК в нетоксичные соли:
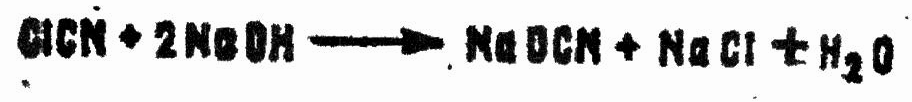
Эта реакция может использоваться для дегазации и анализа СК.
С аммиаком СК образует нетоксичный цианамид:

Реакция происходит даже в парах и пригодна для уничтожения хлорциана в помещениях. По аналогичной схеме реагируют первичные и вторичные амины. Защита от СК аналогична защите от АС.
