
- •NaCl Natrii chloridum.
- •KCl Kalii chloridum
- •NaBr Natrii bromidum.
- •KBr Kalii bromidum
- •NaI Natrii iodidum
- •Ki Kalii iodidum
- •Natrii thiosulfas.
- •Natrii hydrocarbonas.
- •Natrii tеtraborаs seu Borax (бура)
- •Protorgolum seu Argentum proteinicum
- •Collargolum seu Argentum colloidale
- •Solutio Formaldehydi seu Formalinum
- •Hexamethylentetraminum seu Urotropinum seu Methenaminum
- •Глюкоза
- •Димедрол
- •Calcii gluconas
- •2. Метод нейтрализации.
- •Natrii citras pro injectionibus
- •Acidum aminocapronicum
- •Аdrenalini hydrotatras
- •Ephedrini hydrochloridum
- •Резорцин – Resorcinum
- •Acidum benzoicum
- •Acidum salicylicum
- •Natrii benzoas
- •Салицилат натрия – Natrii salicylas
- •Acidum acetylsalicylicum (Aspirinum)
- •Стрептоцид – Streptocidum
- •Норсульфазол –Norsulfazolum seu Sulfathiazolum
- •Phthalazolum-фталазол
- •Anaesthesinum. Aethyliiaminobenzoas
- •Natrii para-aminosalicylas
- •Furacilinum
- •Antipyrinum
- •Analgini.
- •Dibazolum
Phthalazolum-фталазол
2-(пара-(орто-карбокси)-бензамидобензолсульфамид)тиазол
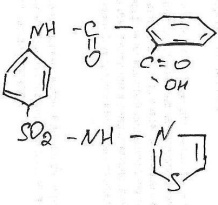
Подлинность.
Т.к. первичная NH2 группа у фталазола отсутствует реакция на амино группу не возможна.
1. кислотный гидролиз. доказательство норсульфазола (ГФ)
Преп. Кипятят с р-ром соляной к-ты , охлаждают и доб. нитрит натрия. Появляется вишнёво-красное окрашивание. Полученную смесь выливают в щелочной р-р ß-нафтола.
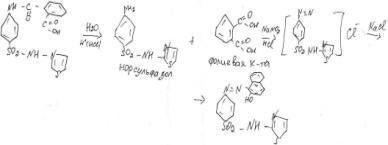
2. кислотный гидролиз и доказательство фталевой к-ты.
Преп. Помещают в фарфоровую чашку доб. несколько кристаллов резорцина и конц. серную кту. Нагревают. Полученный плав расплавляют в щелочи и выливают в большой объем воды. Наблюдается р-р бурого цвета с зеленой флюоресценцией.
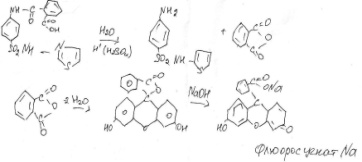
Количественное определение.
Метод кислотно-основного титрования в неводных средах.
Т.н.п. растворяют в диметилформамиде и титруют р-ром щелочи в метиловом спирте с доб. Бензола о,1 моль на литр до зеленой окраске. Индикатор тимоловый синий.
![]()
Anaesthesinum. Aethyliiaminobenzoas
Этиловый эфир ПАБК
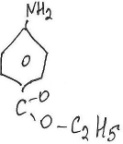
Подлиность.
1. На ароматическую аминогруппу
А) по ГФ получение азокрасителя
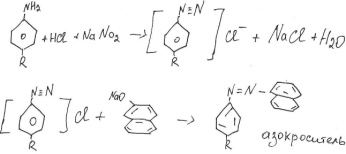
2. лигниновая проба
![]()
3. на аминогруппу на группу легкой окисляемости.
Преп. Взбалтывают с водой доб. соляную к-ту и белильную известь, р-р окрашивается в оранжевый цвет. Для сохранения окраски доб. эфир. Эфирный слой окр. в оранжевый цвет. Для сохранения окрашивания доб. эфир. Эфирный слой окр. В оранжевый цвет.
4. специфические реакции.
Щелочной гидролиз. Доказательство этилового спирта.
Преп. Взбалтывают с р-ром щелочи, нагревают. К охлажденному р-ру доб. йод до светло-желтой окраски, постепенно ощущается запах йодоформа, а затем обр. осадок черного цвета.
![]()
![]()
![]()
![]()
5. определение температуры плавления 89-91,5°.
Количественное определение.
1. По ГФ 10 метод нитритометрии.
Т.н.п. взбалтывают с водой, подкисляют соляной к-той, доб. катализатор кристаллический калий бром и титруют р-ром нитрита натрия медленно при низкой температуре до: а) нейтральный красный – синий. Б) трапеолин 000 + метиленовый синий 1:4 из фиолетового в голубой
![]()
2. внутриаптечные методы
А) метод нейтрализации в спирто-хлороформеной среде. [осн]*HCl+NaOH=[осн]+NaCl+H2O
0,1 м/л ф/ф CHCl3
Novocainum
Procaini hydrochloridum
ß-диэтиламиноэтилового эфира ПАБК гидрохлорид
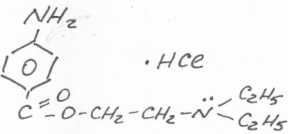
Подлиность.
1. На ароматическую аминогруппу
А) по ГФ получение азокрасителя
2. лигниновая проба
3. на аминогруппу на группу легкой окисляемости.
А) Преп. Взбалтывают с водой доб. соляную к-ту и белильную известь, р-р окрашивается в оранжевый цвет. Для сохранения окраски доб. эфир. Эфирный слой окр. в оранжевый цвет. Для сохранения окрашивания доб. эфир. Эфирный слой окр. В оранжевый цвет.
Б) Преп. растворяют в воде подкисляют серную к-ту доб перманганат калия. Эффект обесцвечивания перманганата калия.
4. специфические реакции.
А) Преп. Растворяют в воде доб. Р-р щелочи. На поверхости р-ра наблюдаются маслянистые пятна.
[нов]*HCl+NaOH=NaCl+[ нов]
Б) На Cl
HCl+AgNO3=AgCl↓+HNO3
AgCl↓+2NH4OH=[Ag(NH3) 2]Cl+2H2O
[Ag(NH3) 2]Cl+2HNO3=2NH4NO3+AgCl↓
Количественное определение.
1. По ГФ 10 метод нитритометрии.
Т.н.п. взбалтывают с водой, подкисляют соляной к-той, доб. катализатор кристаллический калий бром и титруют р-ром нитрита натрия медленно при низкой температуре до: а) нейтральный красный – синий. Б) трапеолин 000 + метиленовый синий 1:4 из фиолетового в голубой
2. Внутреаптечные метод
А) аргентометрия по мору
[осн]*HCl +AgNO3=AgCl↓+[осн]*HNO3
(◦)AgNO3 +K2CrO4=Ag2CrO4↓+2KNO3
желто-роз
Б) Аргентометрия по фаянсу. Индикатор бромфеноловый синий титруют в уксусной у-те до фиолетового осадка
[осн]*HCl +AgNO3=AgCl↓+[осн]*HNO3
В) меркурометрия; меркуриметрия
По индикатору ДФК до фиолетовой окраски р-ра
2[осн]*HCl+Hg2 (NO3) 2=2[осн]*HNO3+Hg2Cl2 монохлорид ртути
2[осн]*HCl+Hg(NO3) 2=2[осн]*HNO3+HgCl3
Dicainum
Tetracaini hydrochloridum
ß-диэтиламиноэтилового эфира парабутил амино бензойной к-ты гидрохлорид
![]()
Подлиность
1. При доб. к р-ру преп. р-ра нитрита натрия обр. осадок белого цвета. Нитрозо соединения после кислого гидролиза с хлористоводородной к-той.
![]()
2. специфические р-ции
А) получение аце-соли.
Преп. Помещают в выпарительную чашку доб. конц. азотную к-ту, нагревают, к полученому р-ру доб. Спиртовой р-р щелочи. Появляется вишнёвое окр ацесоль.
![]()
Б) дикаин растворяют в воде доб. Родонит аммония NH4CNS тиоционат образуется осадок белого цвета имеющий характерную темпиратуру плавления.
в) На Cl
д) определение температуры плавления 146-150
1. По ГФ 10 метод нитритометрии.
Т.н.п. взбалтывают с водой, подкисляют соляной к-той, доб. катализатор кристаллический калий бром и титруют р-ром нитрита натрия медленно при низкой температуре до: а) нейтральный красный – синий. Б) трапеолин 00 из красного в желтый
![]()
2. внутриаптечные методы
А) метод нейтрализации в спирто-хлороформеной среде. [осн]*HCl+NaOH=[осн]+NaCl+H2O
0,1 м/л ф/ф CHCl3
б) аргентометрия по мору
[осн]*HCl +AgNO3=AgCl↓+[осн]*HNO3
(◦)AgNO3 +K2CrO4=Ag2CrO4↓+2KNO3 желто-роз
в) Аргентометрия по фаянсу. Индикатор бромфеноловый синий титруют в уксусной у-те до фиолетового осадка
[осн]*HCl +AgNO3=AgCl↓+[осн]*HNO3
г) меркурометрия; меркуриметрия
По индикатору ДФК до фиолетовой окраски р-ра
2[осн]*HCl+Hg2 (NO3) 2=2[осн]*HNO3+Hg2Cl2 монохлорид ртути
2[осн]*HCl+Hg(NO3) 2=2[осн]*HNO3+HgCl3
