
- •Атомно-эмиссионный спектральный анализ.
- •Методы введения пробы в источник возбуждения
- •Аппаратура для спектрального анализа.
- •Оптические характеристики приборов.
- •Б) Фотографические методы:
- •Методы определения концентрации элементов в пробе.
- •Метод трех эталонов – основан на построении градуировочного графика в соответствии с уравнением (9):
- •Рентгеноспектральный анализ.
- •Возбуждение рентгеновского излучения.
- •Рентгеновская флуоресценция.
- •Дифракция рентгеновских лучей.
- •Аналитическое применение рентгеноспектрального флуоресцентного анализа.
- •Качественный рентгеноспектральный анализ.
- •Количественный рентгеноспектральный анализ.
Атомно-эмиссионный спектральный анализ.
Под атомно-эмиссионным спектральным анализом понимают методы определения химического состава вещества по его оптическому спектру, излучаемому возбужденными атомами этого вещества. Оптический эмиссионный спектр атома представляет собой ряд дискретных излучений, характеризующихся различной частотой и интенсивностью. Дискретные излучения связаны с переходом электронов возбужденного атома с более высоких энергетических уровней на устойчивые стационарные орбитали.
В нормальном (невозбужденном) атоме его электроны занимают все возможные состояния, начиная с 1s уровня и выше. Под влиянием внешних воздействий (нагрев, столкновение с быстро летящими частицами – электронами, ионами) при неупругом соударении происходит переход валентных электронов атома на другие, более удаленные от ядра атома орбитали. Энергия атома возрастает, атом возбуждается. Возбуждение длится около 10-8с, и электрон снова переходит с более удаленного уровня на прежний, или задерживается на промежуточных орбиталях. В процессе обратного перехода излучается энергия. Излучение это монохроматично, и его частота определяется из уравнения
![]() (1)
(1)
где Е1 – энергия электрона на ближнем уровне, эВ.
Е2 – энергия электрона на дальнем, возбужденном уровне, эВ
h = 6,625∙10-34 Дж/с –постоянная Планка.
Поскольку разности энергий Е2 – Е1, Е2 – Е0, Е1 – Е0, и т.д., не равны между собой, то и соответствующие частоты также будут различными. Появляется совокупность излучений, образующих спектр атома. В целом, число возможных энергетических переходов определяется строением электронных уровней атома каждого элемента, и, в первую очередь, числом и размещением внешних, валентных электронов. А интенсивность излучаемых спектральных линий определяется вероятностью осуществления отдельных переходов, Ai,n, числом атомов, в которых осуществляется данный переход, Ni, и температурой.
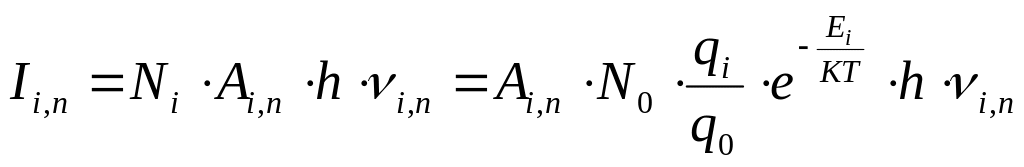 (2)
(2)
где N0 – число атомов в основном состоянии,
q i, q o- статистические веса возбужденного и основного состояний,
Ei –разность энергий между ними,
К-константа Больцмана,
Т- абсолютная температура.
Для эмиссии квантов света определенной частоты, т.е. для получения в спектре атома определенной спектральной линии, атоме необходимо сообщить определенную энергию, которую называют потенциалом возбуждения данной линии. Для каждого атома наиболее легко совершаются переходы его валентных электронов на первый разрешенный возбужденный уровень и обратно.
Линии спектра, соответствующие переходам на нормальный (основной) уровень носят название резонансных линий. Особое аналитическое значение имеют резонансные линии, соответствующие переходу с первого возбужденного уровня на основной. Обладая наиболее низким потенциалом возбуждения среди всех остальных линий спектра данного элемента, они будут наиболее яркими, так как здесь будет наибольшее число переходов электронов. Эти линии преимущественно используются для качественного обнаружения элементов. Потенциалы возбуждения резонансных линий элементов зависят от положения элемента в таблице Менделеева. Низкие потенциалы возбуждения (1,6-3,0) эВ, имеют щелочные металлы. У благородных газов высокие потенциалы возбуждения (12-20) эВ. Большинство металлов занимают промежуточное положение. Если атом получит энергию возбуждения большую, чем требуется переходу электронов на самый высокий энергетический уровень (самую дальнюю орбиталь), то электрон будет выброшен за пределы атома. Произойдет ионизация атома. Если у атома имеется несколько валентных электронов, то он может быть ионизирован дважды, трижды и т.д. Энергия, необходимая для отрыва электрона, называется потенциалом ионизации.
ИСТОЧНИКИ ВОЗБУЖДЕНИЯ СПЕКТРОВ.
1. Газовое пламя – ацетилено-воздушное, ацетилено-кислородное и пламя светильного газа с воздушным или кислородным дутьем или с закисью азота. Установка газового пламени позволяет легко обеспечить высокую стабильность горения пламени, но, ввиду невысокой температуры (1800- 3000 0С), применяется для определения элементов с низким потенциалом возбуждения.
2. Дуга постоянного тока – представляет собой стационарный газовый разряд, протекающий под действием напряжения порядка 200 В и силе тока (2 – 15) А. Температура дуги зависит от подводимой электрической мощности и природы газа в межэлектродном пространстве и достигает значений (4000-8000)0С. Этого достаточно для возбуждения спектров большинства элементов. Её большим недостатком является перемещение анодного и катодного пятен по поверхности электродов, что влечет за собой изменение сопротивления столба дуги и, как следствие, флуктуацию интенсивности во времени. Эффект блуждания дуги можно понизить применением электродов с малым диаметром – 3 мм. В этом случае анодное пятно покрывает весь торец электрода и излучение становиться более стабильным, но сохраняется опасность сильного обгорания электродов и изменения расстояния между электродами, приводящее к изменению температурного режима. Чтобы сгладить этот эффект, вводят балластное сопротивление (Rb). Согласно закону Ома, при Rb>>R, сила тока
![]()
будет сохраняться приблизительно постоянной и горение дуги стабилизируется.
3. Дуга переменного тока. Обычная дуга переменного тока при малой силе тока гореть не может. При переходе фазы переменного тока через нуль образуется пауза, во время которой электроды остывают, термоэлектронная эмиссия прерывается и дуга гаснет. Для периодического поджига дуги используют активатор – высокочастотный контур, генерирующий небольшие искры между электродами для ионизации газа. В этих условиях горение дуги становится стабильным. Дуга переменного тока обладает тем преимуществом, что питается непосредственно от сети переменного тока. Недостаток – менее полное испарение проб труднолетучих элементов.
4. Высоковольтная конденсированная искра – представляет собой нестационарный, кратковременный электрический разряд под действием высокого напряжения, подаваемого на электроды (15000-40000) В. Для пробоя промежутка между электродами в 2-3 мм, используют предварительное накопление заряда на конденсаторе.
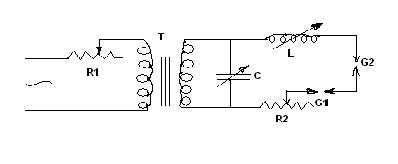
Рис.1.1. Электрическая схема высоковольтной конденсированной искры.
Температура в факеле искры 8000-100000С, а в канале плазмы 30000-400000С, поэтому искра применяется для анализа трудновозбудимых элементов и благодаря большой стабильности искрового разряда широко используется для количественного определения. Из-за кратковременности импульсов (10-4с), электроды в искре нагреваются и обгорают значительно слабее, чем в дуге. В процессе анализа теряется 1-5 мг вещества, в то время как при дуговом режиме 10-50 мг.
Для возбуждения оптических спектров применяют источники света и других типов: низковольтная искра, полый катод, оптические квантовые генераторы – лазеры. Большинство из них используется в локальном спектральном анализе.
