
- •Минобрнауки
- •Кафедра «Материаловедение и технология обработки материалов» Курсовая работа
- •Оглавление
- •Часть II. «Тройные системы»
- •Часть I. «Двойные системы»
- •Характеристика компонентов системы Al-Cu
- •Характеристика фаз двухкомпонентной системы Al-Cu
- •Нонвариантные равновесия системы Al-Cu
- •Анализ фазовых превращений и определение количества фаз и структурных составляющих в сплавах х1, (31%(ат)Al, ост. Cu) и х2, (47%(ат)Al, ост. Cu)
- •Описание кривой охлаждения сплава x1
- •Описание кривой охлаждения сплава x2
- •Расчет для сплава x1
- •Расчет для сплава x2
- •Часть II. «Анализ фазовых равновесий в тройной системе с четырехфазным эвтектическим равновесием»
- •Построение проекции диаграммы состояния на плоскость концентрационного треугольника.
- •Построение граничных двойных систем а-в, в-с, а-с.
- •Построение проекций поверхностей ликвидуса, солидуса и сольвуса системы на плоскость концентрационного треугольника. Нанесение изотерм на эти проекции.
- •Построение изотермического разреза при температуре 765оС.
- •Построение политермического разреза I-I.
- •Анализ фазовых превращений в сплавах.
- •Список литературы:
Расчет для сплава x1
Фазовый состав сплава: γ2.
Структурный состав сплава: γ2.
Расчет количества фаз:
Qγ2 = (37,5 - 31) / (37,5 - 31) = 1.
Расчет количества структурных составляющих:
Qγ2 = (37,5 - 31) / (37,5 - 31) = 1.
Расчет для сплава x2
Фазовый состав сплава: ξ2 + η2.
Структурный состав сплава: ξ2 + Э(ξ2 + η2).
Расчет количества фаз:
Q ξ2 = (47,7 – 47) / (47,7 – 44,8) = 0,24;
Q η2 = (47 – 44,8) / (47,7 – 44,8) = 0,76.
Расчет количества структурных составляющих:
Q ξ2 = (47,7 – 47) / (47,7 – 44,8) = 0,24;
Q Э(ξ2 + η2) = (47 – 44,8) / (47,7 – 44,8) = 0,76.
Рис2
Рис3
Часть II. «Анализ фазовых равновесий в тройной системе с четырехфазным эвтектическим равновесием»
Построение проекции диаграммы состояния на плоскость концентрационного треугольника.
Для построения проекции диаграммы состояния начертим равносторонний концентрационный треугольник со сторонами 200 мм. В вершинах треугольника откладываем чистые компоненты А, В и С, которые имеют температуры плавления: 13000С, 15000С и 12500С соответственно. Стороны АВ, ВС и АС являются проекциями соответствующих граничных двойных систем: А–В, В–С и А–С.
На стороне АВ от точки А до точки В откладываем количество компонента В от 0 до 100% в масштабе 20мм=10%В. На стороне ВС от точки В до точки С откладываем количество компонента С от 0 до 100% в масштабе 20мм=10%С. На стороне АС от точки С до точки А откладываем количество компонента А от 0 до 100% в масштабе 20мм=10%А.
На стороны АВ, ВС и АС, являющихся проекциями граничных двойных систем, нанесем точки, соответствующие химическому составу фаз, участвующих в нонвариантных равновесиях в двойных системах, и точки, соответствующие минимальной растворимости компонентов друг в друге при комнатной температуре. Для этого воспользуемся данными, имеющимися в приложении к заданию по курсовой работе (стр. 5).
Сторона АВ:
– точки
минимальной растворимости компонентов
друг в друге
 (24%В,
ост. А) и
(24%В,
ост. А) и
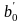 (75%В,
ост. А);
(75%В,
ост. А);
– точки
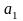 (32%В
ост. А),
(32%В
ост. А),
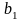 (65%В,
ост. А) и
(65%В,
ост. А) и
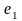 (55%В,
ост. А) соответствуют составу фаз,
участвующих в нонвариантном равновесии.
(55%В,
ост. А) соответствуют составу фаз,
участвующих в нонвариантном равновесии.
Сторона ВС:
– точки
минимальной растворимости компонентов
друг в друге
 (30%С,
ост. В) и
(30%С,
ост. В) и
 (85%С,
ост. В);
(85%С,
ост. В);
– точки
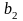 (40%С
ост. В),
(40%С
ост. В),
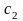 (60%С,
ост. В) и
(60%С,
ост. В) и
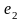 (50%С,
ост. В) соответствуют составу фаз,
участвующих в нонвариантном равновесии.
(50%С,
ост. В) соответствуют составу фаз,
участвующих в нонвариантном равновесии.
Сторона АС:
– точки
минимальной растворимости компонентов
друг в друге
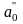 (80%А,
ост. С) и
(80%А,
ост. С) и
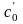 (15%А,
ост. С);
(15%А,
ост. С);
– точки
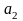 (70%А
ост. С),
(70%А
ост. С),
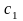 (35%А,
ост. С) и
(35%А,
ост. С) и
 (50%А,
ост. С) соответствуют составу фаз,
участвующих в нонвариантном равновесии.
(50%А,
ост. С) соответствуют составу фаз,
участвующих в нонвариантном равновесии.
В тройной системе А-В-С существуют 4 фазы:
L – трехкомпонентный жидкий раствор;
α – твердый раствор на основе компонента А;
β – твердый раствор на основе компонента В;
γ – твердый раствор на основе компонента С.
В системе А-В-С осуществляется четырехфазная эвтектическая реакция:
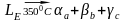 .
Согласно правилу фаз Гиббса эта реакция
является нонвариантной:
.
Согласно правилу фаз Гиббса эта реакция
является нонвариантной:
c = k – f + 1 = 3 – 4 + 1 = 0,
происходит при постоянной температуре 350оС и при постоянстве составов всех фаз. На плоскость концентрационного треугольника эвтектическая плоскость проецируется в виде Δabc.
На плоскость концентрационного треугольника наносим точки:
– отвечающие составам фаз, участвующих в четырехфазной эвтектической реакции: a (55%А, 25%В, 20%С); b (25%А, 45%В, 30%С); c (30%А, 20%В, 50%С), Е (35%А, 30%В, 35%С); треугольник abc чертим сплошной линией;
– отвечающие
составам фаз при комнатной температуре:
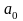 (70%А,
20%В, 10%С);
(70%А,
20%В, 10%С);
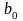 (20%А,
60%В, 20%С);
(20%А,
60%В, 20%С);
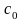 (10%А,
10%В, 80%С).
(10%А,
10%В, 80%С).
С четырехфазным равновесием связаны 4 трехфазные моновариантные равновесия (c = k – f + 1 = 3 – 3 + 1 = 1), осуществляющиеся в интервале температур и с изменением составов всех фаз:
три трехфазные эвтектические равновесия предшествуют четырехфазной реакции:
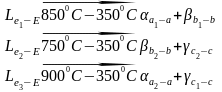
Проводим кривые, соответствующие изменению составов участвующих в этих равновесиях фаз:
– кривые
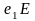 ,
,
 и
и
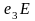 определяют состав жидкой фазы, насыщенной
по отношению к двум видам кристаллов;
выпуклость кривых в сторону более
легкоплавкого компонента.
определяют состав жидкой фазы, насыщенной
по отношению к двум видам кристаллов;
выпуклость кривых в сторону более
легкоплавкого компонента.
– кривые
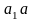 и
и
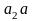 определяют состав α
фазы; выпуклость кривых в сторону
компонента А.
определяют состав α
фазы; выпуклость кривых в сторону
компонента А.
– кривые
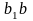 и
и
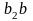 определяют состав β
фазы; выпуклость кривых в сторону
компонента В.
определяют состав β
фазы; выпуклость кривых в сторону
компонента В.
– кривые
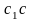 и
и
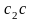 определяют состав γ
фазы; выпуклость кривых в сторону
компонента С.
определяют состав γ
фазы; выпуклость кривых в сторону
компонента С.
Получаем моновариантные линии, образующие линейчатые поверхности, которые ограничивают трехфазные эвтектические объемы. Эти объемы граничат друг с другом по коннодам aЕ, bE и cE. Проводим эти конноды пунктирными линиями. На моновариантных линиях стрелочками указываем направление изменения температуры.
одно трехфазное равновесие следует за четырехфазной реакцией:
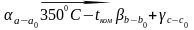
Это
равновесие осуществляется вплоть до
комнатной температуры в объеме, нижней
границей которого является треугольник
а0b0с0.
Треугольник лежит при комнатной
температуре, поэтому чертим его пунктирной
линией. Верхней границей этого объема
является эвтектический треугольник
abc,
лежащий при температуре 350оС,
чертим его сплошной линией. Проводим
моновариантные линии
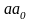 ,
,
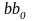 и
и
 ,
изображающие изменение растворимости
двух компонентов в третьем при понижении
температуры от эвтектической
до комнатной. Изменение температуры
указываем стрелочками. Эти моновариантные
линии также образуют линейчатые
поверхности, ограничивающие трехфазный
объем
,
изображающие изменение растворимости
двух компонентов в третьем при понижении
температуры от эвтектической
до комнатной. Изменение температуры
указываем стрелочками. Эти моновариантные
линии также образуют линейчатые
поверхности, ограничивающие трехфазный
объем
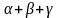 .
.
Соединим точки и , и , и , и ; и , и пунктирными кривыми выпуклостью в сторону однофазных областей. Полученные линии соответствуют составам α, β и γ фаз при комнатной температуре.
Проекция диаграммы состояния тройной системы А-В-С с четырехфазным эвтектическим равновесием на плоскость концентрационного треугольника представлена на рис. 4.
Рис.4
