
- •Лекції з фізики основи молекулярної фізики і термодинаміки
- •Лекція 8
- •Основи молекулярної фізики і термодинаміки
- •Молекулярно-кінетична теорія ідеального газу
- •Основні положення молекулярно-кінетичної теорії
- •Статистичний і термодинамічний методи
- •Макроскопічні параметри стану речовини
- •Ідеальний газ. Дослідні закони ідеального газу
- •Рівняння стану ідеального газу
- •Основне рівняння мкт
- •Середня довжина вільного пробігу молекул
- •Вакуум. Розріджені гази
- •Лекція 9
- •Явища переносу у термодинамічно нерівноважних системах
- •Статистичні розподіли. Закон Максвелла про розподіл молекул за швидкостями теплового руху
- •Барометрична формула. Розподіл Больцмана
- •Лекція 10
- •Основи термодинаміки
- •Закон рівномірного розподілу енергії за ступенями вільності молекул
- •Внутрішня енергія, робота, теплота
- •Перший закон термодинаміки
- •Робота газу. Графічний зміст роботи
- •Теплоємність
- •Застосування першого закону термодинаміки до ізопроцесів ідеального газу
- •Адіабатний процес
- •Лекція 11
- •Коловий процес. Оборотні й необоротні процеси
- •Тепловий двигун. Цикл Карно для теплових двигунів
- •Другий закон термодинаміки
- •Поняття ентропії
- •Статистичний зміст ентропії
- •Лекція 12
- •Реальні гази. Тверді тіла
- •Сили міжмолекулярної взаємодії
- •Рівняння Ван-дер-Ваальса
- •Ізотерми реального газу
- •Внутрішня енергія реального газу
- •Тверді тіла. Моно- і полікристали
- •Типи кристалічних решіток твердих тіл
- •Дефекти у кристалах
- •Теплоємність твердих тіл
- •Фазові переходи
- •Діаграма стану
- •Список літератури Основна
- •Додаткова
- •1 Основні й похідні одиниці системи сі в молекулярній фізиці і термодинаміці
- •2 Десяткові множники та приставки
- •3 Грецький алфавіт
- •4 Латинський алфавіт
- •39600, М. Кременчук, вул. Першотравнева, 20
Типи кристалічних решіток твердих тіл
Усі кристали можна класифікувати за двома ознаками:
кристалографічна ознака класифікує кристали, ураховуючи тільки просторову періодичність у розташуванні частинок;
фізична ознака класифікує кристали залежно від виду частинок, які розташовані у вузлах решітки.
 Головна
відмінність періодичної структури –
це її симетрія, тобто властивість
суміщатися із собою при деяких просторових
переміщеннях, наприклад. при паралельному
переносі, повороті і т.ін. Кристалічній
решітці відповідають 230 комбінацій
елементів симетрії. З переносною
симетрією пов’язане поняття тривимірної
періодичної структури – просторової
решітки або решітки Браве, яка може
бути складена повторенням у просторі
одного й того самого елементу –
елементарної комірки. Усього існує
14 типів решітки Браве, які різняться
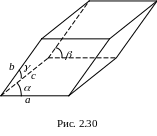
типом симетрії. Елементарна комірка –
це паралелепіпед, параметри якого –
ребра a, b, c і кути ,
,
(рис. 2.30).
Головна
відмінність періодичної структури –
це її симетрія, тобто властивість
суміщатися із собою при деяких просторових
переміщеннях, наприклад. при паралельному
переносі, повороті і т.ін. Кристалічній
решітці відповідають 230 комбінацій
елементів симетрії. З переносною
симетрією пов’язане поняття тривимірної
періодичної структури – просторової
решітки або решітки Браве, яка може
бути складена повторенням у просторі
одного й того самого елементу –
елементарної комірки. Усього існує
14 типів решітки Браве, які різняться
типом симетрії. Елементарна комірка –
це паралелепіпед, параметри якого –
ребра a, b, c і кути ,
,
(рис. 2.30).
За фізичними ознаками розрізняють 4 типи кристалів.
Атомні кристали. У вузлах кристалічної решітки знаходяться нейтральні атоми, які утримуються ковалентним зв’язком квантово-механічного походження. Типові представники: алмаз, графіт, германій, кремній.
Молекулярні кристали. У вузлах знаходяться нейтральні молекули, між якими діють Ван-дер-Ваальсові сили притягання. До молекулярних кристалів належать лід Н2О, сухий лід СО2.
Іонні кристали. У вузлах кристалічної решітки почергово знаходяться іони різних знаків. Зв’язок між ними зумовлений електричними (кулонівськими) силами притягання. Типовий представник – сіль NaCl.
Металічні кристали. У вузлах кристалічної решітки знаходяться позитивно заряджені іони металу, між якими рухаються вільні (валентні) електрони, що утворюють електронний газ. Зв’язок у металічних кристалах забезпечений силами притягання між позитивними іонами у вузлах кристала і негативним електронним газом.
Дефекти у кристалах
Міцність кристалів залежить від виду зв’язку між частинками, з яких побудований кристал, від типу симетрії, від кількості сусідів у частинок, тобто, насамперед, від упаковки кристала. Але ідеально правильна структура може існувати тільки у малих об’ємах.
В ідхилення
від впорядкованого розташування частинок
у вузлах решітки називаються дефектами
кристалічної решітки. Існують
макроскопічні дефекти, які звичайно
виникають на стадії утворення і росту
кристалів (тріщини, сторонні вкраплення),
а також мікроскопічні дефекти, що
зумовлені відхиленнями від періодичності
на атомарному рівні.
ідхилення
від впорядкованого розташування частинок
у вузлах решітки називаються дефектами
кристалічної решітки. Існують
макроскопічні дефекти, які звичайно
виникають на стадії утворення і росту
кристалів (тріщини, сторонні вкраплення),
а також мікроскопічні дефекти, що
зумовлені відхиленнями від періодичності
на атомарному рівні.
Мікроскопічні дефекти поділяються на точкові та лінійні. До точкових дефектів належать вакансії, міжвузлові атоми і домішкові атоми. Вакансія – це відсутність атома у вузлі решітки. Міжвузловий атом – це атом, що проник у міжвузловий простір. Домішковий атом – це атом домішки, що замістив атом основної речовини у вузлі, або той, що проник між вузлами (рис. 2.31.).
Лінійні дефекти або дислокації – це дефекти, які порушують правильність чергування атомних площин у кристалі. Крайова дислокація виникає у результаті зміщення атомних площин, коли одна з них обривається у середині кристалу. Гвинтова дислокація виникає, коли кристал фактично складається з однієї атомної площини, яка вигнута по гвинтовій лінії. Дислокації істотно впливають на фізичні властивості кристалів.
