
- •© Зимон а.Д., , Евтушенко а.М., Крашенинникова и.Г. Учебно-практическое пособие. – м., мгуту, 2004.
- •Свойства дисперсных систем
- •Оптические свойства дисперсных систем
- •8.1. Оптические свойства высокодисперсных систем
- •8.2. Оптическая плотность (экстинкция)
- •Молекулярно-кинетические свойства высокодисперсных систем
- •9.1. Причина молекулярно-кинетических свойств
- •9.2. Броуновское движение
- •9.3. Диффузия
- •9.4. Осмос
- •Устойчивость дисперсных систем
- •10.1. Проблема устойчивости дисперсных систем
- •10.2. Седиментационная устойчивость
- •10.3. Кинетика коагуляции
- •10.4. Термодинамические основы и факторы устойчивости дисперсных систем
- •10.5. Расклинивающее давление и теория длфо
- •10.6. Расклинивающее давление и агрегативная устойчивость
- •10.7. Изменение агрегативной устойчивости при помощи электролитов
- •10.8. Особенности агрегативной устойчивости лиофобных дисперсных систем и структурно-механический барьер
- •Структурно-механические свойства дисперсных систем
- •11.1. Образование, особенности и разрушение структурированных систем
- •11.2. Прочность и вязкость дисперсных систем
- •Получение и очистка дисперсных систем
- •12.1. Классификация способов получения дисперсных систем
- •(В скобках указан вид систем)
- •12.2. Диспергирование
- •12. 3. Получение дисперсных систем за счет конденсационных процессов
- •12.4. Мембраны и мембранные процессы
- •12.5. Мембранная технология и ее применение в промышленности
- •Тесты для самостоятельной проработки
- •Ответы на тесты для самостоятельной проработки
- •Вопросы для самоконтроля
- •Список литературы
- •Физическая и коллоидная химия.
- •Коллоидная химия
- •Раздел второй
- •Учебно-практическое пособие
10.6. Расклинивающее давление и агрегативная устойчивость
Потенциальный барьер и потенциальные ямы определяют агрегативную ycтойчивость и возможность коагуляции в зависимости от кинетической энергии частиц дисперсной фазы, которая определяется величиной kT (k — константа Больцмана), и характеризует энергию взаимодействия частиц, т.е. энергетический аспект этого взаимодействия.
Следует рассмотреть три возможных случая. При высоком потенциальном барьере, превышающем kT, и незначительной второй потенциальной яме (<kT) частицы не в состоянии преодолеть потенциальный барьер; коагуляция отсутствует и соблюдается устойчивость дисперсных систем с жидкой дисперсионной средой. Поэтому потенциальный барьер называют и коагуляционным барьером.
Когда потенциальный барьер и второй минимум незначительны (т.е. kT → 0), частицы в состоянии преодолеть потенциальный барьер и попасть в первую потенциальную яму; что приводит к коагуляции частиц и нарушению агрегативной устойчивости.
При средних значениях второй потенциальной ямы и потенциального барьера частицы не могут подойти друг к другу, и наблюдается фиксированное положение частиц при определенном достаточно большом расстоянии между ними.
На основании представлений о расклинивающем давлении можно определить силу и энергию аутогезии между двумя частицами, а также энергию и силу адгезии частиц в жидкой среде. Согласно теории Дерягина-Брэдли сила и удельная энергия (работа) аутогезионного (адгезионного) взаимодействия выражаются формулами (10.25) и (10.30).
Величина π(h) характеризует изменение расклинивающего давления (см. рис. 10.5, б) в зависимости от расстояния между частицами h. При помощи соотношений (10.25) и (10.31) можно проследить влияние на адгезию и аутогезию свойств жидкой среды, определяющих электростатическое отталкивание, адсорбционных процессов, рН среды и др.
Работа Wког, затрачиваемая на преодоление потенциального барьера и обусловливающая коагуляцию твердых недеформированных частиц, приближенно можно выразить следующим образом:
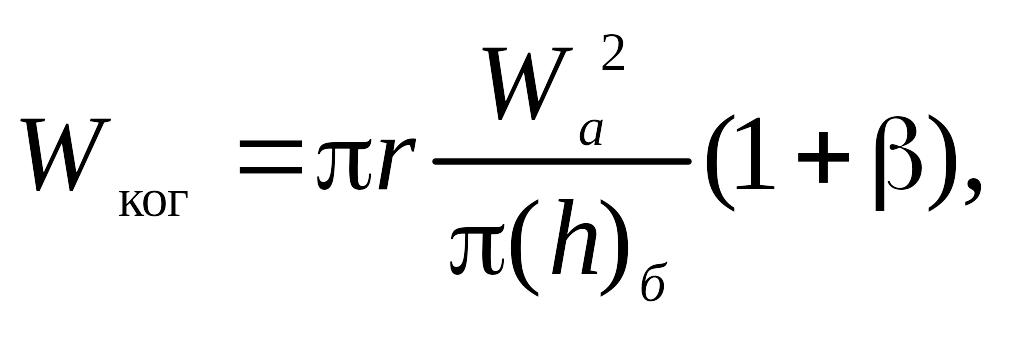 (10.32)
(10.32)
где
![]() ;
π(h)б
и p(h)п
— расклинивающее давление, соответствующее
;
π(h)б
и p(h)п
— расклинивающее давление, соответствующее
потенциальному барьеру и второй потенциальной яме (см. рис. 10.5, б).
Энергия (работа), которую следует затратить на преодоление аутогезионного взаимодействия между частицами (т.е. для отрыва частиц друг от друга) и осуществить процесс, обратный коагуляции, определяется по формуле
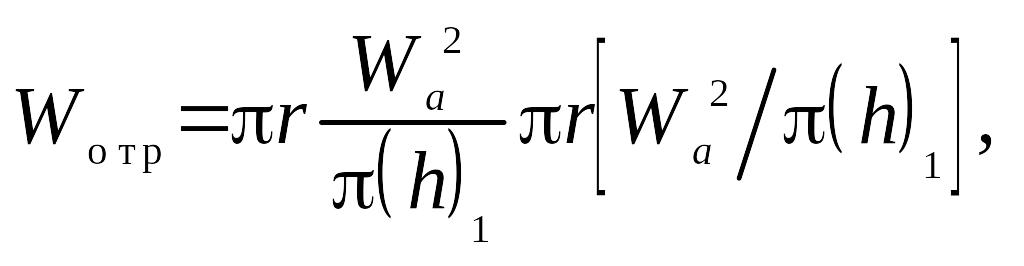 (10.33)
(10.33)
где π(h)1 — расклинивающее давление, соответствующее первой потенциальной яме.
Следует обратить внимание на то, что, согласно формулам (10.32) и (10.33), работа формирования аутогезии частиц в процессе коагуляции и работа преодоления взаимодействия слипшихся частиц не равны между собой, что является следствием изменения расклинивающего давления в зависимости от расстояния между частицами.
Работа, определяемая при помощи формул (10.32) и (10.33), характерна для твердых, не подвергшихся деформации шарообразных частиц. В случае взаимодействия между двумя одинаковыми жидкими или газообразными частицами в эмульсиях и пенах (см. гл. 15 и 16), которые называют текучими в связи с подвижностью границы раздела, изменяется их профиль.
С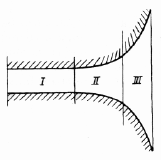 ледует
рассматривать три области: I
— плоскопараллельную, II
— переходную и III
— объемного мениска (рис. 10.6). Межфазовое
поверхностное натяжение в плоскопарал-лельной
области является постоянным, а в области
объемного мениска определяется условием
(2.23) (см. гл. 2) и зависит от радиуса
кривизны поверхности мениска. Кривизна
поверхности в переходной области не
является постоянной, что обусловливает
переменное расклинивающее давление и
межфазовое поверхностное натяжение.
ледует
рассматривать три области: I
— плоскопараллельную, II
— переходную и III
— объемного мениска (рис. 10.6). Межфазовое
поверхностное натяжение в плоскопарал-лельной
области является постоянным, а в области
объемного мениска определяется условием
(2.23) (см. гл. 2) и зависит от радиуса
кривизны поверхности мениска. Кривизна
поверхности в переходной области не
является постоянной, что обусловливает
переменное расклинивающее давление и
межфазовое поверхностное натяжение.
С учетом особенностей взаимодействия текучих частиц сила аутогезии между каплями и пузырьками будет определяться следующим уравнением:
 (10.34)
(10.34)
П
Рис. 10.6.
Области, характеризующие поверхность
контактирующих текучих частиц
Кроме того, под действием внешней силы Рп может происходить деформация текучих частиц, в результате чего изменяется работа при контакте, последующей коагуляции и отрыве таких частиц. Соотношение между Wотр и Wког имеет вид
Wотр = Wког(1 + α1 + α2), (10.35)
где α1 = π(h)б/Pп; α2 = π(h)п/Рn.
Проведенный анализ позволяет выразить условия агрегативной устойчивости эмульсий в случае необратимой коагуляции при Wког >> kT:
 (10.36)
(10.36)
Условие, определяющее самопроизвольное диспергирование осадка эмульсий, выглядит так:
Wотр = 1 + α1 + α2 < Б, (10.37)
где Б — константа.
Влияние межфазового поверхностного натяжения на агрегативную устойчивость эмульсий и их способность к самопроизвольному диспергированию зависит от наличия потенциального барьера на изотерме поверхностного натяжения. При отсутствии потенциального барьера, когда π(h)б = 0 (см. рис. 10.5, б), по мере уменьшения межфазового поверхностного натяжения агрегативная устойчивость эмульсий снижается. Если потенциальный барьер будет значительным, то с уменьшением межфазового поверхностного натяжения наблюдается противоположный эффект, т.е. агрегативная устойчивость эмульсий растет.
Теория ДЛФО и учение о расклинивающем давлении постоянно совершенствуются и развиваются. Межмолекулярное взаимодействие и электростатическое отталкивание являются составляющими расклинивающего давления. Помимо них различают еще адсорбционную и структурную составляющие.
Адсорбционная составляющая расклинивающего давления связана с перераспределением молекул растворителя вблизи поверхности раздела фаз. В результате адсорбции концентрация веществ в тонкой пленке отличается от их концентрации в объеме жидкости. Перекрытие адсорбционных слоев под действием возникающих поверхностных сил (см. рис. 10.4) связано с изменением концентрации раствора и приводит к появлению дополнительной силы (отталкивания или притяжения) между двумя поверхностями, ограничивающими прослойку жидкости. Эта дополнительная сила и составляет адсорбционную компоненту расклинивающего давления πа(h).
В граничных жидких слоях образуются структуры, которые отличаются от структуры этой же жидкости в объеме. Структуры, например, могут возникнуть в связи с сольватацией (в случае воды — гидратацией) поверхности частиц 1 (рис. 10.7) и образованием сольватной (гидратной) оболочки 2. При сближении частиц сольватные слои перекрываются, изменяются структура жидкости и свободная энергия системы [см. формулу (10.24)]. Возникает дополнительная сила отталкивания (или притяжения), вызванная структурной составляющей расклинивающего давления.
К роме
того, возможно отталкивание (позиция
7
на рис. 10.7) одноименно заряженных групп
молекул (например, молекул воды),
образующих сольватную (гидратную)
оболочку. Отталкивание может оказать
влияние на структурную составляющую
расклинивающего давления.
роме
того, возможно отталкивание (позиция
7
на рис. 10.7) одноименно заряженных групп
молекул (например, молекул воды),
образующих сольватную (гидратную)
оболочку. Отталкивание может оказать
влияние на структурную составляющую
расклинивающего давления.
Т
Рис.
10.7.
Образование структурной составляющей
расклинивающего давления между
частицами 1
за счет
перекрытия 3
сольватных слоев 2:
4, 5, 6
— полярные молекулы сольватной
оболочки; 7
— сила отталкивания между одноименно
заряженными молекулами сольватной
оболочки
π(h) = πэ(h) + πм(h) + πa(h) + πc(h). (10.38)
Сочетание этих составляющих, которые проявляются в различных условиях, зависит от свойств дисперсной фазы и дисперсионной среды и определяет более сложный, чем приведенный на рис. 10.5, б, характер зависимости взаимодействия частиц на различных расстояниях, их разделяющих.
