
Окислительное фосфорилирование
Как вырабатывается энергия в клетке в результате распада углеводов? Частично АТФ, как основной макроэрг клетки, может образоваться путем субстратного фосфорилирования. Но главным процессом синтеза АТФ является окислительное фосфорилирование.
Окислительным фосфорилированием называют процесс образования АТФ из АДФ и ФН, сопряженный с транспортом электронов, при котором электроны высокоэнергетического восстановленного донора переносятся промежуточными переносчиками электронов к конечному акцептору электронов - кислороду - с образованием низкоэнергетического восстановленного продукта.
Этот процесс является общим для всех организмов и представляет собой универсальный биохимический путь.
Окислительное фосфорилирование включает два процесса:
а) окисление восстановленных молекул, таких как НАДН или ФАДН2 в ходе нескольких реакций переноса электронов, при этом выделяется энергия;
б) фосфорилирование АДФ с образованием АТФ, которое требует за трат энергии.
Хотя это отдельные процессы, но энергетически они сопряжены: все молекулы, участвующие в каждом из процессов, находятся в одном компартменте - внутренней мембране митохондрий и, благодаря согласованному действию всех участников процесса, та энергия, которая выделяется при переносе электронов, используется для синтеза АТФ.
При переносе электронов возникает разность потенциалов, равная разности между потенциалом восстанавливаемой пары и потенциалом окисляемой пары.
Механизм окислительного фосфорилирования
Для объяснения механизма сопряжения дыхания и фосфорилирования выдвинут ряд гипотез. Рассмотрим три основных.
Механохимическая, или конформационная (Грин, Бойер, 60-е гг. XX в.). В процессе переноса протонов и электронов изменяется конформация белков-ферментов. Они переходят в новое богатое энергией конформационное состояние, а затем при возвращении в исходную конформацию отдают энергию для синтеза АТФ. Гипотеза частично подтверждена:
E0 → Eконформ. сдвигов → E АТФ
Гипотеза химического сопряжения (Липман, Слейтер, Ленинджер, 30-40-е гг. XX в.). В сопряжении дыхания и фосфорилирования участвуют сопрягающие вещества, например вещество "X". Вещество "X" акцептирует протоны и электроны от первого фермента в пункте сопряжения, взаимодействует с Н3РО4. В момент отдачи протонов и электронов второму ферменту пункта сопряжения связь с фосфатом становится макроэргической. Далее макроэрг передается на АДФ с образованием АТФ. Гипотеза логична, но не выделены сопрягающие вещества ("А").
Хемиоосмотическая гипотеза Митчелла (1961). Поданной гипотезе, дыхание и фосфорилирование связаны между собой электрохимическим потенциалом (ЭХП ) на внутренней мембране митохондрий. Для понимания этой гипотезы необходимо знать следующее:
Внутренняя мембрана митохондрий непроницаема для Н+ и ОН-
Во внутреннюю мембрану митохондрий вмонтирована аденозинтрифосфатаза, катализирующая обратимую реакцию:
АТФ + Н2О ↔ АДФ + Н3РО4.
А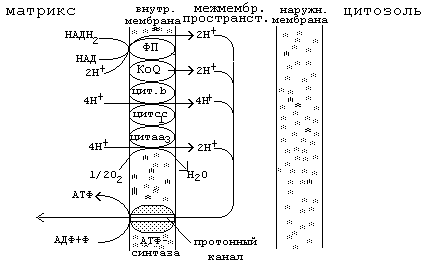 ТФаза
состоит из следующих субъединиц: F0
- это, во-первых, гидрофобный сегмент
из четырех полипептидных цепей, связанный
с внутренней мембраной митохондрий;
во-вторых, это протонный канал, по
которому в норме могут перемещаться
только протоны через мембрану; F1-
сопрягающий фактор, катализирующий
синтез АТФ при перемещении протонов (1
АТФ на 2Н+). Стебелек между F0и
F1 содержит белок,
чувствительный к олигомицину - антибиотику,
блокирующему синтез АТФ путем нарушения
использования протонного градиента. В
укороченной цепи переноса электронов
отсутствует только первый этап, остальной
перенос электронов такой же, как в полной
цепи.
ТФаза
состоит из следующих субъединиц: F0
- это, во-первых, гидрофобный сегмент
из четырех полипептидных цепей, связанный
с внутренней мембраной митохондрий;
во-вторых, это протонный канал, по
которому в норме могут перемещаться
только протоны через мембрану; F1-
сопрягающий фактор, катализирующий
синтез АТФ при перемещении протонов (1
АТФ на 2Н+). Стебелек между F0и
F1 содержит белок,
чувствительный к олигомицину - антибиотику,
блокирующему синтез АТФ путем нарушения
использования протонного градиента. В
укороченной цепи переноса электронов
отсутствует только первый этап, остальной
перенос электронов такой же, как в полной
цепи.
Синтез АТФ осуществляется при перемещении протонов через АТФазу в направлении от ММП к матриксу.
В мембране митохондрий существует активный перенос протонов. Это означает перенос Н+ изнутри митохондрий наружу - такое явление называют работой протонного насоса.
Перенос протонов приводит к возникновению разности концентраций Н+ с двух сторон митохондриальной мембраны, так что более высокая концентрация будет снаружи, более низкая - внутри.
Возникает градиент концентрации Н+, или рН, который способен совершать работу. Выкачивание протонов из митохондрий приводит также к появлению мембранного электрического потенциала, так как в результате выхода ионов Н+ из матрикса в среду наружная сторона мембраны становится более электроположительной, а внутренняя - более электроотрицательной. Таким образом, перенос электронов создает электрохимический градиент ионов Н+, включающий два компонента - градиент рН и мембранный потенциал:
£° = А0 - ZApH,
где е° - электрохимический потенциал; Аф - мембранный потенциал; ZApH -градиент рН.
Большую часть электрохимического потенциала составляет мембранный потенциал, а в градиенте рН коэффициент Z служит для перевода рН в милливольты. Зная общую величину изменения электрохимического потенциала, можно найти и величину изменения свободной энергии.
Основное положение хемиоосмотической теории Митчелла: свойства митохондриальной мембраны, содержащей протонный насос, создают электрохимический градиент, обладающий потенциальной энергией.
Дыхательная цепь транспорта электронов обеспечивает работу протонных насосов, которые используют свободную энергию потока электронов для перекачивания протонов наружу, против градиента концентрации Н+. В результате, как отмечено выше, возникает электрохимический потенциал. Затем выведенные наружу ионы Н+ снова устремляются внутрь через специальные каналы или поры для этих ионов в мембране. В дыхательной цепи электроны идут по градиенту концентрации, и во время их перехода через молекулу АТФ выделяется энергия. Именно эта свободная энергия и служит движущей силой для сопряженного синтеза АТФ из АДФ и фосфата.
Хемиоосмотическая теория не требует никакого промежуточного продукта, который бы обеспечивал сопряжение между переносом электронов и синтезом АТФ. Источником энергии, связывающем окисление и фосфори-лирование, служит градиент концентрации ионов Н+ (при этом важна целостность мембран и специфическая ориентация протонного насоса, откачивающего протоны изнутри митохондрий наружу). Итак, между митохондрией и окружающей средой совершается непрерывный круговорот ионов Н+, за счет которого и синтезируется АТФ.
Разобщение дыхания и окислительного фосфорилирования возникает при повышении проницаемости мембраны митохондрий для протонов в любом месте, а не только в канале АТФазы. При этом не создается электрохимический потенциал и энергия окисления рассеивается в виде тепла. Так действуют ионофоры (2,4-динитрофенол, валиномицин и др.). Они переносят протоны обратно через мембрану, выравнивая градиенты рН и мембранного потенциала. На разобщении дыхания и фосфорилирования базируется терморегуляторная функция тканевого дыхания. Тканевое дыхание, протекающее в митохондриях и не сопровождающееся образованием макроэргов, называют свободным, или нефосфорилирующим, окислением. Образованная в результате окислительного фосфорилирования в митохондриях АТФ обменивается на внемитохондриальную АДФ с помощью специальных белков - транслоказ (составляют до 6% от всех белков внутренней мембраны митохондрий).
Гипоэнергетические состояния возникают: 1) при нарушении поступления субстратов для дегидрирования (на всех этапах от пищи до матрикса митохондрий); 2) при нарушении поступления О2 в митохондрии (на всех этапах от дыхания, связь с Нb, транспорт и др.); 3) при нарушении мембран митохондрий, композиции липидного бислоя и ферментативных ансамблей внутренней мембраны митохондрий.
