
- •Кафедра строительного производства строительные материалы Учебно-методический комплекс
- •Кафедра строительного производства
- •Строительные материалы Учебно-методический комплекс
- •Кафедра строительного производства
- •Рабочая программа дисциплины «строительные материалы»
- •Направление подготовки: 270100 «Строительство»
- •Дополнения и изменения в рабочей программе на 200__/200__уч.Г.
- •Пояснительная записка к рабочей программе учебной дисциплины «Строительные материалы»
- •7.1. Разделы дисциплины и виды занятий
- •7.2. Содержание разделов дисциплины
- •Тема I. Введение
- •Тема 2. Строение и свойства материалов
- •Тема 3. Материалы и изделия из природного камня
- •Тема 4. Керамические материалы и изделия
- •Тема 5. Стекло и плавленые изделия
- •Тема 6. Неорганические вяжущие вещества
- •Тема 7. Металлические материалы и изделия из них
- •Тема 8. Бетоны и бетоноведение
- •Тема 9. Технология сборных железобетонных изделий и конструкций
- •Тема 10. Строительные растворы
- •Тема 11. Автоклавные материалы и изделия
- •Тема 12. Композиционные материалы и изделия
- •Тема 13. Материалы и изделия из древесины
- •Тема 14. Органические вяжущие вещества и материалы на их основе
- •Тема 15. Полимерные материалы и изделия
- •Тема 16. Теплоизоляционные материалы и изделия
- •Тема 17. Акустические материалы
- •Тема 18. Отделочные материалы
- •7.3. Лабораторный практикум
- •8. Самостоятельная и исследовательская работа
- •11. Методические рекомендации по организации изучения дисциплины.
- •12.1. Рекомендуемая литература
- •Кафедра строительного производства Популов м.Ф. Строительные материалы
- •Лабораторная работа № 1. Определение насыпной плотности цемента.
- •Лабораторная работа № 2. Определение нормальной густоты цементного теста.
- •Лабораторная работа № 3. Определение сроков схватывания цементного теста.
- •Лабораторная работа № 4. Определение нормальной густоты гипсового теста.
- •Лабораторная работа № 5. Определение сроков схватывания гипсового теста.
- •Лабораторная работа № 6. Определение истинной плотности песка.
- •Лабораторная работа № 10. Определение зернового состава песка.
- •Лабораторная работа № 11. Определение средней плотности зерен щебня (гравия).
- •Лабораторная работа № 12. Определение насыпной плотности щебня (гравия).
- •Лабораторная работа № 14. Определение водопоглошения щебня (гравия).
- •Лабораторная работа № 15. Определение зернового состава нефракционированного гравия.
- •Лабораторная работа № 16. Определение подвижности бетонной смеси.
- •Лабораторная работа № 17. Определение плотности бетона.
- •Лабораторная работа № 18. Определение подвижности растворной смеси.
- •Лабораторная работа № 19. Определение водопоглощения керамических плиток для полов.
- •Кафедра строительного производства
- •Строительные материалы
- •Популов м.Ф.
- •Методические указания к самостоятельной работе
- •270102 «Промышленное и гражданское строительство»
- •Тема I. Введение
- •Тема 2. Строение и свойства материалов
- •Тема 3. Материалы и изделия из природного камня
- •Тема 4. Керамические материалы и изделия
- •Тема 5. Стекло и плавленые изделия
- •Тема 6. Неорганические вяжущие вещества
- •Тема 7. Металлические материалы и изделия из них
- •Тема 8. Бетоны и бетоноведение
- •Тема 9. Технология сборных железобетонных изделий и конструкций
- •Тема 10. Строительные растворы
- •Тема 11. Автоклавные материалы и изделия
- •Тема 12. Композиционные материалы и изделия
- •Тема 13. Материалы и изделия из древесины
- •Тема 14. Органические вяжущие вещества и материалы на их основе
- •Тема 15. Полимерные материалы и изделия
- •Тема 16. Теплоизоляционные материалы и изделия
- •Тема 17. Акустические материалы
- •Тема 18. Отделочные материалы
- •Формы контроля
- •Контрольная работа 1
- •Контрольная работа 2
- •Приложения
- •Конспект лекций
- •Строительные материалы
- •270102 – Промышленное и гражданское строительство
- •Разработал доцент кафедры строительного производства
- •Тема I. Введение
- •Тема 2. Строение и свойства материалов
- •Тема 3. Материалы и изделия из природного камня
- •Тема 4. Керамические материалы и изделия
- •Тема 5. Стекло и плавленые изделия
- •Тема 6. Неорганические вяжущие вещества
- •Тема 7. Металлические материалы и изделия из них
- •Тема 8. Бетоны и бетоноведение.
- •Тема 9. Технология сборных железобетонных изделий и конструкций
- •Тема 10. Строительные растворы
- •Тема 11. Автоклавные материалы и изделия
- •Тема 12. Композиционные материалы и изделия
- •Тема 13. Материалы и изделия из древесины
- •Тема 14. Органические вяжущие вещества и материалы на их основе
- •Тема 15. Полимерные материалы и изделия
- •Тема 16. Теплоизоляционные материалы и изделия
- •Тема 17. Акустические материалы
- •Тема 18. Отделочные материалы
- •Методические рекомендации преподавателю по учебной дисциплине «Строительные материалы»
- •Активизация студентов
- •Требования к преподавателю
Тема 7. Металлические материалы и изделия из них
Производство и обработка металлов возникли очень давно. Сначала человек использовал самородные металлы и освоил их обработку, затем научился выплавлять металлы и сплавлять их друг с другом, а затем настал железный век. Первыми пла-вильными агрегатами для получения железа из руд были неглубокие, земляные ямы (горны), в которые загружали железную руду и древесный уголь. При переплавке руды она превращалась в сыродутное железо в виде комков (железных криц), после чего подвергалась ковке. В XIII—XIV вв. нашей эры сыродутные горны замени-ли круглыми шахтными печами — домницами. В них развивались более высо-кие температуры и происходило насыщение железа углеродом. В результате в ниж-ней части домницы получался жидкий металл — чугун. Из него затем получа-ли простые отливки (плиты, шары и т.д.).
Примерно в середине XIV в. стали перерабатывать хрупкий чугун в ков-кий и прочный металл — сталь, выжигая углерод из жидкого чугуна в так на-зываемых кричных горнах, которые впоследствии были заменены более совер-шенными способами передела чугуна, такими как пудлинговый, бессемеровс-кий, томасовский, мартеновский. Последние три вместе с разработанным в се-редине XX в. кислородно-конверторным являются основными способами прои-зводства стали в настоящее время.
Существенную роль в развитии отечественной металлургии сыграли ра-боты российских ученых — М.В. Ломоносова, М.А. Павлова, А.А. Байкова, И. П. Бардина и др. Наши соотечественники П.П. Аносов, Д.К. Чернов в XIX в. За-ложили основы металловедения — науки о строении металлов и сплавов. В на-стоящее время металловедение и смежные с ним науки обладают глубокими знаниями о строении металлов и сплавов и природе внутренних связей в них. На основе этих знаний разработаны методы термической обработки металлов и сплавов, позволяющие изменять их свойства в нужном направлении.
Строение металлов.
Все вещества в твердом состоянии имеют кристаллическое или аморф-ное строение. В аморфном веществе атомы или молекулы расположены хао-тично, в то время как в кристаллическом веществе — в строго определенном порядке, и каждая элементарная кристаллическая ячейка представляет собой пространственную геометрическую фигуру. Металлы, в основном, имеют 3 ви-да кристаллических решеток — кубические (объемно- и гранецентрирован-ные) и гексагональные.
Возможны два вида формирования структуры — монокристаллическая и поликристаллическая. Под монокристаллом понимают строго упорядоченную систему элементарных ячеек, в то время как поликристаллическое строение ха-рактеризуется хаотичным расположением огромного количества элементар-ных ячеек. Существование одного и того же металла в нескольких кристалли-ческих формах называется аллотропией или полиморфизмом, а процесс изме-нения кристаллической решетки носит название аллотропического или поли-морфного превращения.
Поскольку полиморфные превращения связаны с формированием новой кристаллической решетки, естественно, меняются и свойства металла. Таким образом, не атомы являются мельчайшими частицами вещества, отражающи-ми его свойства, а именно элементарные кристаллические ячейки, и от того, как и какими модификациями металла будет сформирована кристаллическая структура, будут и свойства металла. Другими словами, свойства металла це-ликом и полностью зависят от его структуры, и любое изменение ее неизбежно приведет к изменению свойств. Температуры, при которых происходят ал-лотропические превращения, называют критическими.
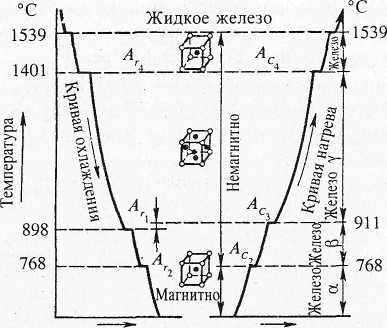
Время Время
Рис. 7.1. Аллотропические превращения железа при охлаждении и нагреве.
Свойства металлов.
Механические свойства характеризуют способность материала сопроти-вляться внешним механическим воздействиям. К основным механическим свойствам относятся прочность, пластичность, твердость, ударная вязкость и др. Механические свойства определяют при испытаниях на одноосное растя-жение. Под деформацией понимают относительное приращение длины. В результате испытаний получают ряд характеристик —предел пропорциональнос-ти — наибольшее напряжение, соответствующее пропорциональному увеличе-нию деформации (закон Гука), предел упругости — величина напряжения, вы-зывающего остаточное удлинение, равное 0,005% от начальной длины, предел текучести— наименьшее напряжение, при котором образец деформируется без заметного увеличения нагрузки; предел прочности — максимальное нап-ряжение, которое образец выдерживает до разрушения.
Полная
деформация образца
![]() складывается из остаточной
складывается из остаточной
![]() и уп-ругой деформации
и уп-ругой деформации
![]() .
Для определения этих
деформаций необходимо на диаграмме
растяжения из точки
А провести прямую, параллельную
прямо-линейному
участку кривой, до пересечения с осью
абсцисс. Для оценки плас-тичности
используют характеристику, называемую
относительным
удлине-нием
.
Для определения этих
деформаций необходимо на диаграмме
растяжения из точки
А провести прямую, параллельную
прямо-линейному
участку кривой, до пересечения с осью
абсцисс. Для оценки плас-тичности
используют характеристику, называемую
относительным
удлине-нием
![]()
где
![]() -
конечная длина образца, перед разрывом,
мм;
-
конечная длина образца, перед разрывом,
мм;
![]() -
начальная длина образца, мм.
-
начальная длина образца, мм.
Нетрудно видеть, что стали, имеющие большую полную деформацию и, следовательно, большую пластичность, имеют меньшую прочность и пре-дел пропорциональности.
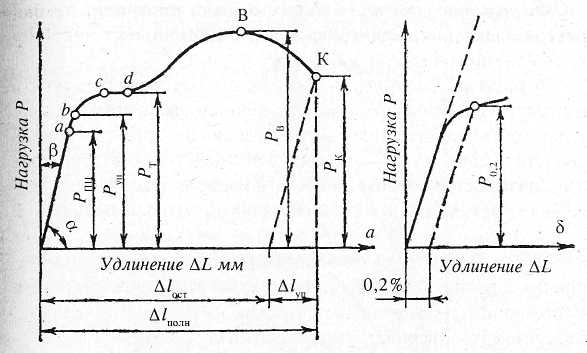
Рис. 7.2. Диаграмма растяжения низкоуглеродистой стали.
Величина
напряжения, характеризуемая углом
наклона прямой
линии ди-аграммы к оси абсцисс, носит
название модуль Юнга или модуль упругости. Модуль
упругости является очень важной
механической характеристикой,
так как он определяет жесткость
конструкции
Е∙I,
где I
— момент инерции сечения. Не-которые
сплавы могут
иметь достаточно высокие прочностные
свойства, однако
низкий модуль упругости не позволяет
использовать их в качестве материала
для несущих конструкций. К таким
материалам
относятся, например, алюминиевые сплавы.
Юнга или модуль упругости. Модуль
упругости является очень важной
механической характеристикой,
так как он определяет жесткость
конструкции
Е∙I,
где I
— момент инерции сечения. Не-которые
сплавы могут
иметь достаточно высокие прочностные
свойства, однако
низкий модуль упругости не позволяет
использовать их в качестве материала
для несущих конструкций. К таким
материалам
относятся, например, алюминиевые сплавы.
При выборе металла для изготовления конструкции отдают предпочтение скорее материалам более пластичным, нежели более прочным с меньшей пластич-ностью. Особенно это важно при нестатических нагрузках, что довольно часто имеет место в строительстве. В качестве концентраторов напряжений могут быть раз-личные изменения в сечении, дефекты на поверхности и внутри металла, сварные швы, зоны металла с различными механическими характеристиками и т.д.
Твердость по Бринеллю. В этом случае в качестве индентора применяют стальные закаленные шарики различного диаметра, для которых выбирают различную нагрузку и время выдержки под нагрузкой. В качестве критерия оценки твердости используется диаметр отпечатка. Метод испытания по Бри-нелю применяется для оценки твердости пластичных материалов, не облада-ющих большой прочностью. Это связано с тем, что при испытании твердых металлов собственная деформация шарика существенно искажает результаты измерения.
Определение твердости по Роквеллу. При этом виде испытаний в качест-ве индентора применяют алмазный конус с углом при вершине 120° для твер-дых металлов и для относительно мягких металлов — стальной закаленный ша-рик диаметром 1,59 мм (1,16"). Преимуществом способа Роквелла является бы-строта измерений. Применение алмазного конуса позволяет измерять твер-дость специальных сталей и других твердых материалов, тонких изделий или поверхностного закаленного слоя.
Определение твердости по Виккерсу. В испытуемый материал вдавлива-ют индентор в виде алмазной четырехгранной пирамиды с углом при вершине 136° при нагрузке от 50 до 1200 Н. Критерием оценки является диагональ отпе-чатка. Преимущество метода Виккерса — возможность измерения твердости материалов как мягких, так и очень твердых, а также измерять твердость то-нких изделий, поверхностных слоев и т.д.
Как следует из оценки каждого метода исследования, в основе ле-жит пластическая деформация под индентором. В настоящее время много-чи-ленными работами исследователей установлены корреляционные связи между твердостью и другими свойствами металла. Так, установлено, что твер-дость по Бринелю связана с прочностью простой зависимостью:
R = 0,34∙НВ,
где R — предел прочности метала, МПа;
НВ — твердость по Бринелю, МПа.
Используя специальные таблицы, можно перевести твердость по Рок-веллу и Виккерсу в твердость по Бринелю. Таким образом, в инженерной пра-ктике бывает достаточным измерить твердость любым наиболее доступным методом и через твердость определить другие механические свойства матери-ала. Более того, в настоящее время разработана и применяется широкая гамма переносных приборов-твердомеров, позволяющих определять твердость не на образцах, а на действующей конструкции и таким образом можно обеспечить оценку ее состояния и прогнозирование ее дальнейшей эксплуатации.
Ударная вязкость характеризует способность материалов сопротивля-ться действию динамических, ударных нагрузок. В технике ударная вязкость определяется путем разрушения стандартных образцов прямоугольного сече-ния обычно с надрезом определенной формы и размерами для создания концентрации напряжений. Испытания производят на маятниковом копре.
Плавление и кристаллизации чистых металлов.
Все металлы находятся в твердом состоянии до определенной темпе-ратуры. Это значит, что до определенной температуры металл сохраняет свою кристаллическую структуру (решетку), в которой атомы, находящиеся в узлах кристаллической решетки, совершают колебательные движения с опреде-ленной амплитудой и частотой порядка 1013 периодов в секунду. При нагреве амплитуда перемещения атомов в узлах кристаллических решеток увеличи-вается и решетка разрушается. Этот момент и называют плавлением, и ве-щество переходит в жидкое состояние. Поскольку атомы в решетке каждого металла связаны строго определенными силами, на что указывает опреде-ленный параметр каждой кристаллической ячейки, то и энергия, необходи-мая для разрушения решетки, имеет строго определенное значение. Вот почему каждый металл имеет свою строго определенную температуру плав-ления, и эта величина является физической характеристикой металла.
При охлаждении жидкого металла избыточная свободная энергия выде-ляется из системы, что приводит к уменьшению количества движения атомов, находящихся в жидкости. Температура, при которой металл переходит из жи-дкого состояния в твердое, называется температурой первичной кристализа-ции. Кроме первичной кристаллизации возможно формирование кристалли-ческой структуры в твердом состоянии — вторичная кристаллизация, что име-ет место при аллотропических превращениях.
В отличие от температуры плавления, которая является для каждого металла физической константой, температура кристаллизации его не является величиной постоянной и зависит от скорости охлаждения.
Процесс кристаллизации начинается с образования так называемых цент-ров кристаллизации. По мере охлаждения количество центров кристаллизации возрастает. Одновременно происходит рост кристаллов правильной формы на основе ранее образованных центров кристаллизации, так как ничто не мешает их формированию. В дальнейшем кристаллы начинают сталкиваться друг с другом, правильная форма отдельных кристаллов нарушается, и образуется поликристаллическая структура с хаотическим расположением зерен, предста-вляющих собой блоки кристаллов или кристаллитов.
Таким образом, при формировании кристаллической структуры необхо-димо рассматривать два фактора — скорость роста количества центров крис-таллизации в единице объема в единицу времени и скорость роста кристаллов. Очевидно, одна и другая величины зависят от скорости охлаждения.
С увеличением скорости охлаждения число центров кристаллизации интен-сивно возрастает, что приводит к образованию мелкозернистой структуры с высо-кими механическими свойствами. Это особенно важно для формирования структуры сплавов на основе компонентов, имеющих аллотропические модификации, так как эти процессы идут не только при первичной кристаллизации, а также при прев-ращениях в твердом состоянии (вторичная кристаллизация). В частности известно, что длительное пребывание металла при высоких температурах приводит к резкому увеличению размеров зерна и существенному снижению механических характерис-тик металла. Например, при сварке неоправданное увеличение размеров сварного шва не только не увеличивает прочностные характеристики соединения, а напротив, снижает их за счет перегрева и, следовательно, ухудшения структуры.
Строение сплавов.
Чистые металлы имеют крайне ограниченное применение в технике. Это связано с тем, что свойства их, как конструкционных материалов, не всегда отвеча-ют требованиям проектировщиков.
В зависимости от физико-химической природы.компонентов возможно обра-зование следующих видов сплавов:
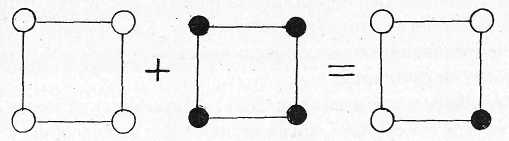
Твердые растворы. В жидком состоянии большинство металлических сплавов представляет собой жидкие растворы. При кристаллизации однородность сохраняется, следовательно, сохраняется растворимость, т.е. атомы одного компо-нента располагаются в кристаллической решетке другого компонента, и твердая фаза, образующаяся в процессе затвердевания, носит название твердого раствора. Такой механизм кристаллизации предполагает образование твердых растворов двух видов: твердые растворы замещения (рис. 7.4) и твердые растворы внедре-ния (рис. 7.5).
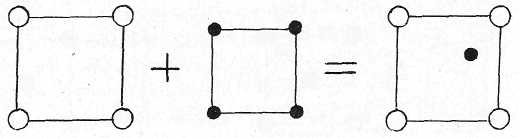
Химические соединения (рис. 7.6). Химические соединения образуют те элементы, которые способны вступать в химическое взаимодействие.
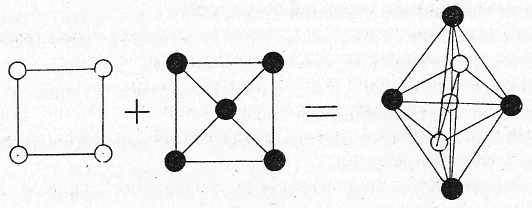
Рис. 7.6. Схема образования химического соединения
При образовании химического соединения соотношение чисел атомов элементов, как правило, соответствует стехиометрической пропорции. Если компонентами химического соединения являются металлические элементы, то такие соединения называются интерметаллическими. Свойства химических соединений существенно отличаются от свойств исходных компонентов. Как правило, химические соединения обладают очень высокой прочностью и очень низкой пластичностью.
Механические смеси (рис. 7.7). Механические смеси образуются в тех случаях, когда компоненты не способны к химическому взаимодействию и не растворяются один в другом в твердом состоянии.
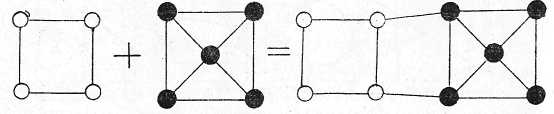
Рис. 7.7. Схема образования сплава, образующего механическую смесь.
В этом случае оба компонента кристаллизуются в свои системы, но они объединены общими связями, и элементарной кристаллической ячейкой спла-ва является сложная решетка компонентов. Свойства механических смесей за-висят от количественного соотношения, а также от размеров и формы зерен.
Диаграмма состояния сплава представляет собой графическое изобра-жение его состояния при определенных температурах и концентрациях ком-понентов. Диаграммы состояния также называют диаграммами равновесия, так как они показывают те состояния, при которых система обладает минимумом свободной энергии.
Каждая точка на диаграмме показывает состояние сплава данной конце-нтрации при данной температуре, каждая вертикаль соответствует изменению температуры для определенного сплава. Изменение фазового состава отмеча-ется точкой. Линии, соединяющие точки аналогичных превращений, разгра-ничивают на диаграмме области фазовых состояний. Вид диаграммы зависит от характера взаимодействия компонентов сплава в жидком и твердом состоя-ниях, т.е. от вида сплава.
Химический состав и структура определяют свойства металлического сплава. Структура в свою очередь зависит от характера взаимодействия ком-понентов сплава, что и отражают диаграммы состояния. Следовательно, меж-ду диаграммами состояния и полученными свойствами сплавов существует определенная зависимость (рис. 7.8).
Сплавы железа с углеродом.
Железоуглеродистые сплавы — стали и чугуны — наиболее важные ме-таллические сплавы современной техники и наиболее производимые.
Максимальное
содержание углерода в сплавах с железом
составляет
6,67%. Это значение соответствует содержанию
углерода в карбиде железа Fe3C
(цеме-нтит), который и будем рассматривать
дальше как самостоятельный компонент.
Диаграмма
состояния железоуглеродистых сплавов
Fe
- C
(рис. 7.8) включает
все сплавы (сталь, чугун), имеющие
практическое значение, и может быть
предста-влена в системе железо-углерод
(пунктирные линии) или железо-цементит
(сплош-ные линии).

 Рассмотрим
диаграмму состояния системы железо —
цементит.
Рассмотрим
диаграмму состояния системы железо —
цементит.
Железо
—
металл серебристо-белого цвета, обладающий
очень
высокой пластичностью (относительное
удлинение составляет
около 50%) при невысокой прочности
(180-250) МПа. Температура
плавления железа 1539°С. В твердом
сос-тоянии железо
может находиться в двух модификациях
—
![]() (объемноцентри-рованный
куб) и
(объемноцентри-рованный
куб) и![]() (гранецентрированный куб).
(гранецентрированный куб).
Цементит — это химическое соединение Fe3C (карбид железа). Кристал-лическая решетка цементита очень сложна. Температура плавления цементита око-ло 1250°С. Аллотропических превращений цементит не испытывает, но при низких температурах он слабо магнитен. Он имеет очень высокую твердость, соизмеримую с твердостью алмаза (НВ > 800), при этом его пластичность близка к нулю. Це-ментит — соединение неустойчивое и при высоких температурах распадается с образованием свободного углерода в виде графита.
Помимо основных компонентов в структуре железоуглеродистых сплавов можно обнаружить следующие структурные составляющие:
Феррит (Ф) — твердый раствор внедрения углерода в -железо. Он обла-дает сравнительно невысокой твердостью НВ (65-130), пластичен ( = 40%), си-льно магнитен, хорошо проводит тепло, обладает хорошей электропроводностью.
Растворимость углерода в феррите очень мала и составляет при температуре 727°С всего 0,025%, при комнатной температуре она много ниже и составляет 0,006%.Твердый раствор углерода в -железе носит название -феррит или высокотемпературный феррит.
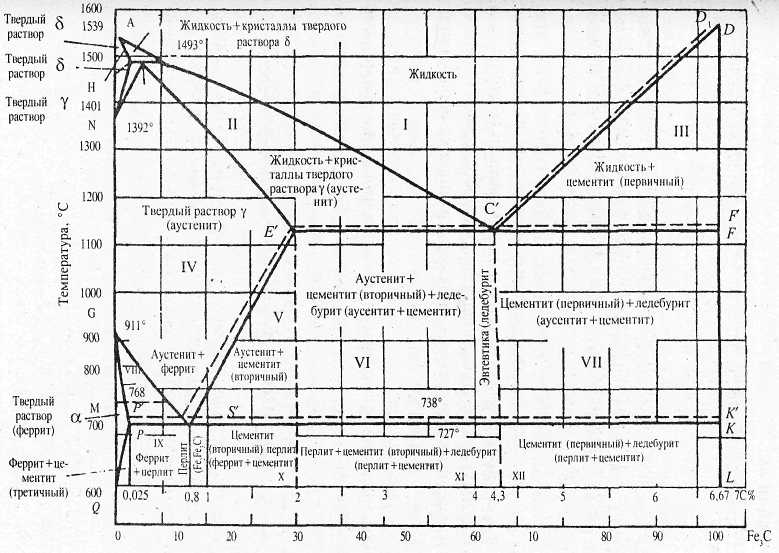

 Рис.
7.8. Диаграмма состояния железоуглеродистых
сталей.
Рис.
7.8. Диаграмма состояния железоуглеродистых
сталей.
Аустенит
(А) —
твердый раствор углерода в
![]() -железе,
имеет решетку
гранецентрированного куба. Аустенит
не магнитен, обладает
относительно невы-сокой твердостью НВ
(170-200). Максимальная растворимость
углерода 2,14% при температуре 1147°С.
При температуре 727°С растворимость
углерода сос-тавляет 0,83 %.
-железе,
имеет решетку
гранецентрированного куба. Аустенит
не магнитен, обладает
относительно невы-сокой твердостью НВ
(170-200). Максимальная растворимость
углерода 2,14% при температуре 1147°С.
При температуре 727°С растворимость
углерода сос-тавляет 0,83 %.
Перлит (П) — механическая смесь, состоящая из очень тонких пластинок или зерен цементита и феррита. Образуется в результате распада аустенита при те-мпературе 727°С. Содержание углерода в перлите 0,83%. Поскольку превраще-ние аустенита в перлит происходит в твердом состоянии, эта смесь называется эвте-ктоид (а не эвтектика, которая образуется при первичной кристаллизации). Элементар-ная кристаллическая ячейка перлита представляет собой композицию двух реше-ток — феррита и цементита, объединенных общими связями, поэтому свойства перлита будут представлять некую величину, лежащую между свойствами феррита и це-ментита. Так, твердость по Бринелю составляет около 250 НВ, относительное уд-линение 5 = 12-15%.
Ледебурит — механическая смесь (эвтектика), образованная цементитом и аустенитом, содержащая 4,3% при температуре 727°С. В интервале темпера-тур от 1147 до 727°С ледебурит состоит из аустенита и цементита, при температуре 727°С аустенит превращается в перлит. Ледебурит характеризуется высокой твердо-стью (НВ = 700 МПа) и, следовательно, высокой прочностью, но в то же время пластичность его близка к нулю.
Точка А на диаграмме показывает температуру плавления чистого железа, точка D — температуру плавления цементита. Процесс кристаллизации распла-ва начинается по линии ABCD (линия ликвидус) и заканчивается на линии AHJ ECF (линия солидус). В температурном интервале кристаллизации существуют одно-временно две фазы — жидкий расплав и кристаллы избыточного компонента по отношению к составу эвтектики.
Ниже линии солидус в затвердевших сплавах при понижении температуры происходят дальнейшие изменения структуры. Это связано с аллотропическими превращениями железа и называется вторичной кристаллизацией. Сплавы с содер-жанием углерода до 2,14% в области IV состоят из одного аустенита. При охла-ждении сплава на линии GS начинается образование феррита, а на линии SE — вторичного цементита. Остающийся при этом аустенит при температуре 727°С полностью распадается на феррит и цементит, образуя при этом механическую смесь эвтектоидного состава (перлит).
Таким образом, сплавы с содержанием углерода до 0,83% называются до-эвтектоидными и состоят при нормальной температуре из феррита и перлита. Спла-вы с содержанием углерода 0,83% называются эвтектоидными и состоят из пер-лита. Если концентрация углерода находится в пределах 0,83% -2,14%, сплав называют заэвтектоидным и его состав — перлит и цементит вторичный.
Рассмотрим превращения в сплавах содержанием углерода более 2,14%. В точке С происходит одновременная кристаллизация аустенита и цементита с образованием сплава эвтектического состава — ледебурита. При содержании углерода (2,14 - 4,3)% сплав называют доэвтектическим, и он состоит из цеме-нтита вторичного, аустенита и ледебурита. При содержании С (4,3 - 6,67) % сплав называется заэвтектическим и состоит из цементита и ледебурита. Сплав с содержанием углерода до 2,14% называется сталь, а больше 2,14% — чугун.
Классификация сталей.
Стали классифицируются по следующим признакам:
I. По химическому составу: 1 — углеродистые; 2 — легированные.
Углеродистые стали подразделяются на низкоуглеродистые с содержа-нием углерода до 0,3%; среднеуглеродистые (0,3-0,65)С% и высокоуглеродис-тые с содержанием углерода от 0,7 до 1,4%.
В соответствии с диаграммой состояния Fe-C, под сталями понимают сплавы с содержанием углерода до 2,14%, однако в практике предельное соде-ржание углерода не превышает 1,4%, в противном случае структура получает-ся очень грубой (крупные иглы цементита), а свойства их нестабильными. Кроме углерода в сталях могут присутствовать различные примеси, такие как кремний, марганец, но их количества невелики и не оказывают сущест-венного влияния на свойства, другие же (сера, фосфор, мышьяк) относятся к вредным примесям и количество их строго регламентируется. Таким образом, свойства углеродистых сталей находятся в прямой зависимости от содержа-ния углерода, и чем оно выше, тем прочнее сталь и ниже ее пластичность.
Легированные стали — стали, в состав которых входят различные эле-менты, придающие сталям требуемые свойства. Сущность процесса легирова-ния заключается во введении в сплав компонентов, которые изменяют структу-ру сплава и, следовательно, придают ему требуемые свойства. В зависимости от количества легирующих компонентов в сплаве различают:
- низколегированные стали — до 5% легирующих компонентов;
- среднелегированные стали — 5-10% легирующих компонентов;
- высоколегированные стали с содержанием легирующих компонентов более 10%.

Принятая система обозначения (маркировки) предполагает следующее: цифра, стоящая на первом месте, указывает количество углерода в сотых до-лях процента (для конструкционных сталей) и десятых (для инструменталь-ных сталей). Буква, стоящая в обозначении, указывает, какой легирующий элемент использован, цифра, стоящая после буквенного значения элемента, показывает его количество в целых процентах. Если после буквенного обоз-начения цифра не указывается, значит, содержание этого элемента находит-ся в пределах 1 %. Если в начале обозначения стали цифра не указывается, то содержание углерода находится в пределах 0,01 % (для конструкционных ста-лей) и 1 % (для инструментальных сталей), а буква А, стоящая в конце бук-венно-цифрового обозначения стали, указывает на пониженное содержание серы и фосфора (до 0,03% каждого). Например: сталь 1Х18Н9Т содержит 0,01% углерода, 18% хрома, 9% никеля и около 1% титана.
II. По назначению — стали подразделяются на конструкционные и инс-трументальные.
Конструкционные стали должны обладать запасом пластичности, так как большинство строительных конструкций работает в области нестатических нагрузок, а в этом случае пластические характеристики должны быть на вы-соком уровне. Поэтому в качестве конструкционных используют низко- и среднеуглеродистые стали с содержанием углерода до 0,65 %. В отличие от конструкционных инструментальные стали должны быть твердыми и проч-ными. В качестве инструментальных сталей, как правило, применяют высо-коуглеродистые или специальные легированные стали.

 III.
По способу производства.
III.
По способу производства.
Основным способом получения стали является передел чугуна, являющегося продуктом доменного производства. В процессе переработки чугуна из него удаля-ют избыток углерода, марганца, кремния и вредные примеси — серу и фосфор.
В настоящее время сталь выплавляют следующими способами:
— конвертерным, мартеновским и электротермическим.
Производство стали в конвертерах (рис. 7.9.) заключается в продувке жи-дкого чугуна воздухом или технически чистым кислородом в специальном уст-ройстве — конвертере. В современном металлургическом производстве дутье осу-ществляется снизу или сверху.
Конвертеры с нижним дутьем представляют собой печь грушевидной фор-мы емкостью 10-60 т чугуна, футерованную изнутри огнеупорным кирпичом либо кислым, либо основным в зависимости от вида процесса (бессемеровский или тома-совский).
Р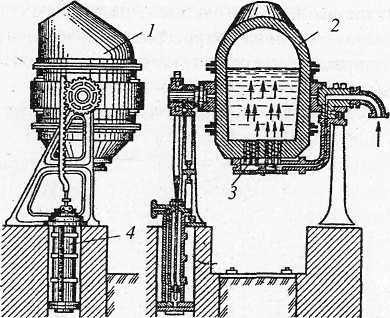 ис.
7.9. Схема конвертера:1 — враща-ющийся
грушевидный сосуд; 2 — фу-теровка; 3
—
фурменные отверстия для подачи воздуха;
4
—
поворотный меха-низм.
ис.
7.9. Схема конвертера:1 — враща-ющийся
грушевидный сосуд; 2 — фу-теровка; 3
—
фурменные отверстия для подачи воздуха;
4
—
поворотный меха-низм.
Продувка снизу осуществляется во-здухом, при этом качество стали оказы-вается невысоким из-за повышенного содержания азота.
Конвертеры с верхним дутьем ис-пользуют для продувки технически чис-тый кислород, при этом возможно испо-льзование дешевых передельных чугу-нов, а также возможно переплавлять до 20-30% стального лома и получать сталь, не уступающую по качеству мартеновской. Емкость кислородных конвертеров достигает 600 тонн.
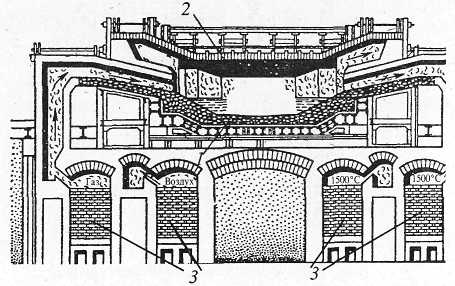
Рис. 7.10. Схема мартеновской печи: 7 — под; 2 — свод; 5 — регенераторы.
В
мартеновской печи (рис. 7.10) выплавляют
сталь заданного
состава из твердого или жидкого чугуна,
стального или чугунного
лома с добавками железной руды, окалины,
флюсов
и ферросплавов, при этом продукты
химических реакций отходят в шлак. Как
и в конвертерах, окисление избыточных
компонентов
расплава протекает при взаимодействии
их с кис лородом
воздуха, а также с составляющими шихты
(рудой и окалиной).
Для ускорения процесса применяют
вдувание чистого
кислорода в расплавленный металл.
Современные мартеновские
печи имеют различную емкость от 1,50 до
300 тонн жидкого металла. В мартеновских
печах выплавляют
как углеродистую, так и легированную
сталь.
лородом
воздуха, а также с составляющими шихты
(рудой и окалиной).
Для ускорения процесса применяют
вдувание чистого
кислорода в расплавленный металл.
Современные мартеновские
печи имеют различную емкость от 1,50 до
300 тонн жидкого металла. В мартеновских
печах выплавляют
как углеродистую, так и легированную
сталь.
Производство стали в электрических печах имеет ряд преимуществ по срав-нению с другими способами производства стали. Это, в частности, более высокая температура расплава (до 2000°С), что позволяет расплавлять металл с высокой концентрацией тугоплавких компонентов (хром, молибден, вольфрам и др.), иметь вы-сокоосновный шлак, что позволяет свести к минимуму содержание вредных приме-сей, создавать восстановительную атмосферу или вакуум, что делает возможным осуществить дегазацию металла и его рафинирование. Для выплавки стали при-меняют печи двух видов — дуговые и индукционные.
Большое распространение в металлургической промышленности получили дуговые электрические печи. Источником тепловой энергии является мощная эле-ктрическая дуга, горящая между специальными угольными электродами.
В индукционных печах нагрев стали осуществляется за счет токов Фуко, гене-рируемых специальным индуктором.
Разливка стали. Готовая сталь сливается из печи в разливочный ковш и с по-мощью мостового крана переносится к месту разливки, где и разливается по изло-жницам. Изложницы представляют собой чугунные или, что реже, стальные фор-мы. Для облегчения выемки слитка их делают конусными. Поперечное сечение из-ложницы зависит от дальнейшего вида обработки слитка и может быть круглым, прямоугольным, квадратным или многоугольным.
В последние годы широко применяется метод непрерывной разливки стали, сущность которого заключается в следующем. Из ковша через промежуточное разливочное устройство жидкая сталь непрерывно поступает в кристаллизатор, охлаждаемый водой. В кристаллизаторе формируется слиток — образуются его поверхности. Наиболее рациональными принято считать сечение от 150x500 до 200x600 мм. Затвердевший слиток вытягивается из кристаллизатора роликами со скоростью 0,5-1,5 м/мин. В начале разливки в кристаллизатор вставляют брус-затравку, на котором начинает кристаллизоваться разливаемая сталь. При этом ме-талл приваривается к затравке и вместе с ней вытягивается роликами.
Существенным недостатком вертикальных установок является их большая высота — 45 м; поэтому в настоящее время широкое применение получили уста-новки радиального типа.
IV. По степени раскисления стали подразделяются на: кипящие — кп; по-луспокойные — пс; спокойные — сп.
Спокойные стали получаются при последовательном раскислении феррома-рганцем, ферросилицием и алюминием. После введения раскислителей реакция раскисления углеродом подавляется и выделение пузырей СО2 прекращается, сталь «успокаивается». Эта сталь наиболее качественная, но и наиболее дорогая.
Полуспокойные стали получаются при раскислении ферромарганцем и уме-ньшенным количеством ферросилиция. По качеству и стоимости она является про-межуточной между спокойной и кипящей сталью.
V. По качеству стали подразделяются на стали обыкновенного качества, качественные и высококачественные.
Качество стали определяется содержанием вредных примесей — серы и фо-сфора. Для сталей обыкновенного качества содержание серы составляет не бо-лее 0,05 %, фосфора — 0,05 %, для сталей качественных допустимое содержа-ние серы — 0,04, фосфора — 0,04, для высококачественных сталей — 0,03% соответственно.
Механизм вредного влияния серы заключается в следующем: в расплаве же-лезо с серой вступают в химическую реакцию с образованием сульфида железа FeS. При кристаллизации сульфид железа с аустенитом образуют механическую смесь. Температура плавления этой механической смеси эвтектического состава составляет 988°С, а это значит, что когда аустенит уже закристаллизовался, эвте-ктика еще находится в жидком состоянии и располагается по границам зерен, и, если в этот момент в металле действуют какие-либо напряжения, то происходит разрушение эвтектики, так как она не обладает достаточной прочностью. Обычно такие разрушения происходят при температуре 900°С и выше и носят название «красноломкость». Это особенно опасно для сварных соединений, так как при свар-ке всегда возникают напряжения из-за неравномерного нагрева.
Механизм вредного влияния фосфора аналогичен, только он является следс-твием эвтектоидных превращений (вторичная кристаллизация) и разрушения могут происходить при температуре 280-300° (синеломкость).
Применение стали в строительстве.
Сталь углеродистая обыкновенного качества. Основное влияние на свойст-ва стали оказывает содержание углерода. С увеличением содержания углерода повышаются, прочность, твердость и износостойкость, но при этом снижаются пластичность и ударная вязкость, а также ухудшается свариваемость. Обозначе-ние марок сталей — буквенно-цифровое. При этом только для сталей обыкновен-ного качества допускается сокращение Ст, что обозначает — сталь.
По ГОСТ 380-71 выпускается семь марок сталей — СтО, Ст1, Ст2,Ст3, Ст4, Ст5, Ст6, где цифры от 0 до 6 — условный номер марки. Степень раскисле-ния обозначают буквами кп, пс, сп. Кипящими выплавляют стали марок СтО—Ст4, спокойными и полуспокойными можно выплавлять стали марок от Ст1 до Ст6. Стали обыкновенного качества подразделяют на 3 группы — А, Б и В. Для сталей по группе А гарантируются механические свойства, для сталей группы Б гарантируется химический состав, для сталей, выпускаемых по группе В, — и механические свойства, и химический состав. Буква А в обозначении, как пра-вило, не указывается, например Ст2кп (сталь марки 2, группа А, кипящая), ВСтЗпс (сталь марки 3, группа В, полуспокойная) и т.д. В обозначении указыва-ется способ производства (М — мартеновский, Б — бессемеровский, К — кис-лородно-конверторный). В группе А индекс М часто опускается, при этом име-ется в виду, что сталь мартеновская, а при отсутствии индексов сп, пс, кп име-ется в виду, что сталь спокойная. Спокойная сталь более качественная, но по стоимости она на 12-15% дороже кипящей. Полуспокойная сталь занимает поло-жение между спокойной и кипящей, и стоимость ее ниже из-за меньшего расхода раскислителей.
Сталь углеродистая качественная. Качественная конструкционная сталь выплавляется в мартеновских и электрических печах (спокойная, полуспокойная и кипящая). В зависимости от химического состава эта сталь делится на две группы: I— с нормальным содержанием марганца и II — с повышенным содержанием марганца. Качественные углеродистые стали поставляют по химическому соста-ву и механическим свойствам. В обозначении слово «сталь» пишут полностью, цифра, обозначающая марку стали, указывает среднее содержание углерода в сотых долях процента. Например, сталь10кп(0,10%С, кипящая), сталь30пс(0,30%С, полуспокойная), сталь 45(0,45%С, спокойная). Для спокойных качественных ста-лей индекс сп может опускаться. Сталь может поставляться в термически обра-ботанном состоянии (отожженная, нормализованная).
Инструментальные качественные стали предназначены для изготовления режущего и мерительного инструмента. Марки этих сталей обозначают буквой У и цифрой, указывающей содержание углерода в десятых долях процента. Например, сталь У7, сталь У9, сталь У12.
Сталь углеродистая высококачественная. Эти стали содержат минималь-ное количество серы и фосфора (до 0,02%), меньшее количество включений и обладают повышенными пластическими характеристиками. Для обозначения высо-кого качества стали в конце буквенно-цифрового обозначения ставят букву А, нап-ример, Сталь 50А, Сталь У ПА и т.д.
Строительные стали.
В связи с тем, что подавляющее большинство элементов строительных конс-трукций соединяют сваркой, основным требованием к строительным сталям явля-ется их хорошая свариваемость, поэтому содержание углерода в них не должно превышать 0,25 %. Более высокое содержание углерода может привести к образова-нию закалочных структур, возникновению внутренних напряжений и даже образо-ванию трещин.
Для изготовления несущих сварных и клепаных конструкций рекомендуют следующие виды сталей: мартеновскую — марок ВМСт3пс (сп, кп ), низколегиро-ванную — марок 15ГС, 14Г2, 10Г2С, 10Г2СД, 15ХСНД, а также кислородно-кон-вертерную марок ВКСт3сп ( пс, кп ). Стали марок Ст4 и Ст5 рекомендуют для несварных конструкций.
Сталь для конструкций, работающих на динамические и вибрационные наг-рузки и предназначенных для эксплуатации в условиях низких температур, должна проверяться на ударную вязкость при отрицательных температурах. К сталям для мостовых конструкций предъявляют специальные требования (ГОСТ 6713-75) по однородности и мелкозернистости, отсутствию внешних дефектов, прочностным и деформационным свойствам.
Для армирования железобетонных конструкций сталь применяют в виде стер-жней, проволоки, сварных сеток, каркасов. Арматурная сталь может быть горяче-катаная (стержневая) и холоднокатаная (проволочная). По форме стержни могут быть круглыми или периодическими (рис. 7.11) для улучшения сцепления с бе-тоном. В ряде случаев для повышения механических свойств (увеличения предела текучести) сталь подвергают деформированию (наклеп) либо термообработке.


Рис. 7.11. Периодический профиль арматурной стали: а — общий вид сте-ржней; б — развернутая поверхность стержня; в — деталь винтового выступа.
Стержневая арматура в зависимостиот механических свойств дели-тся на классы А- I (А-240), А- II (А-300), А- III (А-400), A-IV(A-600), A-V(A-800), A-VI(A-1000). В обозначении класса арматурной стали, например А-240, цифра показывает предел текучести стали. При обозначении класса термиче-ски упрочненной арматурной стали добавляют индекс «т» (например Ат-IV), упрочненную вытяжкой — «в» (например А- IIIв). Арматурная проволока мо-жет быть холоднотянутой — класса B-I (низкоуглеродистая) для ненапрягаемой арматуры и класса В-II (углеродистая) для напрягаемой арматуры. Для обыч-ного армирования преимущественно применяют арматурную сталь классов А- III (марок 25Г2С, 35Г2С и др.), А- II (марки Ст5) и обыкновенную арматур-ную проволоку, а в некоторых случаях также A-I (марки Ст3) и А- IIв. Для пре-дварительно напряженных железобетонных конструкций используют высоко-прочную проволоку, арматурные пряди и арматуру класса A-IV (марок 30ХГ- 2С, 20ХГСТ, 20ХГ2Ц и другие низколегированные стали), а также упрочнен-ную вытяжкой сталь класса А- IIIв (марок 35ГС, 25Г2С). В последнее время широкое применение в строительстве находит арматурная сталь класса А- III (А-500), изготавливаемая из стали Ст3 и прошедшая термомеханическое упро-чнение.
Основы термической обработки металлов.
В целях получения более высоких или специально заданных свойств из-делий из металлов и сплавов их подвергают термической обработке. Смысл ее заключается в изменении структуры путем нагрева изделия до определенной температуры, выдержке при этой температуре в течение определенного време-ни и последующего охлаждения по заданному режиму.
Основными факторами воздействия при термообработке являются:
- температура нагрева — при этой температуре формируется исходная струк-тура, с которой при охлаждении начнутся фазовые превращения;
- время выдержки — время, в течение которого формируется начальная струк-тура во всем объеме изделия. Время выдержки зависит от источника нагрева и толщины изделия;
- скорость охлаждения — определяет формирование конечной структуры.
В последнее время все большее применение получает обработка, в кото-рой объединяются и пластическая деформация, и структурные превращения. В этом случае деформация не только придает изделию внешнюю форму, но и создает наклеп, и термической обработке подвергается наклепанный, т.е. де-формированный, металл. Этот метод носит название термомеханической об-работки.
Отжиг — вид термообработки, имеющий целью улучшение свойств ста-ли, подготовку ее структуры к окончательной термической обработке, прида-ние стали более высоких пластических свойств, снятие внутренних напря-жений и т.д.
Нормализация стали применяется для снятия внутренних напряжений, уменьшения твердости и получения однородной мелкозернистой структуры. Для некоторых сталей (низкоуглеродистые стали) нормализация является окончательной термической обработкой, так как у них получается хорошее сочета-ние пластичности и прочности.
Закалка и отпуск. Назначение закалки и отпуска состоит в придании ме-таллу высокой твердости и прочности при сохранении достаточной вязкости.
Химико-термическая обработка стали. Химико-термической обработкой стали называют термическую обработку, связанную с изменением химического сос-тава, структуры и свойств поверхностного слоя изделия. Цель ее — упрочнение поверхностного слоя с целью повышения твердости, усталостной прочности, из-носоустойчивости и т.д.
Применяются следующие виды химико-термической обработки стали:
Цементация стали — процесс поверхностного науглероживания изделия из низкоуглеродистой стали в углеродосодержащей среде (карбюризаторе) с целью получения твердой поверхности и вязкой середины.
Азотирование — насыщение поверхности стали азотом. Этот процесс обычно осуществляется в среде газообразного аммиака для повышения твердости, прочности, износостойкости и коррозионной стойкости. Детали подвергают азо-тированию после окончательной механической и термической обработки — закал-ки с высоким отпуском.
Цианирование (нитроцементация) — это процесс одновременного насы-щения поверхности стали углеродом и азотом с целью повышения твердости, изно-состойкости и усталостной прочности деталей. Цианирование проводится в распла-вах цианистых солей NaCN или KCN или в смеси метана СН4 и аммиака NH3.
Диффузионная металлизация — это процесс химико-термической обрабо-тки, при котором поверхность стальных деталей насыщается различными элемента-ми: алюминием, кремнием, хромом и др.
Алитирование — насыщение поверхности изделий алюминием. Применя-ется для повышения окалиностойкости и жаростойкости низкоуглеродистых сталей.
Силицирование — насыщение поверхностного слоя кремнием с целью по-вышения окалиностойкости до 800-850°С, а также повышения коррозионной стойкости.
 Хромирование
—
насыщение поверхности изделий хромом
с
целью повы-шения коррозионной стойкости,
износостойкости
и окалиностойкости до темпера-туры
800°С.
Хромирование
—
насыщение поверхности изделий хромом
с
целью повы-шения коррозионной стойкости,
износостойкости
и окалиностойкости до темпера-туры
800°С.
Борироваше — насыщение поверхности бором, имеет целью повысить твердость (до HV1800—2000), сопротивление износу, коррозионную стойкость.
Коррозия металлов и способы защиты.
Коррозия — процесс химического или электрохимического разрушения металлов под действием окружающей среды. Известно, что от коррозии ежегод-но теряется до 10% производимого металла, поэтому борьба с коррозией приобре-тает все возрастающее значение.
В процессе химического разрушения на поверхности металла образуется пле-нка из продуктов окисления (оксидов). В некоторых случаях эта пленка может за-щищать лежащий под ней металл от дальнейшего взаимодействия с окружающей средой. Такие пленки образуются на поверхности алюминия, никеля, свинца и др. При окислении железа в сухом воздухе или в атмосфере сухого кислорода образует-ся также достаточно плотная пленка, однако с ростом толщины она растрескивает-ся и отслаивается от поверхности металла.
Электрохимическая коррозия — наиболее распространенный тип корро-зии. Она происходит чаще всего при воздействии на металл различных электроли-тов. Вода в природе, технике, быту (речная, водопроводная, атмосферные осадки и т.д.) всегда является раствором электролита и вызывает электрохимическую корро-зию. Поэтому различные строительные конструкции, подземные и наземные трубо-проводы и др. подвергаются главным образом электрохимической коррозии.
При соприкосновении металла с электролитом ионы с поверхности металла переходят в электролит. Однако при растворении металла в электролит переходят лишь положительные ионы, в результате электролит заряжается положительно, а сам металл — отрицательно за счет оставшихся на нем электронов.
Металлы обладают различной способностью растворяться в электролитах. Поэтому, если пластинки различных металлов опустить в один электролит, то они будут иметь различные потенциалы, причем чем больше ионов металла перейдет в раствор, тем больше будет отрицательный потенциал этого металла. В таблице приведены значения потенциалов некоторых металлов.
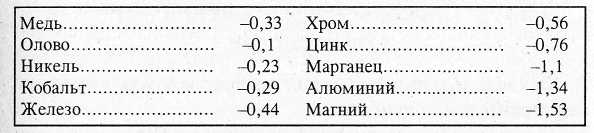
Если соединить электрически различные металлические пластинки, находя-щиеся в электролите, то образуется гальваническая пара, где анодом будет металл с более низким электродным потенциалом, а катодом — с более высоким. В гальванической паре переход ионов в электролит продолжается до полного растворения пластинки анода. Отсюда можно сделать вывод, что чистые металлы и однофаз-ные сплавы должны иметь большую коррозионную стойкость, чем многофазные сплавы. Слой электролита при коррозии может быть весьма незначительным — достаточно небольшой конденсации влаги на поверхности из воздуха, как начина-ется процесс коррозии.
Наличие
сплошной окисной пленки на поверхности
металла предохраняет
его от электрохимической коррозии, так
как изолирует
металл от контакта с электро-литом.
Поэтому такие
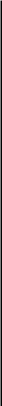
 металлы,
как алюминий, хром, имеющие весьма низкие
эле-ктрохимические потенциалы,
обладают высокой коррозионной стойкостью.
металлы,
как алюминий, хром, имеющие весьма низкие
эле-ктрохимические потенциалы,
обладают высокой коррозионной стойкостью.
Мерой коррозионной стойкости металлов является скорость коррозии в данной среде, которую обычно выражают весом металла (в граммах), превращенного в про-дукты коррозии за единицу времени (1 час), относительно единицы поверхности (1 м2). На скорость коррозии влияют состав металла, механическая и термичес-кая обработка, а также среда (воздух, растворы кислот, вода и т. д.), температура, давление и характер нагрузки.
Применяются следующие способы защиты конструкций от коррозии:
- металлические покрытия бывают двух типов — анодные и катодные. Для ано-дного покрытия используют металлы, обладающие более отрицательным электро-дным потенциалом, чем защищаемый металл (например, цинк, хром). Для катодно-го покрытия выбирают металл, имеющий меньшее отрицательное значение элект-родного потенциала, чем основной металл (медь, олово, никель и др.). Примером анодного покрытия является цинкование, катодного — никелирование.
- химические покрытия заключается в том, что на поверхности изделия искусственно создают защитные неметаллические пленки, чаще всего окисные за счет окисления поверхностного слоя металла. Этот процесс носит название оксидирования.
- фосфатирование - на стальных изделиях создают пленки фосфорнокислых солей железа и марганца.
- неметаллические покрытия производят красками, лаками, эмалями, а также ре-зиной или эбонитом. Это наиболее распространенный способ защиты металличес-ких строительных конструкций от коррозии, что объясняется надежностью данного способа защиты от коррозии в атмосферных условиях и простотой нанесения пок-рытия. При временной защите металлических изделий от коррозии используются невысыхающие масла (технический вазелин, лак этиноль и др.).
Сварка.
Практическое применение электрической дуги для сварки металлов было осуществлено в 1882 г. русским инженером Н.Н. Бенардосом. Помимо этого способа Н.Н. Бенардос разработал основы электрической контактной сварки, сварки в струе газа, а также положил начало разработке автоматов для дуго-вой сварки. В 1888 г. русский инженер Н.Г. Славянов предложил способ свар-ки металлическим электродом, который широко применяется в настоящее время. Он же применил на практике дуговую сварку под слоем насыпного флюса. Большое развитие и широкое промышленное применение сварка по-лучила в 20-е гг. прошлого столетия. Одновременно с совершенствованием ручной дуговой сварки велись работы по разработке механизированных способов сварки. Так, в середине прошлого века были разработаны высокопро-изводительные способы сварки под слоем флюса, электрошлаковой сварки, сварки в среде защитных газов и другие.
Физическая сущность образования сварного соединения — это техноло-гический процесс получения неразъемных соединений за счет расплавления кромок соединяемых элементов в месте их контакта или местного пластичес-кого деформирования металла сопрягаемых поверхностей. Нетрудно предс-тавить, что образование сварного соединения — это процесс установления межатомных связей между атомами кристаллических решеток взаимодейст-вующих систем.
Процесс образования сварного соединения протекает в две стадии:
I — образование физического контакта;
II — химическое взаимодействие или электронный обмен с образова-нием одного из видов сплава (твердый раствор, механическая смесь или химичес-кое соединение).
В зависимости от вида подводимой энергии физический контакт может быть образован или в твердом, или в жидком состоянии. В твердом состоянии физичес-кий контакт образуется за счет механического воздействия, т.е. за счет сжатия двух (или нескольких) элементов.
Классификация способов сварки.
Согласно ГОСТ 19521-74 сварка металлов классифицируется по физичес-ким, техническим и технологическим признакам. В зависимости от энергии, ис-пользуемой для образования сварного соединения, различают три класса сварки: 1) термический — к которому относится сварка, осуществляемая за счет плав-ления при использовании тепловой энергии; 2) термомеханический — сварка с применением тепловой энергии и давления; 3) механический — сварка, исполь-зующая механическую энергию и давление.
В промышленном строительстве используются следующие виды сварки:
а) дуговая открытой дугой, дуговая под флюсом и в защитном газе, электро-шлаковая, газовая — термический класс. По степени механизации дуговая сварка бывает ручной, полуавтоматической или автоматической.
б) Контактная, газопрессовая — термомеханический класс. Существуют следующие виды контактной сварки: стыковая, точечная, шовная (роликовая), газопрессовая,
в) Сварка трением, холодная сварка, ультразвуковая сварка ― механический класс.
Виды сварных соединений и швов
При изготовлении сварных изделий выполняют следующие виды сварных соединений — стыковые (рис. 7.12, а), стыковые с отбортовкой (рис. 7.12, б), нахлесточные (рис. 7.12, в), угловые (рис. 7.12, г), тавровые (рис. 7.12, д), про-резные (рис. 7.12, е), торцовые (рис. 7.12, ж), электрозаклепочные (рис. 7.12, з). Применение того или иного вида соединения зависит от характера конструкции, способа сварки, толщины металла и др. Например, в сосудах, работающих под дав-лением, в трубопроводах применяют, как правило, стыковые швы, в фермах и стой-ках нахлесточные, в сварных балках — тавровые, для тонкого металла применя-ют стыковые швы с отбортовкой и т.д.
Р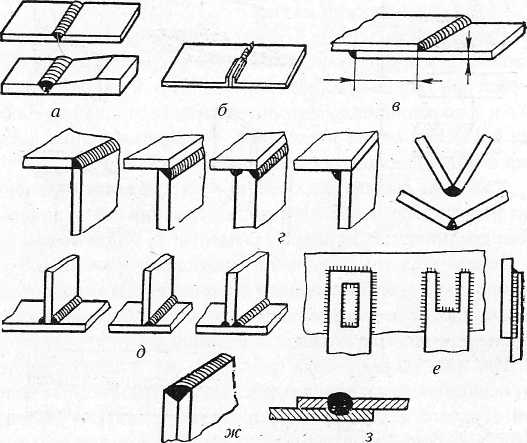 ис.
7.12. Виды сварных соединений:
ис.
7.12. Виды сварных соединений:
а — стыковые; б — стыковой с отбор-товкой; в — нахлесточный;г — угло-вые; д — тавровые; е — прорезные; ж — торцовый; з — электрозаклепоч-ный.
Сварные швы разделяют по сле-дующим признакам:
По расположению относительно направления нагрузки (рис. 7.13,а) — фланговые 1, лобовые 2, комбиниро-ванные 3, косые 4.
По положению в пространстве (рис. 7.13, б) — нижние 1, горизонта-льные 2, вертикальные 3, потолочные 4.
 По
форме наружной поверхности (рис. 7.13, в)
— нормальные (плоские) 1,
выпуклые
(усиленные) 2, вогнутые (ослабленные)
3.
По
форме наружной поверхности (рис. 7.13, в)
— нормальные (плоские) 1,
выпуклые
(усиленные) 2, вогнутые (ослабленные)
3.
По ширине шва (рис. 7.13, г) — ниточные 1 и уширенные 2. Ширина ниточного шва составляет 0,8−1,5dэл, ширина уширенного шва — не более 30 мм.
Рис. 5.40. Классификация свар-ных швов: а — по расположению от-носительно направления нагрузки; б — по расположению в пространст-ве; в — по форме наружной поверх-ности; г — по ширине; д — по коли-честву слоев (проходов); е — по про-тяженности.
По количеству слоев или про-ходов (рис. 7.13, д) — однослойные (однопроходные) 1 и многослойные (многопроходные) 2.
По протяженности (рис. 7.13, е) — сплошные 1 и прерывистые (це-пные и шахматные) 2.
По назначению — прочные, плотные и прочно – плотные.
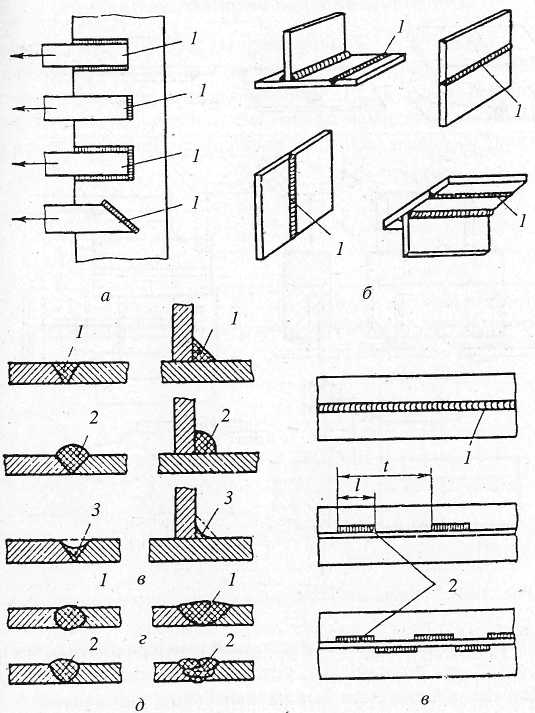
 Обозначение
швов сварных соединений.
По
ГОСТ 2.312-72 швы сварных соединений на
чертежах обозначаются
сплошной (видимые) и штриховой (невиди-мые)
линиями
(рис. 7.14 а),
одинокая
сварная точка обозначается знаком +,
не-видимые одиночные точки не обозначаются.
От линии,
обозначающей шов, про-
Обозначение
швов сварных соединений.
По
ГОСТ 2.312-72 швы сварных соединений на
чертежах обозначаются
сплошной (видимые) и штриховой (невиди-мые)
линиями
(рис. 7.14 а),
одинокая
сварная точка обозначается знаком +,
не-видимые одиночные точки не обозначаются.
От линии,
обозначающей шов, про- водится
линия-выноска с односто-ронней
стрелкой. От наклонной вы-носки проводится
горизонтальная
линия-полка; условное обозначение шва
наносится над полкой, если шов видимый,
или под полкой, если не-видимый
(рис. 7.14, б).
В
попереч-ном сечении соединения границы
шва изображаются сплошными ос-новными
линиями,
а границы сое-диняемых кромок — сплошными
тонкими линиями (рис. 7.14, в).
водится
линия-выноска с односто-ронней
стрелкой. От наклонной вы-носки проводится
горизонтальная
линия-полка; условное обозначение шва
наносится над полкой, если шов видимый,
или под полкой, если не-видимый
(рис. 7.14, б).
В
попереч-ном сечении соединения границы
шва изображаются сплошными ос-новными
линиями,
а границы сое-диняемых кромок — сплошными
тонкими линиями (рис. 7.14, в).
Рис. 7.14. Вспомогательные знаки для обозначения швов.
