
- •Шановні студенти та курсанти!
- •«Роль спадковості в патології людини»
- •«Клініко-генеалогічний аналіз»
- •Класифікація вроджених вад розвитку
- •«Семіотика спадкових захворювань. Особливості проявів спадкових хвороб. Морфогенетичні варіанти розвитку»
- •Спадкові нефритоподібні захворювання
- •Гематуричний нефрит
- •Синдром Шаффера (сімейна гіперпролінемія)
- •Нефронофтіз Фанконі (сімейний ювенільний нефронофтіз)
- •Тубулопатії
- •Ниркова глюкозурія
- •Фосфат-діабет (вітамін d-резистентний рахіт)
- •"Спадкові захворювання нирок”
- •Ахондрогенез.
- •Танатоформна дисплазія.
- •Асфіксична дистрофія грудної клітини (синдром Жена).
- •Діастрофічна дисплазія
- •Гетерозіготна ахондроплазія.
- •Недосконалий остеогенез
- •Гіпофосфатазія
- •Алгоритм обстеження хворих при патології сполучної тканини
- •Лікування
- •Прояв дефіциту незамінних амінокислот
- •Лабораторні дослідження при підозрі на схо
- •Синдром Патау (синдром трисомії 13)
- •Синдром Едвардса (синдром трисомії 18)
- •Синдром трисомії 22
- •Синдром Дауна (синдром трисомії 21)
- •Синдром Шерешевсьеого-Тернера (синдром моносомії х)
- •«Хромосомні хвороби»
- •Класифікація мітохондріальних захворювань
- •Синдром merrf (міоклонус епілепсія, “рвані червоні волокна”)
- •Синдром melas
- •Синдром Кернса-Сейра
- •Синдром Пірсона
- •Синдром mngіе (мітохондріальна нейро-шлунково-кишкова енцефалопатія)
- •Підгостра некротизуюча енцефаломієлопатія Лея
- •Принципи терапії мітохондріальних хвороб:
- •"Мітохондріальні захворювання"
- •Мультифакторіальні хвороби з полігенною спадковою схильністю
- •Факторів
- •Механізми розвитку хвороб зі спадковою схильністю
- •Ішемічна хвороба серця
- •Гіпертонічна хвороба
- •Тромбофілія
- •Цукровий діабет
- •Хронічний панкреатит
- •Бронхіальна астма
- •Епілепсія
- •Шизофренія
- •«Загальна характеристика мультифакторіальних хвороб. Генетична схильність. Заходи профілактики»
- •Профілактика патології зі спадковою схильністю, що базується на визначенні генів схильності
- •Приклади екогенетичних патологічних реакцій
- •Екогенетичні реакції на продукти харчування
- •Фармакогенетика
- •Приклади фармакогенетичних реакцій
- •«Основи екологічної генетики, фармакогенетики»
- •Фактори ризику, що впливають на характер репродуктивних процесів родини
- •Фактори індукованого мутагенезу
- •Показаннями для медико-генетичного консультування є:
- •Функції лікаря-генетика
- •Показання до проведення преконцепційної та пренатальної медико-генетичної консультації
- •Показання до проведення медико-генетичного консультування в ранньому дитинстві та дитинстві
- •Генетик (1-а зустріч)
- •Генетик (2-а зустріч)
- •Показання до преконцепційного лікування та профілактики
- •Преконцепційне лікування Об’єм медикаментозної терапії для преконцепційної профілактики подружжя
- •Пренатальна діагностика
- •Генетик (3-я зустріч)
- •Програма обстеження родини при плануванні вагітності
- •"Медико-генетичне консультування (мгк)"
- •Генетичний скринінг немовлят
- •"Скринуючі програми''
- •Учбово-методична література, рекомендована при вивченні курсу „медична генетика”
- •Медична генетика (самостійна підготовка студентів)
Епілепсія
При більшості форм епілепсії характерна полігенна спадкова схильність, а виникнення захворювання є результатом взаємодії генетичних і середовищних факторів. У розвитку епілепсії встановлено роль генів іонних каналів (калієвих, натрієвих, кальцієвих, хлорних), які мають відношення до механізмів поляризації мембрани нейронів, і генів нейротрансмітерних рецепторів.
Мутація генів калієвих каналів призводять до доброякісних сімейних неонатальних судом; ризик розвитку генералізованої епілепсії згодом дорівнює 16 %. З мутацією генів натрієвих каналів пов'язаний розвиток генералізованої епілепсії з фебрильними судомами.
Ідентифікація генетичного дефекту важлива з клінічної точки зору, оскільки механізм дії багатьох антиконвульсантів базується на модуляції функції іонних каналів. Так, протисудомний ефект карбамазепіну і фентіоніну пов'язаний з потенціюванням інактивації натрієвих каналів.
Шизофренія
Шизофренія, ймовірно, є групою захворювань з різними генетичними дефектами і загальної симптоматологією. Визначено кілька головних генів-кандидатів.
Ген катехол-О-метилтрансферази (СОМТ) бере участь в деградації катехоламінів, включаючи допамін. СОМТ є головним ферментом деградації допаміну в префронтальній ділянці кори. Описано генетичний поліморфізм СОМТ, пов'язаний з присутністю валіну або метіоніну в 108 положенні (коротка форма СОМТ) або в 158 положенні (довга форма СОМТ). Вал-СОМТ алель у хворих на шизофренію зустрічається достовірно частіше.
Другий ген-кандидат — ген серотонінового рецептора 5-НТ2А (13q32). Відмічено зв'язок між шизофренією і поліморфізмом гена Т102С.
Третій ген-кандидат DISС-1, був виявлений у шотландській сім'ї з високою частотою психічних захворювань і збалансованою транслокацією, що веде до розриву цього гена. Участь гена DISС-1, в розвитку шизофренії підтвердилася і в дослідженнях фінських сімей. Білковий продукт гена поки не охарактеризований, так часмо, як і механізм його внеску у розвиток шизофренії.
Дослідження останніх років показали, що середовищними факторами сприяння розвитку шизофренії можуть бути пологова травма і неонатальні вірусні інфекції. Так, в спинномозковій рідині у 29 % хворих на шизофренію було виявлено нуклеотидні послідовності, гомологічні ретровірусним генам. Непрямим доказом ролі вірусних інфекцій служить велика частота хворих на шизофренію серед народжених взимку.
Граф логічної структури теми:
«Загальна характеристика мультифакторіальних хвороб. Генетична схильність. Заходи профілактики»
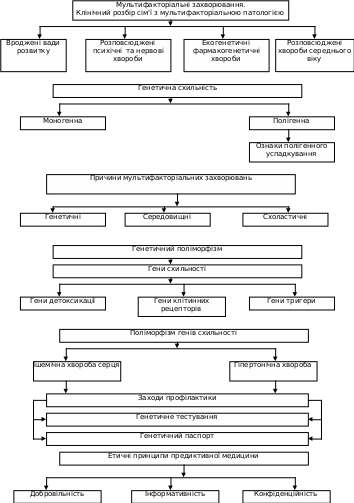
Профілактика патології зі спадковою схильністю, що базується на визначенні генів схильності
Гени та поліморфізми |
Ланка патогенезу |
Захворювання |
Аполіпопротеїну Е (Cys 112 Arg, Arg 158 Cys) |
Порушення ліпідного обміну |
ІХС |
Параоксонази (Gln 192 Arg) |
||
Аполіпопротеїну С III (C/G, позиція 5163) |
|
|
Аполіпопротеїну (a) (C/T, позиція +93) |
|
|
Протромбіну (G/A, позиція 20210) |
Порушення в системі коагуляції і фібрінолізу |
|
V фактора системи згортання крові (Arg506Gln) VII фактора системи згортання крові (Arg353Glu) |
|
|
VII фактора системи згортання крові (I/D промотор, позиція – 323) |
|
|
ІАПГ – 1 (4G/5G промотор, позиція - 675) |
|
|
МТГФР (С/Т, позиція 677) Метілентетрагідрофолатредуктаза |
Дефект обмін метіоніну |
|
АПФ (I/D інтрон 16) |
Активація системи ренін – ангіотензин - альдостерон |
|
АПФ (I/D інтрон 16) |
Активація системи ренін – ангіотензин - альдостерон |
Гіпертонічна хвороба |
Ангіотензіногену (Met235Thr) |
|
|
Аполіпопротеїну Е (Cys 112 Arg, Arg 158 Cys) |
Формування β-амілоїда |
Хвороба Альцгеймера |
АПФ (I/D, інтрон 16) |
Інсулінорезистентність |
Цукровий діабет типу 2 |
ІАПГ – 1 (4G/5G промотор, позиція – 675) |
|
|
Алгоритм профілактичних заходів при ІХС
Прогностично несприятливі поліморфізми генів |
Ланки патогенезу і синдроми |
Профілактика |
||
1-а група |
2-а група |
3-а група |
||
Аполіпопротеїнів (а) Е, С III, параоксонази |
Дісліпідемія, атеросклероз |
Дослідження ліпідного спектру крові |
||
дієта при нормальному і пограничному вмісті ліпідів крові; спостереження в динаміці |
дієта при нормальному і пограничному вмісті ліпідів крові; корекція факторів ризику |
при високому вмісті ліпідів – гіполіпідемічна терапія |
||
МТГФР |
Дисфункція ендотелію, розвиток раннього атеросклерозу, рецидивуючі тромбози коронарних, церебральних і периферичних артерій, венозні тромбози |
Дослідження вмісту рівня гомоцистеіну плазми. У разі підвищення – спостереження фахівця, до компетенції якого відноситься лікування перерахованої патології |
||
при нормальному вмісті – зміна способу життя, у разі підвищення – див. рекомендації для 2-ї і 3-ї груп |
при вмісті 12 мкмоль/л – вживання в їжу продуктів, багатих фолієвою кислотою і вітамінами групи В, при високому рівні 30 мкмоль/л – препарати фолієвої кислоти і вітаміну В12, ангіопротектори або препарати, що володіють властивостями ангіопротекторів |
|||
ІАПГ – 1, протромбіна, факторів V, VII, аполіпопротеіну III |
Активація системи згортання крові, тромбоемболії, у тому числі при варикозній хворобі |
Коагулограма При незмінних показниках |
||
Спостереження в динаміці |
дезагреганти (аспірин) |
|||
При виявленні гіперкоагуляції і гальмування процесу фібрінолізу |
||||
при невиражених змінах – спостереження і обстеження в динаміці |
спостереження і обстеження в динаміці, можливо призначення аспірину |
антиагреганти (аспірин, тиклопидин), пероральні і ін'єкційні форми прямих антикоагулянтів |
||
АПФ, ангіотензиногена, ІАПГ - 1 |
Стимуляція проліферації кардіоміоцитів і клітин гладкої мускулатури судин, стимуляція симпатико-адреналової системи, ГЛЖ, АГ, інсулінорезистентність, ожиріння |
Контроль АД, добове моніторування АД і ЕКГ, дослідження ехокардіографії, визначення рівня цукру в крові, тест на толерантність до глюкози |
||
дієта, зміна способу життя |
оцінка і корекція головних компонентів ризику; за наявності дисфункції лівого шлуночка, АГ і/або діабету – інгібітори АПФ |
інгібітори АПФ або блокатори рецепторів ангіотензину II |
||
Примітка: 1-а група – індивіди, носії генів схильності, що не мають клінічних ознак хвороби.
2-а група - індивіди, носії генів схильності, що мають клінічні ознаки хвороби.
3-а група – хворі індивіди, носії генів схильності з наявністю додаткових факторів ризику (гіпертонічна хвороба, цукровий діабет, ожиріння та ін.
Тема: Основи екологічної генетики,
фармакогенетики
Основні питання:
1. Екогенетика. Екогенетичні хвороби.
Етіологія і патогенез. Класифікація.
Нозологічні форми з різними провокуючими факторами
(лікарські засоби, їжа, клімат).
Професійні хвороби, як екогенетичні у разі малих доз.
Оцінка професійної придатності з екогенетичної точки
зору.
Спадкові фактори схильності до інфекційних захворювань.
Спадковообумовлені патологічні реакції на різні лікарські засоби.
Екогенетика — розділ генетики, що вивчає вплив факторів середовища мешкання на спадковість. Будь-який організм розвивається і існує в тісній взаємодії з навколишнім середовищем. Реакція людського організму на різні агенти навколишнього середовища є предметом екогенетики. Концепція екогенетики вперше була запропонована Брюером в 1971 р.
Екогенетика вивчає 2 типи ефектів:
1) зміну прояву дії визначених алелей при впливі на організм специфічних факторів — екогенетичні синдроми;
2) зміну генетичного матеріалу під дією факторів зовнішнього середовища (індукований мутагенез).
Впродовж еволюції середовище мешкання людини поступово змінювалося. До цих змін організм пристосовувався за рахунок широкої норми реакції, з одного боку, і зміни генотипів в результаті мутацій і подальшого відбору, з іншого боку. В процесі еволюції виникла відносна відповідність умов середовища і видових характеристик людини.
У популяціях під впливом відбору сформувався широкий спадковий поліморфізм генів, що забезпечують взаємодію з середовищем. Не менше 25 % генів, що детермінують антигени, ферменти, рецептори, представлено поліморфними системами, які мають більш ніж 2 алелі. Багато які з них розповсюдились у певних популяціях через якусь селективну перевагу, інші — в результаті дрейфу генів. Частина з них не виявляється фенотипічно.
Сучасний період характеризується великим темпом і інтенсивністю зміни середовища мешкання. У навколишнє середовище надходить величезна кількість хімічних речовин, які входять до складу продуктів (смакові добавки, консерванти, барвники та ін.), предметів побутової хімії, є відходами виробництва. З багатьма з них людина в процесі еволюції не зустрічалася. У зв'язку з появою нових факторів середовища гени, які були такими, що «мовчать», у колишніх умовах, починають виявлятися фенотіпічно в нових умовах і піддаються дії природного відбору.
У деяких випадках ці реакції можуть бути патологічними і обумовлюють так звані екогенетичні хвороби.
Екогенетичними патологічними реакціями, або екогенетичними хворобами називаються генетично обумовлені патологічні реакції на фактори навколишнього середовища. Потенційно токсичні фактори навколишнього середовища діють не на все населення, а тільки на його частину, генетично схильну до такої дії.
Приклади екогенетичних патологічних реакцій
Фактори зовнішнього середовища |
Генетична схильність |
Захворювання |
УФ-промені |
Дефекти ферментів репарації ДНК |
Рак шкіри |
Пил |
Дефіцит антитрипсину |
Емфізема легенів |
Харчові агенти |
|
|
Кінські боби |
Дефіцит Г6ФДГ |
Фавізм |
Сіль |
Дефект К-Nа насоса |
Гіпертонія |
Молоко |
Дефіцит лактази |
Непереносність лактози |
Жири |
Гіперхолестеринемія |
Атеросклероз |
Шоколад |
Зниження активності моно- |
Мігрень |
|
аміноксидази |
|
Алкоголь |
Атипова алкогольдегідро-геназа |
Алкоголізм |
