- •Лекция №27 Патология печени
- •Печеночная недостаточность (пн) – синдром, характеризующийся снижением одной, нескольких или всех функций печени ниже уровня, необходимого для обеспечения нормальной жизнедеятельности организма.
- •Причины печеночной недостаточности
- •Патогенез печеночной недостаточности
- •Метаболизм билирубина
- •Желтухи
- •Метаболизм лекарств в печени
- •Фазы метаболизма лекарственных препаратов в печени
- •Желчегонные препараты
- •Геморрагический синдром при пн обусловлен следующими факторами:
- •Анемический синдром при пн обусловлен следующими факторами:
- •Общая этиология заболеваний печени
- •Основные заболевания печени
- •Опухоли печени
- •Синдром холестаза
- •Синдром цитолиза (повреждения гепатоцитов)
-
Лекция №27 Патология печени
Печеночная недостаточность. Нарушения обмена веществ (белкового, углеводного, липидного, водно-солевого) при патологии печени. Патогенез портальной гипертензии и асцита. Понятие о гепатопротекторах.
Печеночная недостаточность (пн) – синдром, характеризующийся снижением одной, нескольких или всех функций печени ниже уровня, необходимого для обеспечения нормальной жизнедеятельности организма.
ПН делится на виды по следующим признакам:
По числу нарушенных функций:
парциальная;
тотальная.
По течению:
острая;
хроническая.
По исходу:
летальная;
нелетальная.
Причины печеночной недостаточности
Патологические процессы, локализующиеся в печени и желчевыводящих путях:
гепатиты: вирусные, бактериальные, токсогенные;
дистрофии (гепатозы);
циррозы;
опухоли печени;
паразитарные поражения ее;
генетические дефекты гепатоцитов;
камни, опухоли, воспаления желчевыводящих путей с выраженным холестазом.
Внепеченочные патологические процессы:
шок, в том числе послеоперационный;
сердечная недостаточность;
общая гипоксия;
почечная недостаточность;
белковое голодание;
гипоавитаминоз Е;
дефицит селена;
эндокринопатии, в частности острая недостаточность надпочечников.
Патогенез печеночной недостаточности
Действие этиологического фактора изменение молекулярной архитектоники мембран гепатоцитов усиление свободнорадикального и перекисного окисления липидов частичная или полная деструкция мембран + повышение их проницаемости выход из лизосом их гидролаз, что потенцирует повреждение мембран клеток освобождение поврежденными макрофагами фактора некроза опухоли и интерлейкина-1, способствующих развитию воспалительной и иммунной реакции в печени образование аутоантител и аутосенсибилизированных Т-киллеров, вызывающих дополнительное аутоаллергическое повреждение гепатоцитов.
Нарушение участия печени в углеводном обмене заключается в:
гипогликемия натощак из-за снижения способности гепатоцитов расщеплять гликоген до глюкозы и снижения активности инсулиназы;
гипергликемия после приема пищи из-за снижения способности гепатоцитов превращать глюкозу в гликоген.
Это обусловливает характерный признак печеночной недостаточности (ПН) - неустойчивый уровень глюкозы крови.
Нарушение участия печени в липидном обмене характеризуется снижением способности гепатоцитов:
превращать более атерогенную форму холестерина (свободный холестерин) в менее атерогенный эстерифицированный холестерин;
образовывать липопротеиды, обладающие антиатерогенным действием (ЛПВП (-липопротеипды)).
образование холестериновых и пигментных камней: черные – билирубинат кальция, коричневые – билирубинат кальция + жирные кислоты (холевая, дезоксихолевая, таурохолевая).
Первые два изменения ведут к увеличению в крови уровня свободного холестерина и к снижению антиатерогенных фосфолипидов, что способствует отложению холестерина в стенках сосудов и развитию атеросклероза.
Нарушение участия печени в белковом обмене включает:
снижение синтеза гепатоцитами альбуминов гипоальбуминемия и гипоонкия крови, что на стадии развития портальной гипертензии способствует развитию асцита;
диспротеинемия - снижение количества альбуминов и увеличение содержания в плазме глобулинов.
уменьшение биосинтеза ферментов и белков - прокоагулянтов (протромбина, проакцелерина, проконвертина) развитие коагулопатий (этому способствует также уменьшение всасывания в кишечнике жирорастворимого витамина К, поскольку ПН сочетается с нарушением желчеобразовательной и желчевыделительной функции печени);
снижение активности процесса дезаминирования аминокислот и синтеза мочевины из аминогрупп и аммиака в орнитиновом цикле, что ведет к снижению в крови содержания мочевины. Дефицит -кетоглутаровой к-ты снижение окисления и образования АТФ.
Нарушение биосинтеза гепатоцитами ферментов заключается в уменьшении секреции гепатоцитами в кровь образуемых ими ферментов (холинэстеразы, инсулиназы и др.). Кроме того, повреждение гепатоцитов сопровождается увеличением выхода из них в кровь внутриклеточных ферментов: аланин-трансаминазы и глютамат-трансаминазы.
Расстройство обмена витаминов состоит в:
снижении всасывания в кишечнике жирорастворимых витаминов A, D, Е, К;
уменьшении способности гепатоцитов превращать провитамины в активные витамины (например, каротин в витамин А);
торможении процесса образования из витаминов коферментов (например, из пантотеновой кислоты - ацетил коэнзим А, из витамина B1 - кокарбоксилазы пирувата).
Портальная гипертензия – синдром, сопровождающийся повышением давления в бассейне воротной вены, связанный с наличием препятствия оттоку крови (блок).
В зависимости от локализации блока выделяют следующие формы портальной гипертензии:
Постгепатическая (надпеченочная) связана с препятствием во внеорганных отделах печеночных вен или в нижней полой вене проксимальнее места впадения в нее печеночной вены (синдром Бада-Киари, врожденное мембранозное заращение нижней полой вены, первичные сосудистые опухоли (лейомиома и др.), повышение давление в нижней полой вене при правожелудочковой сердечной недостаточности).
Внутрипеченочная связана с блоком в самой печени:
постсинусоидальный блок (циррозы печени, хронический алкогольный гепатит, веноокклюзионная болезнь и т.д.);
парасинусоидальный блок (хронический гепатит, массивная жировая инфильтрация печени);
пресинусоидальный блок (гепатоцеребральная дистрофия, первичный билиарный цирроз, метостазы печени и др.);
Прегепатическая (подпеченочную) связана с препятствием в стволе воротной вены или ее крупных ветвей (тромбоз воротной вены, сдавление воротной вены опухолью и т.д.).
Основным патогенетическим фактором синдрома портальной гипертензии является механическое препятствие оттоку крови.
Наиболее характерное следствие портальной гипертензии - образование коллатералей между бассейном воротной вены и системным кровотоком.
При прегепатической портальной гипертензии развиваются портальные анастомозы, восстанавливающие ток крови из отделов портальной системы, расположенных ниже блока, во внутрипеченочные ветви портальной системы.
При внутри- и надпеченочной портальной гипертензии анастомозы обеспечивают отток крови из системы воротной вены в обход печени в бассейн верхней или нижней полой вены.
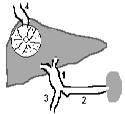
Схема венозной системы печени
|
На рисунке представлена схема венозной системы печени: 1 - v.portae, 2 - v.lienalis, 3 - v.mesenterica superior, 4 - v.v.hepaticae. |
Она складывается из приводящих и отводящих вен. Приводящие вены - это система воротной вены, которая формируется из двух стволов - селезеночной и верхней брыжеечной вены.
Войдя в ворота печени вместе с ветвями печеночной артерии, венозные разветвления воротной вены образуют капиллярную сеть, которая несет смешанную артериальную и венозную кровь. В синусоидах кровь контактирует с гепатоцитами. Отводящими коллекторами являются печеночные вены, которые впадают в нижнюю полую вену.
Нарастающее гидростатическое давление в портальной системе наряду с повышенным притоком через печеночную артерию постепенно приводит к повышению давления в основном стволе воротной вены примерно. Пока это происходит, развивается интенсивная коллатеральная циркуляция, которая на первых порах компенсирует повышение давления в системе воротной вены. Эти коллатеральные анастомозы существую и в норме, но они не приспособлены к такому повышению кровотока, венозные стволы варикозно расширяются.
Особенно опасны коллатерали в области пищевода, поскольку могут развиваться тяжелые кровотечения. Расширяются также коллатеральные анастомозы в области передней брюшной стенки, а также в области прямой кишки.
Шунтирование крови в обход печеночной паренхимы по сути означает частичное функциональное отключение печени, последствия которого для организма весьма многообразны. К важнейшим из них относятся:
Бактериемия - результат выключения РЭС печени, что обусловливает повышенный риск "метастатической" инфекции.
Эндотоксемия.
Гиперантигенемия - перегрузка антигенным материалом кишечного происхождения иммунной системы организма.
С повышением давления в воротной вене связано образование асцита. Чаще он встречается при постгепатической и внутригепатической портальной гипертензии.
Асцит - водянка (скопление внеклеточной жидкости) брюшной полости.
Заболевания, которые проявляются исключительно или преимущественно асцитом:
Болезни печени и ее сосудов: циррозы, рак, болезнь Бадда-Киари, веноокклюзионная болезнь.
Болезни брюшины: туберкулезный перитонит, перитониты другой этиологии.
Болезни сердца: констриктивный перикардит, застойная сердечная недостаточность.
Другие болезни: опухоли и кисты яичников (синдром Мейгса), кисты поджелудочной железы, болезнь Уиппла, саркоидоз, микседема.
Факторы, способствующие образованию асцита
Портальная гипертензия.
Повышение лимфопродукции в печени, связанное с блокадой оттока венозной крови из печени.
Падение онкотического давления плазмы, связанное, в первую очередь, со снижением синтеза альбуминов печенью.
Нарушение функции почек, связанное с нарушением оттока крови из почек.
Изменение гормонального обмена - вторичный альдостеронизм ( разрушения, инактивации альдостерона в гепатоцитах).
Порочный круг: скопление жидкости в брюшной полости (асцит) ОЦК ишемия почек активация РААС.
Борьба против возникшего асцита включает назначение мочегонных средств, желательно калий-сберегающих (из-за возникающего альдостеронизма) и препаратов калия.
Воздействием на основное звено патогенеза при большинстве хронических и острых поражениях печени будет назначение гепатопротекторов.
Гепатопротекторы ‑ препараты, улучшающие метаболизм гепатоцитов, стабилизирующие их мембрану, предохраняющие их от разрушения (карсил, силибор, легалон).

Нарушение барьерной и детоксикационной функции печени. Фармакологическая разгонка детоксицирующей функции печени. Желтухи. Патогенетические варианты желтух. Принципиальное деление желчегонных препаратов на группы.
Нарушение антитоксической функции печени характеризуется:
Снижением обезвреживания печенью:
кишечных ядов - фенольных ароматических соединений (фенола, индола, скатола), биогенных аминов (кадаверина, путресцина, тирамина), аммиака;
ядовитых метаболитов: низкомолекулярных жирных кислот (валериановой, капроновой), метилированных и аминных производных серосодержащих аминокислот (тауриновой, цистина, метионина), токсического производного пирувата ацетоина;
экзогенных ядов (грибкового, микробного, паразитарного происхождения, ядохимикатов и др.).
Снижением инактивации клетками Купфера (звездчатыми ретикулоэндотелиоцитами) коллоидальных частиц и микроорганизмов.
Иногда, при сильной интоксикации, при угрозе или возникновении печеночной комы применяют препараты, усиливающие детоксицирующкю функцию печени, разгонку ее ферментов, особенно системы микросомального окисления – цитохромы (фенобарбитал).
Вместе с тем, следует учитывать, что другие фармакологические препараты способны наоборот угнетать ферментативные системы печени (левомицетин, бутадион, блокаторы холинэстеразы, моноаминооксидазы), а это может усилить интоксикацию при гепатитах и циррозах печени, а также изменить фармакокинетику других лекарств.
Желтуха проявляется желтой окраской кожи, слизистых оболочек, мочи и полостных жидкостей при участии билирубина.
Для правильной дифференциальной диагностики желтух необходимо знать фундаментальные физиологические основы образования и экскреции билирубина.