
- •Электорофорез Анализ молекулярной массы и субъединичного
- •1. Введение
- •Методические указания по выполнению практических
- •Электрофорез макромолекул
- •Экспериментальное исследование электрофореза в геле
- •3.1 Описание эксперимента
- •Н азначение: Обеспечивает одновременное заполнение раствором геля 4-х сборных кювет.
- •4.3.2 Камера электрофоретическая
- •4.3.3 Источник питания
- •4.4 Комплект приборов для проведения микрогельэлектрофореза (№2)
- •4.4.2 Камера электрофоретическая для микроэлектрофореза
- •5. Вопросы и задания к практической работе
- •Библиографический список
Экспериментальное исследование электрофореза в геле
3.1 Описание эксперимента
Наиболее ценным методом определения молекулярной массы белков является электрофорез в присутствии додецилсульфата натрия в полиакриламидном геле (Вебер и Осборн, 1969). Экспериментально установлено, что только при определенных условиях электрофоретическая подвижность зависит от молекулярной массы, и на эту зависимость не влияет общий заряд макромолекулы. Для этого белок обрабатывают 1% раствором додецилсульфата натрия (ДСН), который является детерогентом и хорошим денатурирующим агентом белков. Кроме того, добавляют -меркапэтанол для разрыва дисульфидных связей. Додецилсульфат натрия совершенно одинаково связывается со всеми белками: 1,4 кг ДСН на 1 кг белка. Каждая молекула ДСН несет один отрицательный заряд и, таким образом, общая плотность заряда примерно одинаковая для разных белков. Таким образом, поверхностная шуба из молекул ДСН устраняет зарядовые различия, существующие в нативных белках. После денатурации белка полипептидная цепь представляют вытянутый цилиндр постоянного диаметра 1,8 нм. Длина таких стержней коррелирует с молекулярной массой белков: чем длиннее цилиндр, тем больше молекулярная масса (рис.1, а).
В качестве носителя при электрофорезе используют полиакриламидный гель в концентрации от 5 до 15%. Экспериментально установлена линейная связь между электрофоретической подвижностью и логарифмом молекулярной массы:
u=b – a lgM , (5)
где a и b - постоянные, зависящие от свойств полиакриламидного геля. Для определения молекулярной массы исследуемого белка необходимо построить калибровочную кривую. В одинаковых условиях проводится электрофорез маркерных белков с известной молекулярной массой и строится зависимость u=f (lgM) (рис.1, б). По измеренной электрофоретической скорости и на калибровочной кривой с высокой точностью (до 5%) находят молекулярную массу исследуемого белка.
Второе важное преимущество электрофореза в присутствии ДСН состоит в том, что этот метод позволяет определять субъединичное строение сложных белков, имеющих четвертичную структуру.
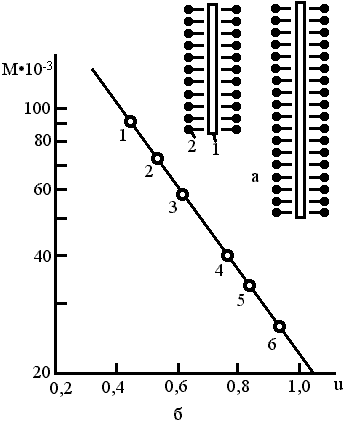
Рис.1. Электрофорез в присутствии додецилсульфата натрия (ДСН):
а) – комплекс полипептидной цепи (1) с молекулами ДСН (2);
б) – полулогарифмическая зависимость молекулярной массы М от относительной электрофоретической подвижности u; маркерные белки: 1 – фосфорилаза А, 2 – трансферин, 3 – каталаза, 4 – овальбумин, 5 – пепсин, 6 – химотрипсиноген.
КОМПЛЕКТЫ ПРИБОРОВ ДЛЯ ЭЛЕКТРОФОРЕЗА В ГЕЛЕ
4.1 Назначение:
Комплекты приборов для электрофореза предназначены для формирования пластин геля и проведения злектрофоретического разделения белков и нуклеиновых кислот.
4.2 Типы комплектов:
• Комплект приборов для проведения классического гельэлектрофореза (комплект №1)
• Комплект приборов для проведения микрогельэлектрофореза (комплект №2)
4.3 Комплект приборов для проведения классического гельэлектрофореза (№1)
В состав комплекта входят:
• бокс для формирования пластин геля;
• камера электрофоретическая;
• источник питания.
4.3.1 Бокс для формирования пластин геля
