
- •1.Курсовое проектирование.
- •1.1.Оформление пояснительной записки.
- •1.2.Оформлене графической части проекта.
- •1.3.Задания для выполнения расчета процесса ректификации.
- •2.0.Материальный баланс.
- •2.1.Определение давления в колонне.
- •2.2Определение температурного режима колонны.
- •2.3.Построение диаграммы фазового равновесия.
- •2.4.Определение числа теоретических тарелок.
- •2.5. Определение расхода пара и флегмы.
- •3.0 Тепловой баланс колонны.
- •4.0. Гидравлический расчет.
- •5.0. Определение диаметра штуцеров.
- •6.0. Определение толщины тепловой изоляции.
- •7.0. Определение площади поверхности теплопередачи кипятильника и дефлегматора.
- •8.0. Пример расчета (вариант №1, см.Табл. 1)
- •8.1. Составление материального баланса колонны [26]
- •8.2. Определение давления в колонне
- •8.3. Построение диаграммы фазового равновесия в координатах у-х
- •8.4. Определение числа теоретических тарелок в колонне
- •8.5. Определение расходов пара и флегмы в колонне
- •8.6. Тепловой баланс колонны
- •8.7. Гидравлический расчет.
- •8.8. Определение диаметров штуцеров
- •8.9. Определение толщины тепловой изоляции колонны
- •8.10. Определение площади поверхности дефлегматора теплопередачи кипятильника и дефлегматора.
- •Библиографический список:
2.2Определение температурного режима колонны.
При заданном составе паровой, жидкой или парожидкостной смеси и фиксированном давлении в системе температура, составляющая равновесию в таких условиях, определяется расчетом.
Температура верха колонны определяется из уравнения изотермы паровой фазы:
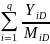 =
1 (15)
=
1 (15)
Где,
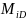 – коэффициент распределения (константа
фазового равновесия); i-того
компонента при температуре и давлении
наверху колонны;
– мольная доля компонента в паре наверху
колонны, в случае полной конденсации
паров в дефлегматоре
=
;
q–
число компонентов смеси.
– коэффициент распределения (константа
фазового равновесия); i-того
компонента при температуре и давлении
наверху колонны;
– мольная доля компонента в паре наверху
колонны, в случае полной конденсации
паров в дефлегматоре
=
;
q–
число компонентов смеси.
Температура внизу колонны определяется из уравнения изотермы жидкой фазы:
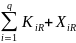 =
1 (16)
=
1 (16)
Где,
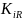 – коэффициент распределения i-того
компонента при температуре и давлении
низа колонны.
– коэффициент распределения i-того
компонента при температуре и давлении
низа колонны.
Если
сырье поступает в колонну при температуре
начала кипения смеси, т.е. доля отгона
сырья на входе в колонну e=0,
температура сырья
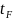 определяется по уравнению изотермы
жидкой фазы (16). Если сырье поступает в
колонну при температуре конца кипения
смеси, доля отгона е=1,температура сырья
определяется по уравнению изотермы
паровой фазы (15). Если сырье поступает
в колонну в виде парожидкостной смеси,
т.е.
определяется по уравнению изотермы
жидкой фазы (16). Если сырье поступает в
колонну при температуре конца кипения
смеси, доля отгона е=1,температура сырья
определяется по уравнению изотермы
паровой фазы (15). Если сырье поступает
в колонну в виде парожидкостной смеси,
т.е.
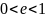 ,
температура сырья на входе в колонну
,
температура сырья на входе в колонну
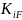 определяется из уравнения:
определяется из уравнения:
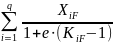 =
1 (17)
=
1 (17)
или
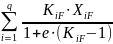 =
1 (18)
=
1 (18)
Где, - коэффициент распределения i-того компонента смеси при температуре и давлении в зоне питания колонны.
Уравнение
(17) лучше использовать при доле отгона
е=0,5, а уравнение (18) дает лучший результат
при доле отгона е 0,5.
0,5.
Коэффициенты
распределения
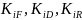 зависят от температуры, поэтому уравнение
(15) - (18) при расчете температур
,
,
решаются методом последовательного
приближения.
зависят от температуры, поэтому уравнение
(15) - (18) при расчете температур
,
,
решаются методом последовательного
приближения.
2.3.Построение диаграммы фазового равновесия.
В процессах перегонки и ректификации равновесные концентрации фаз определяются зависимостью:
 =
=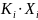 (19)
(19)
Где,
- мольная концентрация i-того
компонента в паре, равновесном с жидкостью
состава
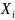 .
.
В
случае, когда разделяемую смесь можно
считать идеальной, т.е. для всех компонентов
смеси выполняется закон Раули, коэффициент
распределения
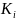 рассчитывается как отношение давления
насыщенного пара компонента
рассчитывается как отношение давления
насыщенного пара компонента
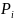 при ректификационной температуре к
общему давлению в системе П:
при ректификационной температуре к
общему давлению в системе П:
=
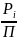 (20)
(20)
Для идеальных смесей зависимость между равновесными составами фаз выражается уравнением Рауля-Дальтона:
=
 (21)
(21)
Для многих жидких смесей расчет коэффициента распределения можно производить по уравнению (20), если общее давление в системе П 0,49 Па (5ат.).
Давление насыщенных паров индивидуальных веществ или зависимости для их расчета приведены в работах [1-6].
Для
бинарных смесей, подчиняющихся закону
Рауля, диаграмму фазового равновесия
в координатах у-х (рис.2) строят по
следующему алгоритму. Температурный
интервал выкипания разделяемой смеси
определяется, как разность температур
кипения чистого низкокипящего
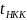 и чистого высококипящего
и чистого высококипящего
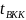 компонентов при выбранном давлении в
системе П. В этом интервале температур
от
до
принимается ряд значений температуры
(обычно десяти значений бывает достаточно);
для каждой температуры определяется
значение насыщенных паров компонентов
и рассчитывается из соотношения (20)
коэффициенты распределения низкокипящего
компонента. Из соотношения (22) рассчитывается
мольная концентрация низкокипящего
компонента
компонентов при выбранном давлении в
системе П. В этом интервале температур
от
до
принимается ряд значений температуры
(обычно десяти значений бывает достаточно);
для каждой температуры определяется
значение насыщенных паров компонентов
и рассчитывается из соотношения (20)
коэффициенты распределения низкокипящего
компонента. Из соотношения (22) рассчитывается
мольная концентрация низкокипящего
компонента
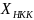 в жидкости, кипящей при выбранной
температуре и давлении П:
в жидкости, кипящей при выбранной
температуре и давлении П:
=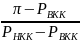
Где,
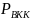 ,
,
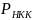 – давление насыщенных паров высококипящего
и низкокипящего компонентов.
– давление насыщенных паров высококипящего
и низкокипящего компонентов.
После
этого из соотношения (21)определяется
мольная концентрация низкокипящего
компонента в паре
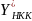 ,
равновесном с жидкостью. Далее строится
диаграмма фазового равновесия в
координатах у-х (см. рис.2).
,
равновесном с жидкостью. Далее строится
диаграмма фазового равновесия в
координатах у-х (см. рис.2).
В
тех случаях, когда для компонентов
разделяемой смеси наблюдаются значительные
отклонения от закона Рауля, приведенный
выше алгоритм вычисления равновесной
паровой и жидкой фаз сохраняется,
изменяется лишь способ расчета
коэффициента распределения
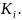

Рис.2. Диаграмма фазового равновесия бинарной смеси в координатах у-х.
В работе [9] рассмотрены методы расчета для смесей, не подчиняющихся закону Рауля. С целью облегчения расчетов разработаны различные монограммы для определения коэффициента распределения [6, 10], в частности, для ориентировочных расчетов широко используется номограмма Де-Пристера [5, 9]. Для многих бинарных смесей равновесные составы паровой и жидкой фаз приведены в работе [11].
