
Медичні комп'ютерні системи візуалізації
Медичні комп'ютерні системи візуалізації — це приладо-комп'ютерні системи, призначені для дослідження внутрішніх органів та їхніх структур з виведенням зображення на екран. Інформацію "збирають" інформаційні промені — хвильові процеси різної фізичної природи, які можна використати як інформацію, що надходить від тіла людини. Згідно із законами фізики, усе живе на Землі існує і розвивається в постійній взаємодії з випромінюваннями та пружними коливаннями. Інформаційними променями можуть бути інфрачервоні (системи динамічного теплобачення), рентгенівські (комп'ютерні рентгенівські томографи), радіоактивні (позитронно-емісійні томографи), ультразвукові (системи УЗД), електромагнітно-резонансні (магнітно-ядерні резонансні томографи для МРТ). Розуміння фізичної природи і біологічної дії випромінювання на людину дуже важливе при вивченні комп'ютерних систем візуалізації, які можна розглядати як новий напрямок радіології1.
Медична радіологія — галузь медицини, що розробляє теорію і практику застосування випромінювань для медичних потреб. Медична радіологія включає дні основні наукові дисципліни: діагностичну радіологію (променеву діагностику) і терапевтичну радіологію (променеву терапію). Променева діагностика розглядає питання впливу випромінювань на організм людини з метою профілактики і розпізнавання хвороб. Без радіології сьогодні не може обійтися жодна медична дисципліна, у тому числі й інформатика.
Принцип обробки даних у візуальних комп'ютерних системах: інформаційні промені, що виходять від досліджуваного органа, фіксуються датчиками-приймачами, перетворюються на електричні сигнали, відцифровуються за допомогою АЦП і надходять у пам'ять комп'ютера (схема 11). Після обробки програмним забезпеченням МПКС інформація реконструюється у вигляді зображення і подається на екран монітора лікаря. На підставі даних аналізу картинки та зіставлення клінічних симптомів встановлюють діагноз. Слід уточнити, що саме лікар, а не машина розпізнає відхилення від норми при аналізі зображення.
Комп'ютерна томографія
КТ — принципово новий та універсальний метод пошарового дослідження тонких шарів тканин. Звідси назва методу — томографія (від грец. tomos — шар). За її допомогою можна вивчати всі частини тіла, всі органи, визначати положення, форму, розміри, стан поверхні та структуру органа, досліджувати його функції, у тому числі кровообіг, а також вимірювати щільність будь-якої ділянки тканин. Сучасні томографи дають змогу одержувати зображення дуже тонких шарів — від 0,5 до 10 мм. Зображення може бути площинне (2D) і об'ємне (3D). Термін "комп'ютерна томографія" на сьогодні застосовується стосовно різних сканувальних комп'ютерних томографічних методів дослідження, а не тільки щодо рентгенологічної комп'ютерної томографії, винайдення якої започаткувало розвиток описувальних методик.
Залежно від природи інформаційних променів виділяють такі види КТ:
рентгенологічну КТ (РКТ);
томографію з використанням електромагнітних полів (МРТ);
томографію з використанням електромагнітного випромінювання (позитронно-емісійна (ПЕТ)).
Процес удосконалювання КТ триває. Медична техніка на світовому ринку модернізується з кожним роком. Стрімко інтегруються нові комп'ютерні технології, застосовуються нові принципи обстеження. Сучасний комп'ютерний

Прогрес КТ прямо пов'язаний зі збільшенням кількості детекторів, тобто зі збільшенням кількості проекцій, що збираються одночасно. У першому поколінні КТ кількість детекторів становила 2, у другому — 30—50, у третьому — 300—500, у четвертому — 1000—5000. У другому поколінні було вперше застосовано віялову форму пучка рентгенівського випромінювання. Кожне наступне покоління комп'ютерних томографів відзначалось істотно меншим часом реконструкції КТ-зображень і більшою швидкістю обертання рентгенівської трубки, що дало змогу прискорити і розширити сфери діагностичного застосування КТ-досліджень.
Рентгенівська комп'ютерна томографія
Як було зазначено вище, при КТ уперше було використано рентгенівське випромінювання як джерело інформації для математичної обробки. Цей чутливий і високоінформативний метод рентгенодіагностики — пошарове рентгенологічне дослідження, засноване на комп'ютерній реконструкції зображення, одержуваного при круговому скануванні об'єкта вузьким пучком рентгенівських променів.
Фізична природа процесу томографування полягає в наступному: інформаційний промінь сканує ("переглядає") людське тіло по окружності. По інший бік рентгенівської трубки встановлено систему датчиків, кількість яких змінювалася від двох (перше покоління томографів) до 500 (третє покоління) і до кількох тисяч твердотільних датчиків, розташованих у кілька рядів (четверте покоління).
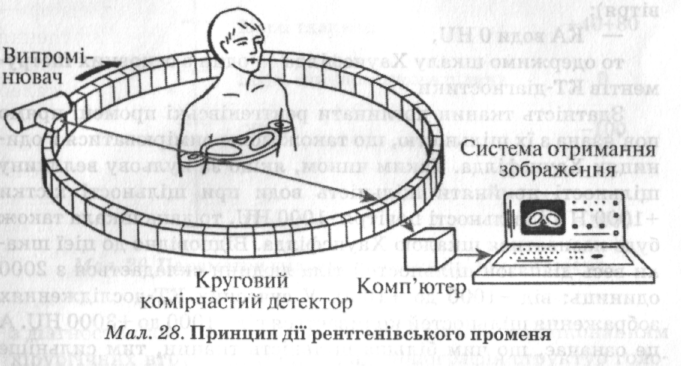
Мал. 3. Принцип дії рентгенівського променя
Ці датчики фіксують змінені кількісні характеристики інформаційних променів, тобто відтворюють ступінь ослаблення пучка. Обертаючись навколо пацієнта, рентгенівський промінь "переглядає" його тіло під різними ракурсами, у цілому під кутом 360° (мал. 3). До кінця обертання випромінювача в пам'яті комп'ютера зберігаються зафіксовані сигнали всіх датчиків. Накопичена інформація у вигляді масиву даних обробляється ППЗ, за допомогою якого реконструюється графічне зображення зрізу (графічна матриця). Воно складається з кількох десятків тисяч світлових точок, яскравість яких пропорційна щільності тканин, через які проходив пучок випромінювання. При цьому комп'ютером розраховується коефіцієнт ослаблення променів або коефіцієнт абсорбції (КА) тканин, що виражається в одиницях Хаунсфілда (Hounsfield Units, HU), для кожної точки зображення. Ця величина показує, наскільки біологічна тканина здатна поглинати (послаблювати) рентгенівські промені. Кістка поглинає рентгенівські промені сильніше порівняно з іншими тканинами і має найбільший КА (+800+ +3000 HU). Повітря практично не поглинає промені і має найменший КА (-1000 HU). Якщо розмістити на прямій три основні точки КА:
КА максимального ослаблення +1000 HU (щільність кам'янистої частини скроневої кістки);
КА мінімального ослаблення -1000 HU (щільність повітря);
КА води 0 НU, то одержимо шкалу Хаунсфілда — один з основних інструментів КТ-діагностики.
Здатність тканин поглинати рентгенівські промені прямо пов'язана з їх щільністю, що також може вимірюватися в одиницях Хаунсфілда. Таким чином, якщо за нульову величину щільності прийнята щільність води при щільності кістки + 1000 HU і щільності повітря -1000 HU, то дана шкала також буде називатися шкалою Хаунсфілда. Відповідно до цієї шкали весь діапазон щільностей тіла людини складається з 2000 одиниць: від -1000 до +1000. У сучасних КТ-дослідженнях зображення щільностей коливається від -1000 до +3000 HU. A це означає, що чим більша щільність тканин, тим сильніше вона поглинає випромінювання і тим світлішою ця тканина є на екрані: кістка біла, повітря чорне. Таким чином, нормальні і патологічні утворення розрізняють за градаціями переходу від чорного до білого кольору. Деякі тканини і відповідні їм параметри щільності, виражені в одиницях Хаунсфілда, наведено на мал. 29.

Користуючись клавіатурою, лікар може збільшувати це зображення, виділяти і збільшувати окремі його частини, вимірювати розміри органа, визначати щільність кожної ділянки тканини в умовних одиницях. За серією двовимірних зображень за допомогою математичних методів обробки можна відновити об'ємне зображення об'єкта.
У медицині побачити невидиме або ледве помітне оком означає встановити діагноз на ранній стадії захворювання, коли ще можна уникнути небезпечного розвитку патології та оперативного втручання. Основою візуального аналізу будь-яких зображень є пошук і виявлення ледве помітних і невидимих оку лікаря діагностичних ознак. КТ використовують не тільки з діагностичною метою, а і як метод контролю за виконанням хірургічних втручань. Наприклад, топографія структур головного мозку різко змінюється після розкриття черепа при втручанні на патологічному вогнищі. Під час операції потрібна постійна корекція в оцінці взаємодії анатомічних структур. Під контролем КТ уводять волоконно-оптичні прилади і мікрохірургічні інструменти в ушкоджені ділянки дисків хребців і виконують найтонші операції.
Спочатку існували комп'ютерні томографи для дослідження тільки головного мозку. Це зараз звучить буденно, але 35 років тому вперше у світі людство одержало можливість заглянути усередину живого мозку й судити про порушення в ньому не по непрямих ознаках, а вивчати морфологічні зміни самого субстрату, диференціювати сіру й білу речовину. Технічний прогрес привів до вдосконалювання апаратур: з'явилися могутніші, швидкісні апарати, пристосовані для дослідження всього тіла пацієнта (мал. 5). Проблему диференціації органів і тканин, що мають рівну або дуже близьку щільність за шкалою Хаунсфілда, було вирішено шляхом внутрішньовенного контрастного посилення, тобто введення таких речовин в організм людини, які, накопичуючись в органах, змінювали їхню щільність. Методики контрастного посилення дають змогу розрізняти й визначати характер пухлин (новоутворень) на фоні м'яких тканин, що їх оточують, у тих випадках, коли вони не видимі при звичайному дослідженні.
Мал. 5. Дослідження усього тіла пацієнта
На сьогодні нараховуються чотири покоління рентгенівських комп'ютерних томографів. Прикладом томографа третього покоління є спіральний томограф, названий так через обертальне переміщення віялового рентгенівського пучка, що створює траєкторію спіралі. Більшість сучасних установок в Україні — це апарати третього покоління. Якщо на апаратах першого покоління процес зчитування інформації і реконструювання одного зображення займав кілька хвилин, на апаратах другого — десятки секунд, то на томографах третього і четвертого поколінь — кілька секунд. Таким чином, щоб дослідити головний мозок на томографах першого покоління з товщиною зрізу 10 мм (тобто кількість зрізів — до 8), необхідно було затратити 8—10 хв. У 2004—2005 роках було розроблено 32- і 64-зрізові мультиспіральні томографи, які є вершиною технічного прогресу (мал. 6).
.
Мал. 6. Спіральний комп’ютерний томограф
Недоліком КТ є створення променевого навантаження (рентгенівське випромінювання), тому застосування її без достатніх підстав (показань) небажане.
Томографія з використанням електромагнітних полів
Д ругий
вид КТ —
томографія ядерно-магнітного резонансу
(ЯМР, або МРТ). Термін "ЯМР-томографія"
було замінено на "МРТ-томографію"
в 1986 році у зв'язку з розвитком у людей
нуклеофобії після Чорнобильської
аварії. У новому терміні відсутнє
нагадування про "ядерність"
походження методу, що і дало змогу
впровадити його безболісно в повсякденну
медичну практику.
ругий
вид КТ —
томографія ядерно-магнітного резонансу
(ЯМР, або МРТ). Термін "ЯМР-томографія"
було замінено на "МРТ-томографію"
в 1986 році у зв'язку з розвитком у людей
нуклеофобії після Чорнобильської
аварії. У новому терміні відсутнє
нагадування про "ядерність"
походження методу, що і дало змогу
впровадити його безболісно в повсякденну
медичну практику.
Д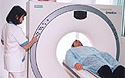
 жерело
інформаційних променів — людина, яка
випромінює електромагнітне резонансне
випромінювання. Фізична суть МРТ: якщо
систему (досліджувану ділянку тіла
пацієнта), що перебуває в постійному
магнітному полі, опромінити зовнішнім
змінним електромагнітним полем, частота
якого точно дорівнює частоті переходу
між енергетичними рівнями ядер атомів,
то ядра почнуть переходити у квантовий
стан, енергетично вищий. Інакше
кажучи, спостерігається резонансне
поглинання енергії електромагнітного
поля. У разі припинення впливу змінного
електромагнітного поля виникає резонансне
виділення енергії, що і фіксує система.
МРТ дає можливість одержувати зображення
будь-яких шарів тіла людини. Більшість
сучасних MP-томографів
"налаштовані" на реєстрацію
радіосигналів ядер водню, що містяться
у тканинній рідині або жировій тканині.
Тому MP-томограма
дає картину просторового розподілу
молекул, що містять атоми водню (як
відомо, людина складається на 75—80 %
з води, до складу якої входить водень,
що дає резонансне електромагнітне
випромінювання, тобто несе інформацію).
Чутливі датчики (високочастотні котушки)
сприймають сигнали релаксації, тобто
інформаційні промені від пацієнта, і
направляють їх в обчислювальний
комплекс, де інформація обробляється
до вигляду зображення. С
жерело
інформаційних променів — людина, яка
випромінює електромагнітне резонансне
випромінювання. Фізична суть МРТ: якщо
систему (досліджувану ділянку тіла
пацієнта), що перебуває в постійному
магнітному полі, опромінити зовнішнім
змінним електромагнітним полем, частота
якого точно дорівнює частоті переходу
між енергетичними рівнями ядер атомів,
то ядра почнуть переходити у квантовий
стан, енергетично вищий. Інакше
кажучи, спостерігається резонансне
поглинання енергії електромагнітного
поля. У разі припинення впливу змінного
електромагнітного поля виникає резонансне
виділення енергії, що і фіксує система.
МРТ дає можливість одержувати зображення
будь-яких шарів тіла людини. Більшість
сучасних MP-томографів
"налаштовані" на реєстрацію
радіосигналів ядер водню, що містяться
у тканинній рідині або жировій тканині.
Тому MP-томограма
дає картину просторового розподілу
молекул, що містять атоми водню (як
відомо, людина складається на 75—80 %
з води, до складу якої входить водень,
що дає резонансне електромагнітне
випромінювання, тобто несе інформацію).
Чутливі датчики (високочастотні котушки)
сприймають сигнали релаксації, тобто
інформаційні промені від пацієнта, і
направляють їх в обчислювальний
комплекс, де інформація обробляється
до вигляду зображення. С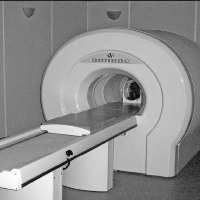 истема
для МРТ складається з:
истема
для МРТ складається з:
магніту, що створює статистичне магнітне поле з напругою від 0,5 до 1,5 Т і З Т. Магніт порожній. У ньому є тунель, у якому розміщується пацієнт. Стіл для пацієнта має автоматичну систему керування рухом у поздовжньому і вертикальному напрямках;
високочастотних котушок різної конфігурації для дослідження різних ділянок тіла пацієнта. Котушки служать для радіохвильового збудження ядер водню і створення ефекту спину, а також прийому інформаційного сигналу. Котушки накладають на досліджувану ділянку. Створюється додаткове магнітне поле і збудження ядер водню (поглинання енергії електромагнітного поля). Котушки сприймають електромагнітне випромінювання (водневий спектр) від пацієнта при резонансному виділенні енергії. Таким чином, метод засновано на вимірюванні електромагнітної відповіді атомів водню на збудження їх певною комбінацією електромагнітних хвиль у постійному магнітному полі високої напруги.
Локальна комп'ютерна мережа системи, що складається з 2—З ПК, здійснює обробку даних, управляє системою магнітного поля, забезпечує узгодженість усіх компонентів МРТ. При цьому вирішується головне завдання — одержання зображення тонких шарів тіла людини в будь-якому розрізі — фронтальному, сагітальному, аксіальному і косій площинах. Можливими стали одержання об'ємних зображень органів, вимірювання швидкості кровотоку, току спинномозкової рідини, визначення рівня дифузії в тканинах, візуалізація активації кори головного мозку при функціонуванні органів, за які відповідає ця ділянка кори.
МРТ протипоказана при:
клаустрофобії,
за наявності сторонніх металевих включень в організмі (штучні металеві суглоби, кульові осколки, які можуть зміститися під дією магнітного поля),
вживлених кардіостимуляторів, робота яких може бути порушена. При МРТ, як і при рентгенологічному дослідженні, можна застосовувати штучне контрастування тканин. Із цією метою використовують хімічні речовини, що містять ядра з непарним числом протонів і нейтронів, наприклад, сполуки фтору, або ж парамагнетики, які змінюють час релаксації води і тим самим посилюють контрастність зображення.
МРТ — високоефективний діагностичний метод, абсолютно безпечний для пацієнта навіть за умови багаторазового застосування.
Позитронно-емісійна томографія
ПЕТ — радіонуклідний томографічний метод дослідження внутрішніх органів людини. Інформаційним променем виступає радіоактивне випромінювання тіла людини під дією введених радіофармпрепаратів (РФП) з малим періодом піврозпаду: 11С-вуглець (період піврозпаду Т1/2 становить 20,4 хв), 13N-asoт (Т1/2 — 10 хв), 15О-кисень (Т1/2 — 2,03 хв), 18Р-фтор (Т — 110 хв). Після цього людина стає джерелом випромінювання, тобто інформації. Метод засновано на реєстрації пари -квантів, що виникають при анігіляції електронів і позитронів. При анігіляції пара "позитрон — електрон" зникає, утворюючи два -кванти, що розлітаються в протилежних напрямках. Кожний із цих квантів має енергію 511 кеВ. Ці два кванти реєструються двома протилежно розташованими датчиками, розміщеними в кілька рядів кільцем діаметра 45— 65 см. Сприйняте високочастотне електромагнітне випромінювання (-кванти) перетворюється на цифровий код, а потім обробляється на ПК.
Чутливість ПЕТ вища, ніж КТ і МРТ. За допомогою ПЕТ вдається констатувати зміну витрат глюкози, міченої 11С в "очному центрі" головного мозку, при відкриванні очей. Тому ІІЕТ використовують при дослідженнях найтонших метаболічних процесів у мозку, аж до розумових. Позитронно-активні радіонукліди дуже швидко розпадаються. До того ж усі вони циклотронного походження. Отже, ПЕТ застосовують лише в радіологічному центрі, оснащеному циклотроном, радіофармацевтичною лабораторією, позитронним томографом і комп'ютером для обробки інформації.
Ультразвукове дослідження
У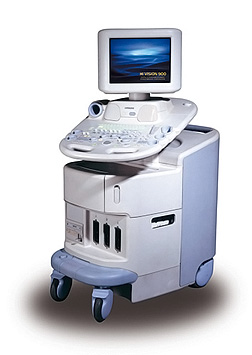 ЗД
—
досить поширений метод діагностики.
Інформаційним променем є ультразвукова
хвиля (УЗХ), відбита від межі розділення
двох різних за щільністю середовищ.
Ультразвуком взагалі називають
високочастотні звукові хвилі із частотою
понад 20 кГц. У медицині застосовують
частоти діапазону 2—10 МГц. Особливістю
УЗХ є їхня здатність відбиватися від
границь середовищ, що різняться щільністю.
Пучок УЗХ направляється на досліджувану
ділянку, попередньо змочену гелем
для зменшення повітряної щілини між
датчиком і поверхнею шкіри, а, отже,
і для зменшення втрати енергії
ультразвукового потоку. Відбиті УЗХ
вловлюються датчиком (датчик є
високотехнологічним приладом, здатним
як генерувати, так і сприймати УЗХ)
апарата. Після посилення УЗХ і перетворення
в електричні сигнали інформація
оцифровується за допомогою АЦП і
передається в пам'ять комп'ютера.
Комп'ютер за допомогою програмного
забезпечення обробляє оцифровану
інформацію і видає на екран д вовимірну
реконструкцію зображення всіх тканин,
крізь які пройшли УЗХ.
ЗД
—
досить поширений метод діагностики.
Інформаційним променем є ультразвукова
хвиля (УЗХ), відбита від межі розділення
двох різних за щільністю середовищ.
Ультразвуком взагалі називають
високочастотні звукові хвилі із частотою
понад 20 кГц. У медицині застосовують
частоти діапазону 2—10 МГц. Особливістю
УЗХ є їхня здатність відбиватися від
границь середовищ, що різняться щільністю.
Пучок УЗХ направляється на досліджувану
ділянку, попередньо змочену гелем
для зменшення повітряної щілини між
датчиком і поверхнею шкіри, а, отже,
і для зменшення втрати енергії
ультразвукового потоку. Відбиті УЗХ
вловлюються датчиком (датчик є
високотехнологічним приладом, здатним
як генерувати, так і сприймати УЗХ)
апарата. Після посилення УЗХ і перетворення
в електричні сигнали інформація
оцифровується за допомогою АЦП і
передається в пам'ять комп'ютера.
Комп'ютер за допомогою програмного
забезпечення обробляє оцифровану
інформацію і видає на екран д вовимірну
реконструкцію зображення всіх тканин,
крізь які пройшли УЗХ.
УЗД є методом медичної візуалізації, який почали застосовувати понад 40 років тому. Сфера застосування ультразвуку в медицині надзвичайно широка. З діагностичною метою його використовують для виявлення захворювань органів черевної порожнини і нирок, органів малого таза, щитоподібної залози, грудних залоз, лімфатичної і серцево-судинної систем, в акушерській і педіатричній практиці. В абдомінальній практиці УЗД дає змогу візуалізувати й охарактеризувати (розміри контури, структура, щільність) усі паренхіматозні органи (печінку, селезінку, підшлункову залозу, нирки), наповнені рідиною порожнисті органи (жовчний міхур і протоки), кровоток судини, фрагменти кишкових петель, вільну рідину в черевній порожнині, збільшені лімфатичні вузли, пухлинні конгломерати, змінений червоподібний відросток. Роздільна здатність сучасних апаратів становить 1—2 мм. Недоступними для УЗД є тканини, що містять повітря, і кістки.
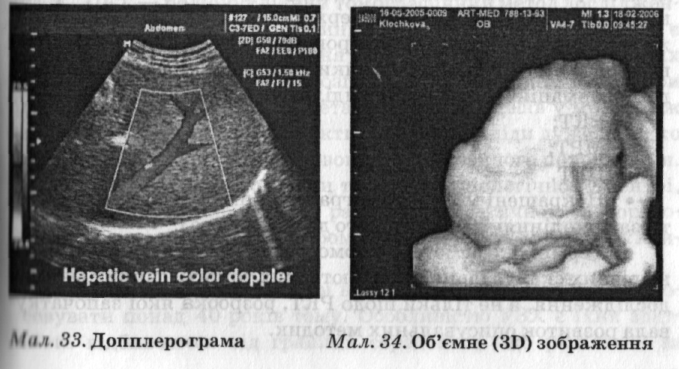
З ображення
приймається в режимі сірої шкали (від
абсолютно білого до абсолютно чорного
кольору). Для дослідження потоків
рідини застосовують штучне виділення
кольорів у колірних апаратах Допплера
(Color
Doppler).
Наприклад, кровотік до датчика
прийнято позначати червоним кольором,
від датчика — синім, турбулентний
кровотік — синьо-зелено-жовтим кольором
(мал.
33).
Колірний допплер застосовують для
дослідження кровотоку в судинах, в
ехо-кардіографії. У сучасних
приладо-комп'ютерних системах УЗД
використовують нові функціональні
можливості: автоматичне обчислення
обсягу структур складної форми, одержання
об'ємних (3D) зображень (мал. 34) у режимі
сірої шкали і кольорового допплера,
одержання будь-якого зрізу в кожній з
трьох проекцій.
ображення
приймається в режимі сірої шкали (від
абсолютно білого до абсолютно чорного
кольору). Для дослідження потоків
рідини застосовують штучне виділення
кольорів у колірних апаратах Допплера
(Color
Doppler).
Наприклад, кровотік до датчика
прийнято позначати червоним кольором,
від датчика — синім, турбулентний
кровотік — синьо-зелено-жовтим кольором
(мал.
33).
Колірний допплер застосовують для
дослідження кровотоку в судинах, в
ехо-кардіографії. У сучасних
приладо-комп'ютерних системах УЗД
використовують нові функціональні
можливості: автоматичне обчислення
обсягу структур складної форми, одержання
об'ємних (3D) зображень (мал. 34) у режимі
сірої шкали і кольорового допплера,
одержання будь-якого зрізу в кожній з
трьох проекцій.
До основних переваг УЗД відносять:
універсальність та інформативність;
мобільність і швидкість виконання;
неінвазивність;
відсутність променевого навантаження.
Метод УЗД простий, доступний і безпечний. Він не має нічого спільного з рентгенівським випромінюванням. Саме тому УЗД широко застосовують в акушерстві. Медики вважають, що раз на рік його повинна проходити кожна людина, адже що раніше виявлено хворобу, тим легше її лікувати.
УЗД здійснюють у режимі реального часу. Це дає змогу простежувати, як змінюється зображення тієї або іншої деталі залежно від проекції, і швидко переходити від однієї зображуваної площини до іншої.
Недоліки УЗД: ослаблення УЗ-променя у високощільних тканинах; результати УЗД залежать від досвіду лікаря набагато більше, ніж при інших методах.
Стисло про головне
Медичні комп'ютерні системи візуалізації — це приладо-комп'ютерні системи, призначені для дослідження внутрішніх органів та їхніх структур з виведенням зображення на екран. Інформацію "збирають" інформаційні промені — хвильові процеси різної фізичної природи, які можна використати як інформацію, що надходить від тіла людини.
КТ — принципово новий і універсальний метод пошарового дослідження тонких шарів тканин. З її допомогою можна досліджувати всі частини тіла, всі органи, визначати положення, форму, величину, стан поверхні і структуру органа, досліджувати функції, у тому числі кровообіг органа, а також вимірювати щільність будь-якої ділянки тканини. Залежно від природи інформаційних променів виділяють такі види КТ:
РКТ;
МРТ;
ПЕТ.
Моделі томографів прийнято систематизувати за поколіннями (від першого до четвертого).
Термін "комп'ютерна томографія" застосовують стосовно різних сканувальних комп'ютерних томографічних методів дослідження, а не тільки щодо РКТ, розробка якої започаткувала розвиток описувальних методик.
РКТ засновано на обробці зафіксованого інформаційного рентгенівського сигналу при проходженні його через досліджувану ділянку з подальшою комп'ютерною обробкою. В основі формування зображення лежить шкала Хаунсфілда, що показує залежність щільності біологічних тканин від їхньої здатності послаблювати (поглинати) рентгенівські промені.
32- і 64-зрізові мультиспіральні томографи — апарати третього покоління, оснащені кількома тисячами твердотільних датчиків, розташованих у кілька рядів. Томограф несе променеве навантаження (рентгенівське випромінювання), і застосування КТ без достатніх на те підстав (показань) небажане. Довжина зони сканування тіла пацієнта має бути обмеженою, не перевищувати 20—25 см.
Джерелом інформаційних променів при МРТ є тіло людини, що дає електромагнітне резонансне випромінювання. Більшість сучасних MP-томографів "налаштована" на реєстрацію радіосигналів ядер водню, що містяться у тканинній рідині або жировій тканині. Тому MP-томограма — це картина просторового розподілу молекул, що містять атоми водню. МРТ протипоказана при клаустрофобії, за наявності в тілі сторонніх металевих предметів, вживлених кардіостимуляторів. При МРТ, як і при рентгенологічному дослідженні, можна застосовувати штучне контрастування тканин. МРТ — високоефективний діагностичний метод, абсолютно безпечний навіть за умови багаторазового застосування.
ПЕТ — радіонуклідний томографічний метод дослідження внутрішніх органів людини. Інформаційним променем є радіоактивне випромінювання тіла людини під дією введених РФП з малим періодом піврозпаду. ПЕТ використовують при дослідженнях найтонших метаболічних процесів у мозку, аж до розумових. Позитронно-активні радіонукліди дуже швидко розпадаються. До того ж усі вони циклотронного походження. Отже, ПЕТ можна проводити тільки в радіологічному центрі, оснащеному циклотроном, радіофармацевтичною лабораторією, позитронним томографом і комп'ютером для обробки інформації.
УЗД — метод медичної візуалізації, який почали застосовувати понад 40 років тому. Особливістю УЗХ є їхня здатність відбиватися від границь середовищ, що різняться за щільністю. Відбиті УЗХ вловлюються датчиком апарата. Після посилення УЗХ і перетворення їх на електричні сигнали інформація оцифровується за допомогою АЦП і передається в пам'ять комп'ютера. Комп'ютер за допомогою програмного забезпечення обробляє цю інформацію і видає на екран двовимірну реконструкцію зображення всіх тканин, крізь які пройшли УЗХ. Метод УЗД простий у застосуванні, доступний і безпечний.
Контрольні питання
Назвіть відомі вам медичні комп'ютерні системи візуалізації.
Як відбувається збирання інформації в системах візуалізації?
Чому комп'ютерні системи візуалізації можна розглядати як новий напрямок радіології?
Які інформаційні промені використовуються в системах візуалізації.
Назвіть сучасне трактування терміну "комп'ютерна томографія".
Визначте фізичний принцип дії рентгенівського комп'ютерного томографа.
Які три точки покладено в основу шкали Хаунсфілда?
Наведіть приклади третього покоління томографів.
Які інформаційні промені використовуються в МРТ?
Перерахуйте протипоказання до проведення МРТ.
Які інформаційні промені використовуються в ПЕТ?
Який із трьох методів КТ найбезпечніший для людини?
Назвіть етапи процесу обробки інформації при УЗД.
Назвіть галузі застосування УЗД.
Для самостійного вивчення
Системи дозиметричного планування. Системи дозиметричного планування (СДП) належать до спеціальних інформаційних систем, що працюють у променевій терапії. Призначення систем — планування променевого навантаження на пацієнта при проведенні променевої терапії. При цьому здійснюється прогнозування результатів лікування після моделювання того радіаційного поля, впливу якого зазнаватиме пацієнт. СДП застосовують в Україні з кінця 80-х років XX століття. Для кращого розуміння роботи СДП слід на понятійному рівні розібрати суть променевої терапії.
Онкологічні захворювання — одна з найактуальніших проблем у світовій охороні здоров'я. У середньому близько 70 % онкологічних хворих проходять курс променевої терапії. Іонізуючий вплив на злоякісні новоутворення є одним із найефективніших терапевтичних методів. В основі такого лікування лежить процес опромінення ракової пухлини різними за своєю фізичною природою видами випромінювання: електронним, позитронним, нейтронним, фотонним, рентгенівським. Частинки високих енергій руйнують ракові клітини пухлини і пригнічують їхнє відтворення. Підхід "чим вища доза випромінювання, тим краще" у променевій терапії онкологічних захворювань абсолютно неприйнятний. Наприклад, відповідно до медичних норм оптимальним є променеве навантаження 70 Гр. При меншому навантаженні частина ракових клітин залишиться живою, при більшому народжуються нові клітини-мутанти, резистентні до випромінювання. І при цьому вони зберігають здатність розмножуватися. Розподіл дози іонізуючого випромінювання в тканинах і органах пацієнтів підпорядковується складним фізичним законам. Високі дози шкідливі, низькі не ефективні. Це завдання потрібно вирішувати щоразу, в індивідуальному порядку.
Друге завдання пов'язане з першим: оскільки чітка межа безпеки між здоровими тканинами прилеглих органів та опромінюваною мішенню відсутня, то виникає проблема ураження здорових тканин, що може загрожувати здоров'ю і життю пацієнта. Ідеальної дози, здатної стерилізувати пухлину без ураження здорової тканини, не існує. На цьому етапі вводиться поняття про оптимальну дозу, тобто дозу, що дає максимум шансів зруйнувати пухлину і мінімальний ризик розвитку ускладнень. Потрібний точний розрахунок променевих навантажень на прилеглі здорові органи. До появи СДП такий розрахунок вівся вручну за допомогою ізодозних прозорих карт. З погляду фізики, людина — це насамперед багатошарова система, що складається з великої кількості різнорідних тканин, які неоднаково поглинають випромінювання.
Таким чином, при плануванні променевої терапії необхідно:
застосувати однорідну дозу на весь опромінюваний об'єкт, наскільки це можливо, щоб уникнути як передозування, так і недостатньої дози порівняно з оптимальною;
знайти такий технічний спосіб опромінення, що дав би змогу обмежити вплив опромінення (застосовувати найнижчу дозу) на здорові тканини;
точно оцінити дози, які застосовують при опроміненні різних ділянок тіла, і впевнитися, що жоден орган не зазнає впливу небезпечної для нього дози.
Для вирішення таких завдань у комп'ютер СДП уводять дані:
ЛПЗ, прізвище хворого, вік тощо;
вихідну дозиметричну інформацію про радіоактивне джерело, що міститься в апараті. Комп'ютер коригуватиме вихідну потужність дози з урахуванням розпаду радіоактивного джерела;
контури тіла пацієнта, мішені (ділянки, що зазнає опромінення), внутрішніх органів уводяться вручну з рентгенівських знімків або шляхом "скачування" томограми з комп'ютерного томографа;
розміри полів опромінення — розміри мішені (пухлина, лімфовузли, доопераційне поле, післяопераційне поле) Таку інформацію, як було зазначено, безпосередньо одержують із даних томографічних досліджень локалізації пухлин;
щільність тканин, що зазнають опромінення. У такті спосіб буде враховано їхню неоднорідність (гетерогенність), не однакову їх "прозорість" для опромінення;
режим опромінення (ротація, один зі статичних, комбінований).
Таким чином, скласти індивідуальний план опроміненення можна на основі введених у комп'ютер трьох вузлових 11 метрів, які є вихідними точками обробки даних: анатомічних даних (п. 3,4), точного опису джерела опромінення (п. 2) і обраного режиму променевих процедур (п. 6).
Після цього запускається програма на виконання і на екрані монітора системи поверх уведеного контуру (п. 3) з'являються лінії замкнутих кривих — ізодозні лінії, що показують кількісний розподіл дози у відсотках по всьому контуру. Саме на цьому етапі на екрані монітора можна побачити будь-яку ділянку, що опромінюється. Якщо здорові тканини потрапляють у зону високої дози опромінення, на що вказує карта ізодоз, то такий варіант лікування відкидається і в комп'ютер СДП уводять інші дані (змінюють режими опромінення). Цей процес здійснюють кілька разів, поки не буде обрано найкращі умови і модель поля прогнозуватиме терапевтичний ефект із найменшими ускладненнями. Окрім графічного зображення поля СДП розраховує дози, оцінює дозовий розподіл у тканинах і задає оптимальні параметри сеансу опромінення. Отриманий у вигляді сукупності ізоліній (ізодоз) розподіл доз наносять на топометричну карту і використовують для визначення таких параметрів опромінення, як разова поглинена доза, час опромінення, розмір поля опромінення, розташування точки центрації осей пучків випромінювання. Таким чином, перебираючи різні варіанти моделей поля, обирають найкращий варіант променевої терапії в кожному конкретному випадку.
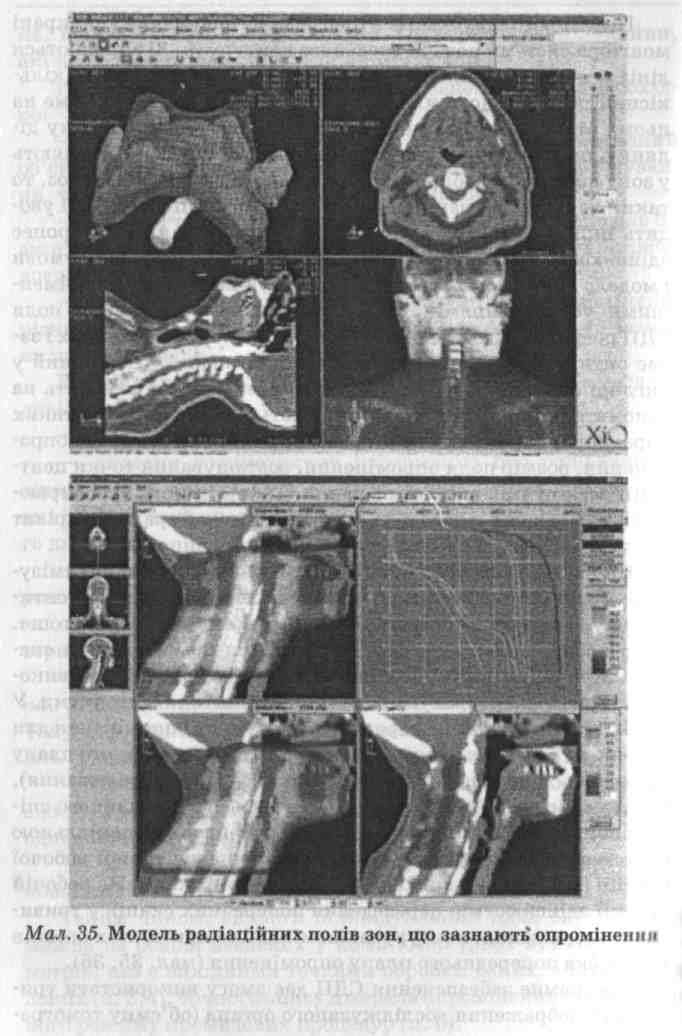
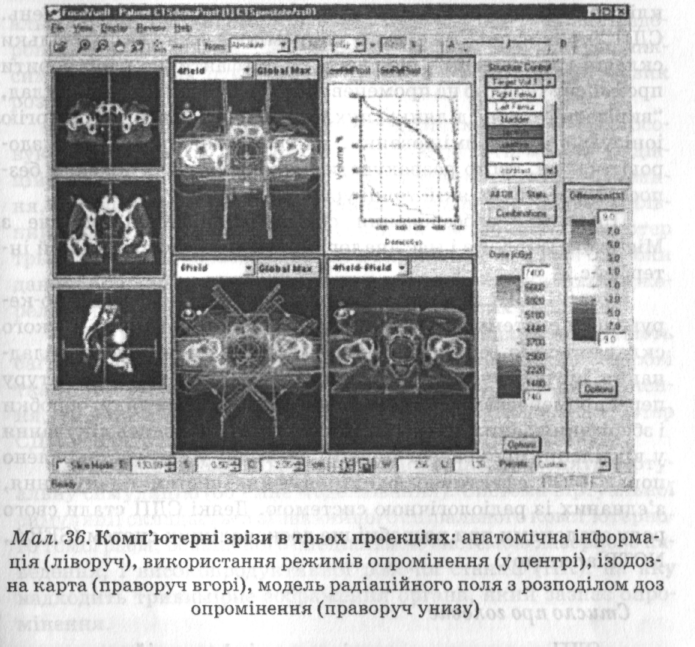
На сьогодні створено такі СДП, які самостійно оптимізують, моделюють об'ємне радіаційне поле, розраховують оптимальну дозу опромінення за заданим об'ємом пухлини тощо. Така робота неможлива без застосування комп'ютерних систем, які працюють на високопродуктивних процесорах і використовують для розрахунку складні математичні алгоритми. У СДП останніх поколінь перед початком курсу опромінення для перевірки адекватності вже отриманого дозиметричного плану проводиться віртуальна симуляція (об'ємне моделювання). Система віртуальної симуляції складається зі звичайного спірального комп'ютерного томографа, оснащеного спеціальною системою лазерного наведення, і високопродуктивної робочої станції (ПК), на яку надходять комп'ютерні скани. На робочій станції здійснюється переведення поперечних сканів у тривимірне зображення, контурування мішені та критичних органів і розробка попереднього плану опромінення (мал. 35, 36).
Програмне забезпечення СДП дає змогу використати тривимірне зображення досліджуваного органа (об'ємну томограму), му), переглянути його і зробити розріз у будь-якій площині. Лікар може вибрати точку на цій моделі в середині пухлини і дати завдання комп'ютерній системі розрахувати кількість енергії, яку потрібно підвести конкретно в цю зону.
СПД оснащено потужними робочими станціями — сучасними комп'ютерами, які дають змогу лікарю-радіотерапевту проводити віртуальну КТ-симуляцію будь-яких процедур дистанційного опромінення і здійснювати передпроменеву розмітку тіла пацієнта, а так само миттєво відтворювати відхилення дози від запланованого значення.
Сучасні СДП ґрунтуються на найширшому застосуванні новітніх комп'ютерних та інформаційних технології і забезпечують прямий доступ через Internet до серверів провідних клінік Європи і США для одержання медичних зображень. СДП "прив'язані" до систем випромінювання, які настільки складні і "витончені", що дають змогу фактично перетворити променеву терапію на променеву хірургію. Можна, наприклад, "вирізати" певну ділянку пухлини і передати в неї енергію іонізуючого випромінювання, мало зачепивши прилеглі здорові тканин, тобто розрахувати променеві навантаження безпосередньо в будь-якій точці ураженого органа.
Програмне забезпечення систем планування сумісне з Microsoft Windows і має аналогічний користувальницький інтерфейс.
Сучасні СДП інтегровані в радіологічну інформаційно-керувальну систему ЛПЗ, медична інформаційна система якого складається із серверів, робочих станцій, мережевого обладнання, що поєднує всю опромінювальну апаратуру й апаратуру передпроменевої підготовки для введення, перегляду, обробки і зберігання даних про всіх пацієнтів, які проходять лікування у відділенні променевої терапії. Сьогодні у світі встановлено понад 1400 ефективно функціонуючих систем планування, з'єднаних із радіологічною системою. Деякі СДП стали свого роду еталонами при розробці ще досконаліших систем (SERA, NCTPlan тощо).
Стисло про головне
СДП належать до спеціальних інформаційних систем, які застосовуються у променевій терапії. Призначення систем — планування променевого навантаження на пацієнта при проведенні променевої терапії.
В основі променевої терапії лежить процес опромінення ракової пухлини різними за своєю фізичною природою видами випромінювання. Частинки високих енергій руйнують раком і клітини пухлини і пригнічують їхнє відтворення. При цьому у зв'язку з розбіжністю іонізуючого променя частина енергії потрапляє на прилеглі здорові органи, чинячи на них негативний вплив.
Розподіл дози іонізуючого випромінювання в тканинах і органах пацієнтів підпорядковується складним фізичним законам. Високі дози — шкідливі, низькі — не ефективні. Ідеальної дози, здатної стерилізувати пухлину без ураження здорової тканини, не існує. Уводять оптимальну дозу, що дає максимум шансів на руйнування пухлини і мінімальний ризик розвитку ускладнень.
У процесі передпроменевої підготовки хворого застосовують СДП, які дають можливість побудувати модель радіаційного поля, заздалегідь спрогнозувати результати лікування, підібрати оптимальний варіант опромінення. Індивідуальний план опромінення ґрунтується на уведених у комп'ютер трьох вузлових параметрах, які є вихідними точками обробки даних: анатомічна інформація про пацієнта, точний опис джерела опромінення і обраний режим променевих процедур.
СДП моделюють процес опромінення, дають можливість багаторазово переглядати їхні різні варіанти. Якщо здорові тканини потрапляють у зону впливу високої дози опромінення, то такий варіант лікування відкидається і в комп'ютер СДП уводять інші дані (змінюють режими опромінення).
За допомогою СДП останніх поколінь проводять віртуальну симуляцію (об'ємне моделювання). Система віртуальної симуляції складається зі звичайного спірального комп'ютерного томографа, оснащеного спеціальною системою лазерного наведення, і високопродуктивної робочої станції (ПК), на яку надходить тривимірне зображення органа, який зазнає опромінення.
Контрольні питання
У якій сфері застосовують СДП?
Перерахуйте основні завдання, які вирішують СДП.
Які медичні дані вводять у СДП для вирішення її завдань?
У який спосіб можна ввести анатомічну інформацію І систему?
Назвіть особливості СДП останніх поколінь
