
ОБМІН ЛІПІДІВ
Ліпідами називають неоднорідні в хімічному відношенні речовини, загальною властивістю яких є добра розчинність у неполярних органічних розчинниках: ефірі, бензині, хлороформі, ацетоні, метиловому та етиловому спиртах тощо. За своєю хімічною будовою ліпіди, у більшості випадків, - це складні ефіри вищих жирних кислот з гліцерином чи якимись іншими спиртами специфічної будови. У складі ліпідів, крім цих компонентів, зустрічаються фосфорна кислота, азотисті основи або вуглеводи.
Функції цього класу сполук важливі і різноманітні. Насамперед, ліпіди у комплексі з білками є структурними елементами мембран клітин і клітинних органел. У зв'язку з цим вони визначають транспорт речовин у клітини і беруть участь у ряді інших процесів, що зв'язані з функціонуванням мембран.
Ліпіди є енергетичним матеріалом для організму людини. При окисненні 1 г жиру виділяється до 9 ккал (до 39 кДж) енергії, тобто у 2 рази більше, ніж при розщепленні 1 г вуглеводів. За рахунок жирів раціону забезпечується в середньому 25-35% енергії, необхідної людині на добу. Одночасно ліпіди є запасними речовинами, у формі яких депонується метаболічне паливо. Ліпіди виконують і захисну функцію. У вигляді жирової прокладки захищають тіло й органи людини від механічного пошкодження, служать жировим мастилом для шкіри. Деякі із ліпідів мають відношення до імунітету (гліколіпіди). Регуляторну активність мають простагландини, тромбоксани і лейкотрієни.
Прямим доведенням наявності на поверхні клітини спеціального морфологічного утворення - плазматичної мембрани стали безпосередні електронно-мікроскопічні дослідження, які встановили також тришарову структуру всіх клітинних мембран, що відповідає внутрішньому ліпідному шару, вкритому ззовні та зсередини білковими молекулами.
Функції біомембран:
а)відмежовування внутрішньоклітинного простору від навколишнього хімічного середовища за рахунок вибіркової проникності плазматичних мембран для іонів та молекул;
б)створення та підтримання на плазматичній мембрані іонних градієнтів та електричних потенціалів;
в)регуляція клітинних функцій біорегуляторними хімічними сигналами, що надходять від нервової та ендокринної систем;
г)поділ клітини на окремі компартменти,що характеризуються специфічними наборами ферментів, метаболітів та реакцій обміну речовин;
д)створення структурних, біофізичних умов для організації мембранозв'язаних мультиферментних комплексів (ферментних ансамблів), які реалізують життєво важливіклітинні функції (наприклад, електронтранспортних ланцюгів у мембранах мітохондрій та ендоплазматичного ретикулуму, функціонування іонних каналів та насосів);
є) участь у процесах міжклітинної взаємодії як необхідного фактора регуляції клітинного росту, створення тканин (гістогенезу).
Мембранні структури тваринної клітини:
плазматична мембрана;
мембрани ендоплазматичного (саркоплазматичного) ретикулуму;
мітохондріальні мембрани;
ядерна мембрана;
мембрани комплексу Гольджі;
мембрани лізосом та фагосом;
мембрани пероксисом (мікротілець).
Молекулярні компоненти біомембран
Головними хімічними компонентами біологічних мембран є білки, ліпіди та вуглеводи. Співвідношення між вказаними біохімічними компонентами значно відрізняється в окремих типах біомембран і залежить від їх функціональної та біохімічної спеціалізації.
Як свідчать дані, вміст білків у клітинних мембранах становить у середньому 50-75 %, ліпідів - 25-45 %, вуглеводів - 0-10 %. Для зовнішніх клітинних (плазматичних) мембран притаманна наявність певної кількості вуглеводів, що входять до складу гліколіпідів та глікопротеїнів, для мієлінових мембран мозку - значна концентрація ліпідів. Внутрішні (субклітинні) мембрани мітохондрій, ендоплазматичного ретикулуму містять відносно більшу кількість білків, що відображує наявність у цих мембранних структурах важливих мультиферментних комплексів.
Ліпіди мембран. Ліпідні компоненти біологічних мембран представлені переважно різними класами полярних ліпідів: фосфоліпідами (фосфатидилхоліном, фосфатидилетаноламіном, фосфатидилсерином, сфінгомієліном) - до 80-90 % загального вмісту мембранних ліпідів; гліколіпідами (переважно глікосфінголіпідами). Зовнішня плазматична мембрана характеризується значним вмістом вільного холестеролу та його ефірів і наявністю гліколіпідів, які відсутні в інших мембранних структурах.
Особливістю структурної організації молекул ліпідів, що входять до складу біологічних мембран - фосфоліпідів та гліколіпідів - є наявність у них гідрофільної "головки ", що утворена залишком фосфату, етерифікованим полярними або зарядженими групами, та гідрофобних "хвостиків", які утворені ацилами насичених та ненасичених жирних кислот (С16, С18, С20 тощо).
Молекула холестеролу входить до складу біомембран також завдяки наявності в її структурі гідрофобної частини (поліциклічний вуглеводень циклопентанпергідрофенантрен) та гідрофільної - ОН-групи.
Білки мембран. Білки біологічних мембран - це, переважно: ферменти; білки іонних каналів та інших систем мембранного транспорту; рецепторні білки, що зв'язують зовнішні ліганди та беруть участь у трансформації хімічного сигналу в біологічну реакцію клітини.
Певна кількість мембранних білків зв'язана з вуглеводами (глікозильована) у вигляді глікопротеїнів.
За характером розташування у мембрані білки поділяють на зовнішні (периферичні, поверхневі) та внутрішні. Зв'язок білків із різними мембранними структурами буде розглянуто нижче.
Вуглеводи мембран. Вуглеводи в складі біологічних мембран зв'язані з іншими хімічними компонентами мембрани у вигляді гліколіпідів та глікопротеїнів.
Гліколіпіди мембран є, головним чином, похідними сфінгозину (глікосфінголіпіди, або глікоцераміди).
Глікопротеїни мембран є молекулярними структурами, що утворюються за рахунок ковалентних зв'язків олігосахаридних ланцюгів з мембранними білками. Ці зв'язки формуються за участю гідроксильних груп серину або треоніну (О-глікозидні зв 'язки) та амідної групи аспарагіну (N-глікозидний зв'язок).
Мономерними залишками у складі олігосахаридних ланцюгів мембранних гліколіпідів та глікопротеїнів є такі моносахариди та їх похідні: галактоза, глюкоза, фруктоза, маноза, галактозамін, глюкозамін, нейрамінова та сіалова кислоти.
Гліколіпіди та глікопротеїни входять до складу, як правило, плазматичної мембрани клітини, контактуючи із зовнішньоклітинним оточенням та міжклітинним матриксом. Олігосахаридні залишки виконують функції лігандів для зовнішніх білків, тобто забезпечують процес розпізнавання та міжклітинної взаємодії, особливо важливі в реакціях клітинного імунітету. Аномальні зміни структури поверхневих гангліозидів у мембранах пухлинних клітин призводять до втрати характерного для росту нормальних клітинних пластів феномену "контактного гальмування", що супроводжується притаманним злоякісним пухлинам інфільтративним ростом.
Молекулярна організація біомембран. Наявність у мембранних ліпідах (гліцерофосфоліпідах, сфінгофосфоліпідах, гліколіпідах) полярних головок та неполярних гідрофобних структур (вуглеводневих радикалів жирних кислот та сфінгозину) визначає їх амфіфільну (амфіпатичну) природу, тобто здатність до взаємодії як з гідрофільними (полярними), так і з гідрофобними (неполярними) молекулами.
Завдяки амфіфільній будові молекул, ліпіди, що беруть участь у побудові біомембран, здатні до утворення в полярних середовищах упорядкованих структур: міцел, моношарових та бішарових плівок (моношарів та бішарів).
а) Міцели - молекулярні структури, які амфіфільні ліпіди утворюють у водному (полярному) оточенні. У міцелах вуглеводневі хвости ліпідів вкриті від контакту з водою та утворюють гідрофобну фазу, а гідрофільні головки молекул розташовуються на поверхні. Міцелярні структури характерні для ліпопротеїнів крові та для ліпідних комплексів, що всмоктуються в кишковому тракті.
б) Мономолекулярні шари - плівки, які амфіфільні ліпіди утворюють на поверхні водних розчинів. У мономолекулярних шарах гідрофільні головки молекул взаємодіють з водною фазою, а вуглеводневі хвости спрямовані до повітряної фази. Мономолекулярний шар, що утворює в легеневих альвеолах фосфогліцерид дипальмітоїлфосфатидилхолін, виконує функцію легеневого сурфактанту, який протидіє злипанню легеневих альвеол.
в) Бімолекулярні шари - молекулярні структури, в яких вуглеводневі хвости ліпідів спрямовані всередину, утворюючи неперервний вуглеводневий бішар, а гідрофільні (полярні) головки направлені в бік водної фази, що оточує бімолекулярну плівку, яка утворилася; бімолекулярні шари є основою будови біологічних мембран.
Амфіфільний характер мембранних ліпідів є фізико-хімічною властивістю, що зумовлює їх здатність до утворення ліпідних бішарів, які складають основу молекулярної структури біологічних мембран.
Рідинно-мозаїчна модель будови біомембрани
Вперше припущення про те, що основу молекулярної організації біомембран складає подвійний ліпідний шар (бішар), було висунуте в 1925 р. Гортером та Гренделем (Е. Gorter, F. Grendel). У 1935 p. Даніелі та Даусон (J. F. Danielli, H. Dawson) запропонували модель, згідно з якої біологічні мембрани складаються з подвійного шару ліпідів, який вкрито із зовнішнього та внутрішнього боку шарами білків - "бутербродна"модель.
М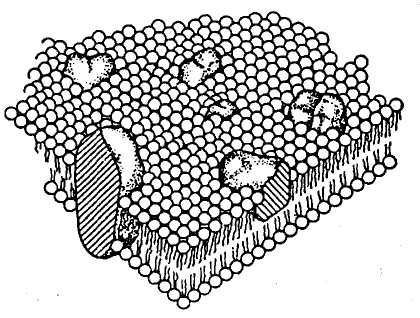 одифікація
моделі Даніелі -Даусона (модель Стейна
– Даніелі, 1956) постулювала наявність у
біомембранах полярних пор, придатних
для трансмембранного переносу гідрофільних
молекул.
одифікація
моделі Даніелі -Даусона (модель Стейна
– Даніелі, 1956) постулювала наявність у
біомембранах полярних пор, придатних
для трансмембранного переносу гідрофільних
молекул.
Згідно з сучасною рідинно-мозаїчною моделлю, основу (безперервний матрикс) біологічної мембрани складає полярний ліпідний бішар, в який занурені окремі білкові молекули.
За умов нормальних фізіологічних температур ліпіди біомембран знаходяться в рідкому стані, являючи собою "ліпідне озеро", в якому плавають, подібно до айсбергів, мембранні білки.
За своєю локалізацією відносно інших компонентів біомембрани мембранні білки поділяються на такі типи:
а)поверхневі (периферичні) білки;
б)білки, що частково занурені у бішар;
в)внутрішні (інтегральні) білки.
Біофізичні властивості мембран
1. Плинність та в'язкість ліпідної фази, що визначається співвідношенням між ненасиченими (рідкими) та насиченими (твердими) жирними кислотами у складі мембранних ліпідів та постійною рухомістю вуглеводневих хвостів ацилів та сфінгозину (подібно до "корзини із живими зміями").
Холестерол, що входить до складу біомембран, виконує важливу функцію модифікатора фізико-хімічних властивостей ліпідного бішару, стабілізуючи його шляхом обмеження рухомості внутрішньомембранних компонентів, тобто зменшуючи плинність та збільшуючи в'язкість матриксу мембранних ліпідів.
Рухомість окремих молекулярних компонентів мембрани — ліпідів та білків.
Ліпіди біомембран мають певну впорядкованість, але разом з тим вони здатні до латеральної дифузії, тобто переміщення впродовж рідинної ліпідної фази (рідинно-кристалічний стан мембранних ліпідів).
До латеральної дифузії здатні також молекули мембранних білків, що сприяє утворенню внутрішньомембранних білок-білкових ансамблів (кластерів). Важливим прикладом фізіологічного значення кластероутворення білків у площині біологічної мембрани є "шапкоутворення" (capping) мембранних рецепторів лімфоцитів при дії на клітину чужорідних лігандів.
Особливості травлення ліпідів
Травлення ліпідів проходить у тих відділах травного тракту, де є необхідні умови: 1) наявність ліполітичних ферментів, які гідролізують ліпіди; 2) умови для емульгування ліпідів; 3) оптимальне рН середовища для дії ліполітичних ферментів (середовище повинно бути нейтральним або слабколужним).
Такі умови створюються в кишечнику дорослої людини. У дитини, особливо немовляти, близькі умови створюються для травлення триацилгліцеринів молока шлунковою ліпазою, рН середовища шлункового вмісту дитини біля 5,0 (слабкокисле середовище), жир молока знаходиться у вигляді емульсії, тому можливе часткове розщеплення жиру ліпазою. У дорослої людини сильнокисле середовище інактивує шлункову ліпазу.
Після того як хімус попадає у дванадцятипалу кишку, проходить нейтралізація соляної кислоти шлункового соку бікарбонатами, які містяться в панкреатичному та кишечному соках. Одночасно проходить емульгування жиру під дією жовчних кислот, які надходять у кишечник у складі жовчі. У жовчі містяться переважно такі жовчні кислоти – холева, хенодезоксихолева та їх кон'югати з гліцином і таурином – глікохолева і таурохенодезоксихолева. Жовчні кислоти виконують такі біологічні функції: 1) емульгуючу; 2) активатора ліполітичних ферментів; 3) транспортну (утворюючи з вищими жирними кислотами транспортний комплекс, сприяють їх всмоктуванню в кишечнику).
Всі жовчні кислоти є амфіфільними сполуками, тобто мають властивості емульгаторів. Розміщуючись на поверхні розподілу двох фаз жир-вода, жовчні кислоти запобігають їх розшаруванню. Перистальтика кишечника допомогає подрібненню великих крапель жиру, а жовчні кислоти зберігають їх у суспендованому стані, запобігаючи злиттю дрібних жирових крапель. Додатковими емульгаторами є вільні жирні кислоти, а також утворені на їх основі мила, моноацилгліцерини, які утворюються у ході травлення ліпідів, фосфоліпіди їжі та продукти їх часткового травлення (фосфохолін).
Гідроліз триацилгліцеринів, які складають основну масу ліпідів їжі, проходить за схемою, що представлена на рис. 1

Рис. 1. Гідроліз тригліцеридів:
1 - триацилгліцеролліпаза [КФ 3.1.1.3]; 2 - діацилгліцеролліпаза [КФ 3.1.1.34]; 3 - моноацилгліцеролліпаза [КФ 3.1.1.23].
Гідроліз фосфоліпідів здійснюється групою ліполітичних ферментів, які називають фосфоліпазами. Існує декілька типів фосфоліпаз, які позначають як А1, А2, С і D. Вони гідролізують різні зв'язки у молекулі фосфоліпідів.
Гідроліз сфінгофосфатидів і цераміду проходить за рахунок сфінгомієлінфосфодіестерази [КФ 3.1.4.12] кишечника. Eфіри холестерину, які надходять з їжею, розщеплюються панкреатичною холестеролестеразою [КФ 3.1.1.13].
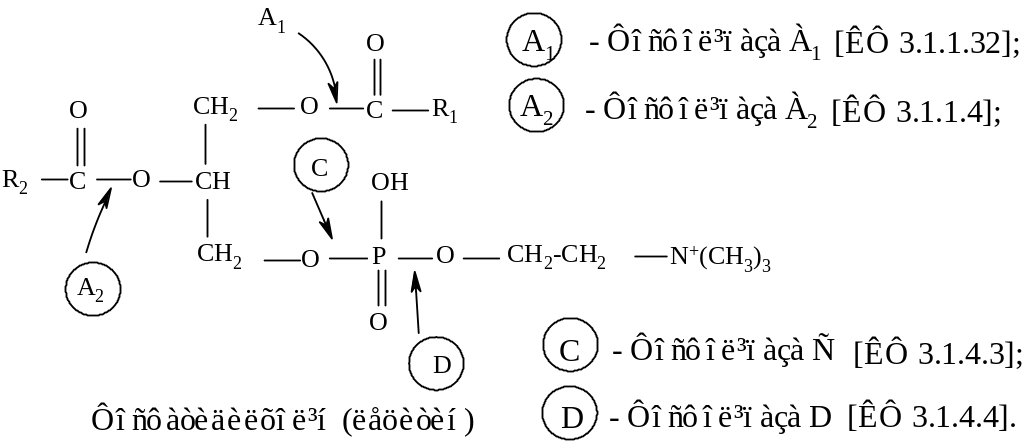
Місце дії фосфоліпаз на ефірні зв’язки фосфоліпідів.
Всмоктування продуктів гідролізу ліпідів
Всмоктування продуктів травлення ліпідів має свої особливості. Так, всмоктування жирних кислот залежить від довжини вуглецевого ланцюга. Коротколанцюгові жирні кислоти (до 10 вуглецевих атомів) транспортуються простою дифузією всередину кишечного епітелію. Довголанцюгові жирні кислоти (більше 14 вуглецевих атомів) утворюють транспортні комплекси з жовчними кислотами. Ці комплекси називають холеїновими кислотами. У такому вигляді жирні кислоти проходять через мембрану кишечного епітелію. Вважається, що це полегшена дифузія, де роль переносника виконують жовчні кислоти. Всередині стінки кишечника холеїновий комплекс розпадається, і жовчні кислоти переходять у кров ворітної вени і далі – в печінку. Із печінки вони знову надходять з жовчю і повертаються до кишечника. Цей кругообіг називають кишечно-печінковою циркуляцією жовчних кислот.
Частково ліпіди всмоктуються у вигляді триацилгліцеринів (біля 3-6%) шляхом піноцитозу і значна частина (до 50%) – у вигляді 2-моноацилгліцерину. Останні переходять мембранний бар'єр шляхом простої дифузії. Крім того, легко всмоктуються гліцерин, фосфати у вигляді натрієвих і калієвих солей, холін та інші спирти, сфінгозин і холестерин. Частина продуктів неповного гідролізу фосфоліпідів, наприклад, фосфохолін, також всмоктуються в кишечнику. Особливості їх транспорту ще не вияснені, хоча доведено, що частково вони всмоктуються шляхом простої дифузії, а для деяких з них виявлені переносники.
Продукти травлення ліпідів, які надійшли у слизову кишечника в результаті всмоктування, транспортуються у кров і лімфу. Такі продукти гідролізу ліпідів, як коротколанцюгові жирні кислоти, гліцерин, фосфати, холін та інші спирти добре розчинні у воді і надходять із слизової кишечника до ворітної вени і далі – в печінку. Деяка частина продуктів неповного гідролізу фосфоліпідів (гліцерофосфохолін, гліцеролфосфат), які всмокталися в кишечнику, також виявляються у крові ворітної вени.
Довголанцюгові жирні кислоти, холестерин, деякі триацилгліцерини, моноацилгліцерини і більша частина гідролізованих фосфоліпідів виявляються у лімфі. Проте, перш ніж надійти до лімфи, в епітеліальних клітинах (ентероцитах слизової оболонки ворсинок тонкої кишки) ліпіди піддаються ресинтезу (синтезу заново).
Метаболізм транспортних форм ліпідів
Ліпіди не розчинні у воді і тому транспортуються плазмою крові у вигляді комплексів з білками, які називаються транспортними формами ліпідів. Розрізняють 5 основних класів транспортних форм ліпідів, які характеризують і називають за 1) їх розділенням методом ультрацентрифугування (хіломікрони, ліпопротеїни дуже низької щільності (ЛПДНЩ), ліпопротеїни проміжної щільності (ЛППЩ), ліпопротеїни низької щільності (ЛПНЩ), ліпопротеїни високої щільності (ЛПСЩ)); 2) ідентифікацією методом імуноелектрофорезу – омега-ліпопротеїни, пре-бета-ліпопротеїни (ЛПДНЩ), проміжні між бета і пре-бета-ліпопротеїни, бета-ліпопротеїни (ЛПНЩ), альфа-ліпопротеїни (ЛПВЩ).
Транспортні форми ліпідів різняться своїми розмірами, складом і функціями. Найбільшими за розмірами є хіломікрони та ЛПДНЩ. Вони містять основну масу ліпідів і незначну кількість білків. ЛПВЩ – це найменші частки з високим вмістом білків і меншим вмістом ліпідів.
Структура всіх ліпопротеїнів подібна. Ліпопротеїни складаються з гідрофобного ядра, представленого неполярними ліпідами (триацилгліцеролами та ефірами холестерину) та зовнішнього шару, в який входять апобілки, холестерин, фосфоліпіди.
Білкова частина ліпопротеїнів називається аполіпопротеїном (апобілком). Апобілки позначаються буквами латинського алфавіту, синтезуються в печінці або кишечнику і виконують різноманітні функції – активатора ферментів, місця приєднання до рецептора тощо. Розрізняють інтегральні (Апо-В) та периферійні апобілки (Апо-С). Для кожного класу ліпопротеїнів притаманні свої апобілки і місце їх синтезу визначає місце утворення даного ліпопротеїну. Так, основними апобілками ЛПВЩ є А-І і А-ІІ. Апобілок В-48 входить до складу хіломікронів і синтезується в кишечнику, а Апо-В-100 синтезується в печінці і є основним білком ЛПНЩ та ЛПДНЩ, синтезованих у печінці. Апобілки С (С-І, С-ІІ, С-ІІІ) – це невеликі поліпептиди, синтезуються в печінці і можуть вільно переходити від одних ліпопротеїнів до інших, тому є периферійними апобілками. Апобілок С-ІІ є важливим активатором позапечінкової ліпопротеїнліпази, апобілок А-І у складі ЛПВЩ є активатором фермента етерифікації холестерину. Апо-Е необхідний для розпізнання рецепторами гепатоцитів транспортних форм ліпідів. Апо-D – білок-переносник ефірів холестерину з одних транспортних форм на інші.

Клітини кишечнику та печінки синтезують емульговані ліпіди.
Хіломікрони утворюються в ентероцитах кишечника та гепатоцитах навіть при голодуванні і забезпечують транспорт триацилгліцеролів та ефірів холестерину через лімфатичну систему до різних тканин та печінки. Апобілок В синтезується рибосомами шорохуватого ендоплазматичного ретикулуму. У гладенькому ендоплазматичному ретикулумі він утворює ліпопротеїни з триацилгліцеролами, холестерином та його ефірами. У комплексі Гольджі ліпопротеїни збагачуються вуглеводними залишками. При злитті секреторної вакуолі з мембраною ентероцита відбувається зворотний піноцитоз - вивільнення хіломікронів з клітин кишечника у міжклітинний простір, які далі надходять у лімфатичні капіляри, а потім у кровоносну систему.
Аналогічно утворюються хіломікрони і ЛПДНЩ у гепатоцитах і вивільняються в кровоносну систему. Особливістю ЛПДНЩ та хіломікронів, синтезованих у печінці, є наявність апобілка В-100. Вже в кровоносному руслі до хіломікронів та ЛПДНЩ приєднуються апобілки С та Е, які постачаються ЛПВЩ, синтезованими в печінці.
Необхідним компонентом хіломікронів та ЛПДНЩ є апобілок В. При абеталіпопротеїнемії порушується синтез цього білка і відповідних ліпопротеїнів. У клітинах кишечника та печінки накопичуються “крапельки” ліпідів.
Катаболізм хіломікронів відбувається у плазмі крові за участі фермента ліпопротеїнліпази [КФ 3.1.1.34], яка прикріплена до стінок капілярів протеглікановими ланцюгами гепарансульфату. Кофакторами ліпопротеїнліпази є фосфоліпіди та апобілок С-ІІ, який міститься в хіломікронах та ЛПДНЩ і прикріплюється до ліпопротеїнів через фосфоліпіди. Під дією ферменту тригліцериди хіломікронів або ЛПДНЩ гідролізують до діацилгліцеролів, моноацилгліцеролів та гліцерину. Найбільш активна ліпопротеїнліпаза в капілярах жирової клітковини, серця, скелетних м’язів та молочної залози під час лактації. Так забезпечуються серце та жирова тканина жирними кислотами. Частина жирних кислот, які вивільняються при гідролізі, зв’язуються і транспортуються в плазмі крові альбуміном, а основна маса жирних кислот транспортується в тканини. У цитоплазмі клітин виявлені специфічні Z- білки, які зв’язують жирні кислоти.
Під дією ліпопротеїнліпази хіломікрони втрачають до 90% триацилгліцеролів та апобілок С (апо-Е залишається). Позбавлені тригліцеридів хіломікрони залишаються в кров’яному руслі як багаті на холестерин ліпопротеїни і називаються залишками хіломікронів (ремнантами). Залишки хіломікронів та ЛПДНЩ поглинаються клітинами печінки за участі специфічних рецепторів апобілка Е і гідролізуються лізосомальними ферментами. Частина ЛПДНЩ перетворюється на ЛППЩ, які, в свою чергу, перетворюються на ЛПНЩ. Апобілок В, специфічний для ЛПДНЩ, разом із залишками ліпопротеїнів переходить і зберігається в наступних транспортних формах.
Залишки хіломікронів, ЛПДНЩ та ЛПВЩ2 катаболізують у печінці за участі ліпази печінки, що вивільняється гепарином.
ЛПНЩ утворюються з ЛПДНЩ (частина може безпосередньо синтезуватися в печінці) і поглинаються печінкою, наднирниками, жировою тканиною тощо – клітинами, що мають рецептори до ЛПНЩ. Фібробласти, лімфоцити, клітини артерій тощо мають рецептори, специфічні до апобілка В-100 ЛПНЩ, тому їх деградація відбувається як в позапечінкових клітинах, так і в гепатоцитах.
Рецептори ЛПНЩ – це глікопротеїни, що складаються з 5-ти доменів, належать до родини рецепторів, які транспортують макромолекулу всередину клітини шляхом ендоцитозу. ЛПНЩ розпадаються в клітинах під дією лізосомальних ферментів (протеаз та кислих ліпаз). Холестерин та його похідні дифундують з лізосом і пригнічують активність ферментів його синтезу (3-окси-3-метилглутарил-КоА-редуктази) і стимулюють активність фермента внутрішньоклітинної етерифікації – ацил-КоА :холестеролацилтрансферази. Холестерол також пригнічує синтез рецепторів ЛПНЩ, чим обмежує їх поглинання клітиною. ЛПНЩ є транспортною формою холестеролу і транспортують його до клітин. У хворих на сімейну гіперхолестеринемію рецептори В-100 не функціонують. Існує пряма кореляція між вірогідністю виникнення коронарного атеросклерозу і концентрацією ЛПНЩ у сироватці крові.
ЛПВЩ синтезуються як у кишечнику, так і в печінці. Вони дископодібної форми і майже не містять ефірів холестерину. ЛПВЩ, що синтезуються в кишечнику, містять тільки Апо-А, а апобілки С і Е (синтезуються тільки в печінці) приєднують тільки після їх надходження у кров. ЛПВЩ є джерелом апобілків С і Е, які необхідні для метаболізму хіломікронів та ЛПДНЩ. ЛПВЩ містять специфічний фермент, що синтезується в печінці і забезпечує в організмі людини основний шлях утворення ефірів холестерину – лецитин: холестерол-ацилтрансферазу (ЛХАТ) та апобілок А-І, що є активатором ЛХАТ. Цей фермент у складі ЛПВЩ каталізує реакцію перенесення залишку жирної кислоти з другого положення фосфатидилхоліну на вільний холестерин (надходить з тканин) з утворенням ефіру холестерину, який переміщується у гідрофобну частину міцели і ЛПВЩ перетворюються на сферичні частки. ЛПВЩ транспортують ефіри холестерину за участі апобілка D на ліпопротеїни більш низької щильності – ЛПНЩ, ЛПДНЩ, хіломікрони, і, в кінцевому рахунку, - до печінки. З печінки холестерин екскретується в жовч, що і забезпечує зниження його рівня в плазмі крові. ЛПВЩ забезпечують транспорт холестерину з тканин до печінки і тому існує обернена залежність між вірогідністю виникнення коронарного атеросклерозу та концентрацією ЛПВЩ у сироватці крові.
