
Отчеты по лабораторным работам / лаба 1 / лаба1
.docЦель: Определение молярной массы эквивалента металла Al методом вытеснения водорода.
Теоретическая часть:
-
Эквивалент – это реальная или условная частица вещества, которая может замещать, присоединять, высвобождать, а также быть каким-либо образом равнозначной одному атому или иону водорода в кислотноосновных или ионообменных реакциях или одному электрону в окислительно-восстановительных реакциях.
-
Эквивалентная масса – это масса моля эквивалентов.
-
Закон эквивалентов: Вещества взаимодействуют друг с другом в эквивалентных соотношениях, т.е. эквивалент одного вещества взаимодействует с эквивалентом другого вещества, а моль одного вещества взаимодействует с молем другого вещества.
Э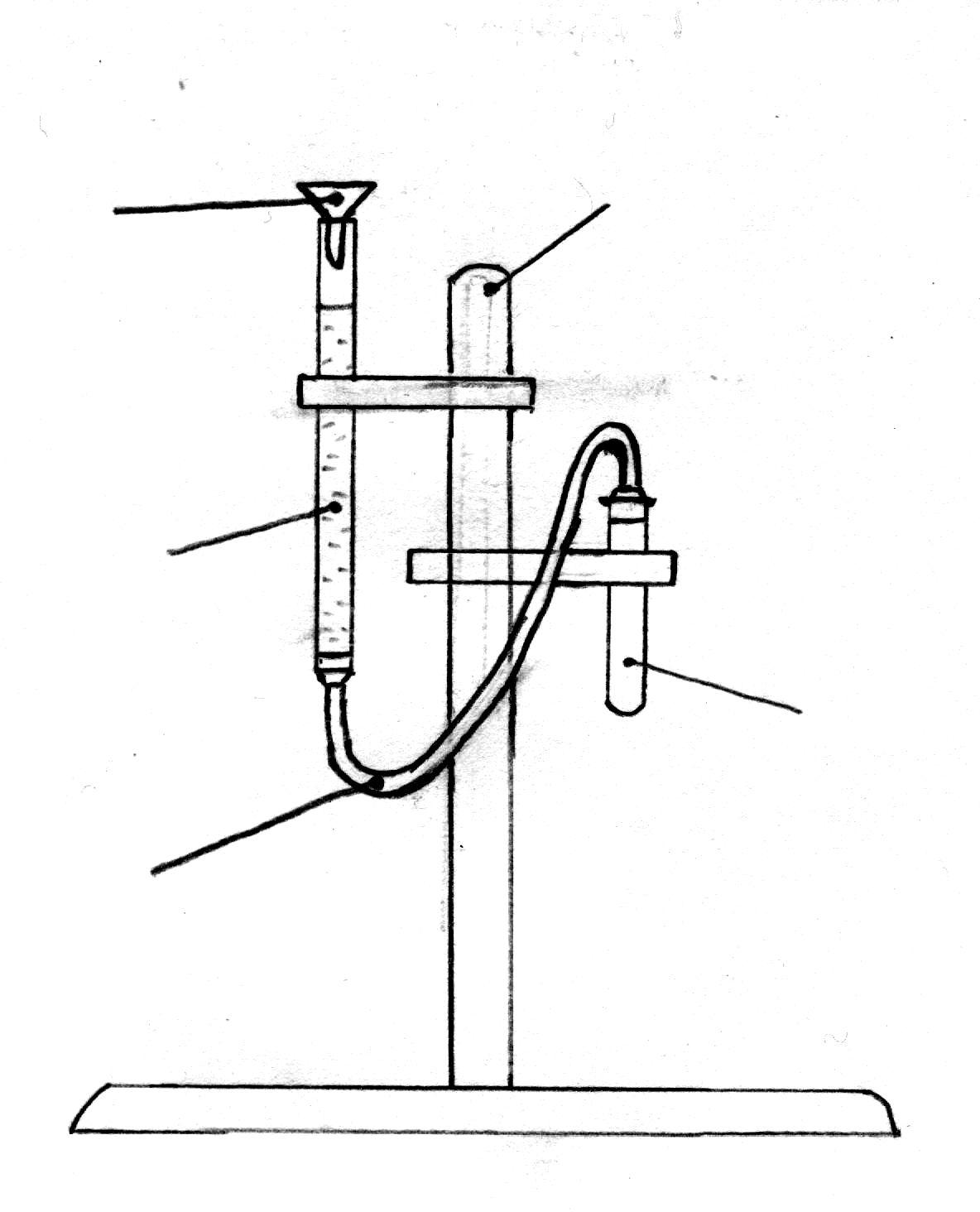 кспериментальная
часть:
кспериментальная
часть:
воронка штатив
беретка
пробирка
соединительная
трубка
Наливаем в пробирку кислоту, насыпаем туда металл, перемешиваем, определяем объем водорода выделившегося в результате реакции.
Экспериментальные данные:
t = 22º; T = 295K; p = 759 мм.рт.ст.; mAl = 0,0148 ; T0 = 273K;
p0 = 760 мм.рт.ст.; h = 19,827 мм.рт.ст. VH = 49 мл.
Расчет:
-
Приводим объем выделившегося водорода к нормальным условиям:
![]()
![]()
-
Определяем эквивалентную массу одного моля эквивалента водорода:
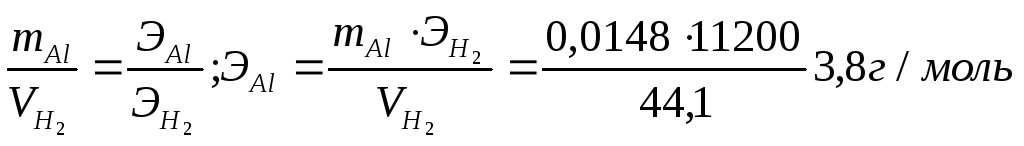 ;
;
-
Рассчитываем относительную и абсолютную ошибку эксперимента:

Вывод: Определена эквивалентная масса металла Al равная 3,8 г/моль, ошибка абсолютная равна 5,2 , ошибка относительная равна 57,7%.
