
Технология синтеза мономеров / Основы и технологии мономеров Платэ
.pdf221
В качестве побочных продуктов образуются 2- и 4-пиколины и ряд высококипящих пиридиновых оснований. Выделение метилэтилпиридина из реакционной смеси осуществляется ректификацией.
Дегидирование 2-метил-5-этилпиридина. Дегидрирование метилэтил-
пиридина в метилвинилпиридин является обратимой эндотермической реакци-
ей. Проведение |
реакции под вакуумом |
или в среде |
инертного |
раство- |
рителя смещает |
равновесие в сторону |
образования |
целевого |
продукта. |
Процесс проводят при 848-923 К в инертном носителе, в качестве которого чаще всего используют пары воды. Катализаторами реакции служат смешанные оксиды металлов, главными компонентами которых являются Fe2O3, ZnO, Mg2O3, Al2О3. В качестве промоторов применяют Cr2O3, K2CO3, KF, CaO. В этих условиях степень конверсии метилэтилпиридина составляет 35-70%, а выход метилвинилпиридина на прореагировавший алкилпиридин - 40-85%.
Поскольку селективность реакции сильно понижается с повышением конверсии метилэтилпиридина, то процесс дегидрирования желательно вести с глубиной превращения не выше 50%; тогда достигается сравнительно стабильный выход метилвинилпиридина – в интервале 70-80%. Ниже приведена зависимость селективности процесса дегидрирования метилэтилпиридина от температуры реакции.
|
Степень конверсии |
Выход |
Т, К |
2-метил-5-этилпиридина, |
5 винил-2 метилпиридина, |
|
% |
% |
863 |
29 |
80 |
883 |
38 |
76 |
903 |
49 |
73 |
Этот процесс отличается от процесса дегидрирования этилбензола при получении стирола тем, что гетероциклический метилэтилпиридин в условиях реакции является менее стабильным, чем аналогичное ароматическое соединение. Помимо деструкции пиридинового цикла и дегидрирования боковых цепей одновременно протекают реакции деалкилирования и алкилирования. В катализате обнаруживаются пиридин, 2- и 3-пиколины, 2,5-лутидин, 3-этилпиридин, 3-винилпиридин, 2,5-дивинилпиридин и другие. Наличие в катализате даже небольших количеств дивинилпиридина приводит к большим осложнениям в процессе выделения метилвинилпиридина ректификацией, так как эта примесь способствует образованию нерастворимого губчатого полимера в ректификационных колоннах.
Синтез 2- и 4-винилпиридинов и 2-винил-5-этилпиридина
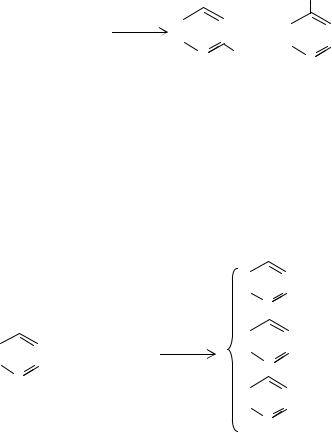
Исходными продуктами для получения этих мономеров по методу Ладенбурга являются соответственно 2- и 4-пиколины и метилэтилпиридин. Пи-
222
колины, так же, как и метилэтилпиридины получают конденсацией ацетальдегида с аммиаком. Реакцию проводят в газовой фазе над оксидными катализаторами, чаще всего над алюмосиликатом, при 648-723 К. В результате реакции образуются примерно в равном соотношении 2- и 4-пиколины с суммарным
выходом 50-60%: |
|
|
CH3 |
||||||
6CH3CHO + 2NH3 |
|
N |
|
CH3 |
+ |
|
N |
|
+ 6H2O + 2H2. |
|
|
|
|
||||||
|
|
|
|
|
|
|
|||
Побочными продуктами синтеза являются в основном 4-метил 3 этилпиридин, 4-метил-3-этилпиридин и другие высококипящие пиридиновые основания. Целевые продукты из реакционной смеси выделяют ректификацией.
Синтез винилпиридинов состоит из двух стадий: оксиметилирования метилпиридинов и дегидратации пиридилэтанолов.
Гидроксиметилирование метилпиридинов. Реакция формальдегида с метилпиридинами протекает крайне неселективно: наряду с пиридилэтанолом (монозамещенные производные пиколина) образуются ди- и три-замещенные пиколины:
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2CH2OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
N |
|
|
|
|
Пиридилэтанол |
||
n |
|
|
|
|
CH3 + n CH2O |
|
|
|
|
|
|
|
|
CH(CH2OH)2 |
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
N |
|
|
|
|
Диол |
||||
|
||||||||||||||
|
|
|
|
|||||||||||
|
|
N |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
C(CH2OH)3 |
|
|
|
|
|
|
|
|
N |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
Триол |
|||
Такой характер протекания реакции объясняется высокой подвижностью атомов водорода метильной группы пиколинов, приводящей к полному замещению их гидроксиметильными группами. Общим приемом повышения селективности этой реакции является проведения синтеза при низкой (по сравнению с концентрацией пиколина) концентрации формальдегида, т.е. при большом избытке пиколина.
Реакцию оксиметилирования алкилпиридинов проводят, как правило, в жидкой фазе в интервале температур 413-593 К под давлением инертного газа 2,0-17,0 МПа. В качестве формилирующего агента обычно используют формалин или параформ.
Дегидратация пиридилэтанолов. Дегидратации можно подвергать продукты реакции оксиметилирования, из которых предварительно выделен исходный алкилпиридин. Наиболее перспективным является вариант, при котором на дегидратацию можно подавать продукты реакции оксиметилирования без какой-либо предварительной обработки. Разработаны следующие способы дегидратации:
223
-дегидратация чистых пиридилэтанолов в присутствии щелочных катализаторов с селективностью 97-99%.
-дегидратация пиридилэтанолов в газовой фазе над твердыми катализаторами при температуре ~ 673 К над оксидом алюминия.
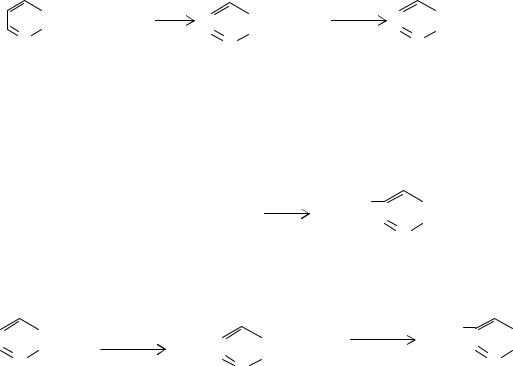
Получение 2-винилпиридина. 2 Винилпиридин получают альдольной конденсацией 2-алкилпиридина с формальдегидом с последующей дегидрата-
цией образовавшегося спирта:
|
|
CH3 |
+ CH2O |
|
|
H+ |
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
CH CH OH - H2O |
|
|
CH=CH2 |
||
N |
|
|
|
N |
|
||||
|
|
N |
|
||||||
|
|
|
2 2 |
|
|
||||
Получение 2-винил-5-этилпиридина.Процесс получения 2-винил-5
этилпиридина осуществляют в две стадии.
На первой стадии нагреванием паральдегида с избытком аммиака в жидкой фазе при 473-523 К и давлении 5,0 МПа в присутствии в качестве катализатора уксусной кислоты получают 2-метил-5-этилпиридин:
4CH3—CHO + NH3 |
-H2O |
C2H5 |
|
|
CH3 |
|
|
||||
|
|
|
|
||
|
|
N |
|
||
|
|
|
|
|
На второй стадии проводят конденсацию образовавшегося полупродукта с формальдегидом и получают 2-винил- 5- этилпиридин:
C H |
|
|
|
CH2O |
|
|
|
|
|
|
|
|
C2H5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
C2H5 |
|
|
|
|
|
|
|
|
|||||
2 |
5 |
|
|
CH3 |
|
|
|
|
|
|
|
-H2O |
|
|
|
CH=CH2 |
|
|
|
|
|
|
|
|
|
|
CH2CH2OH |
|
|
|
|||
|
|
N |
|
|
|
|
|
|
|
|
N |
|||||
|
|
|
|
|
|
|
N |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|||||||
6.3 N-ВИНИЛПИРРОЛИДОН
Поливинилпирролидон обладает целым комплексом интересных, а в некоторых отношениях уникальных, свойств, что позволяет использовать его в самых разнообразных областях. Однако основной областью его применения является медицина.
В зависимости от величины молекулярной массы поливинилпирролидон используют:
- для выведения токсических веществ из организма (полимер с низкой моле-
кулярной массой - ~ 10 000-15 000);
-в качестве основы плазмозаменяющих растворов (полимер со средней молекулярной массой – 25 000–40 000) при переливании крови;
-для пролонгирования действия лекарств (полимер с высокой молекулярной массой – ~ 60 000);
-в качестве энтеросорбента (в сшитой форме).
224
Винилпирролидон и его сополимеры широко применяют в текстильной промышленности, в производстве бумаги и фотоматериалов, в пищевой промышленности, сельском хозяйстве, строительной технике.
Впервые N-винилпирролидон синтезировали прямым винилированием - пирролидона ацетиленом. Позже были разработаны другие методы синтеза, основанные на реакциях отщепления (дегидрогалогенирование, дегидратация и т.д.) и замещения (перевинилирование). Наибольший интерес представляет метод винилирования ацетиленом, так как он используется и в лабораторной практике, и в промышленности. Методы синтеза путем перевинилирования имеют лишь лабораторное значение.
6.3.1. Прямое винилирование -пирролидона ацетиленом
Прямое винилирование -пирролидона ацетиленом осуществляют при 373-573 К и давлении 1,5-4 МПа. В этих условиях ацетилен способен разлагаться со взрывом:
C2Н2  2С+ Н2 Н = 226 кДж/моль.
2С+ Н2 Н = 226 кДж/моль.
При атмосферном давлении разложение происходит лишь при взрыве детонатора. В условиях реакции винилирования при высоком давлении энергия, необходимая для инициирования распада ацетилена, очень мала, что делает процесс взрывоопасным. В связи с этим для проведения реакции винилирования разработаны специальные технология и аппаратура. Одним из путей снижения взрывоопасности производства является разбавление ацетилена инертными газами, например азотом или парами реагирующих веществ. За рубежом процесс проводят, как правило, с применением ацетилено-азотных смесей. В России используется оригинальный метод винилирования, разработанный А.Е. Фаворским и М.Ф. Шостаковским, в котором разбавление ацетилена осуществлется парами винилируемого агента или образующегося винилового производного.
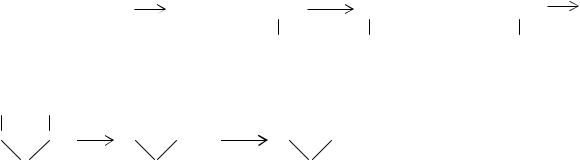
Процесс винилирования пирролидона практически состоит из пяти ста-
дий: |
|
|
|
|
|
|
|
|
|
|
|
|
H2 |
|
|
|
|||
2CH2O + HC CH |
|
|
|
|
CH2—C C—CH2 |
CH2—CH2—CH2—CH2 -H2 |
|||||||||||||
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
||||||||||||||||
Форм- |
Ацетилен |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
OH |
OH |
|
|
|
OH |
OH |
|||||||||||
альдегид |
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
Бутиндиол-1,4 |
|
|
|
|
Бутандиол-1,4 |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
CH2—CH2 |
|
|
|
CH2—CH2 |
|
CH2—CH2 |
|
|||||||||||
|
CH2 CO NH3 |
|
|
|
CH2 |
|
CO CH CH |
|
|
|
|
|
CO |
|
|
|
|||
|
|
|
|
|
|
|
|||||||||||||
|
|
|
CH2 |
|
|
|
|
||||||||||||
|
O |
|
|
|
|
NH |
|
|
N—CH=CH2 |
|
|||||||||
-Бутиролактон |
-Пирролидон |
N-Винилпирролидон |
|
||||||||||||||||
Бутиндиол-1,4 синтезируют, пропуская ацетилен и 30%-ный водный раствор формальдегида через колонну, содержащую ацетиленид меди, при 373 К и 0,5-
225
0,7 МПа. Полученный 35%-ный водный раствор бутиндиола-1,4 гидрируют под давлением 20 МПа на никелевом катализаторе. Образующийся бутандиол-1,4 дегидрируют с почти количественным выходом до -бутиролактона при 523 К в присутствии медного катализатора. -Бутиролактон нагревают с безводным аммиаком в автоклаве при 443-453 К и повышенном давлении. Винилирование - пирролидона проводят ацетиленом, разбавленным азотом, при температуре 373-378 К и давлении 1,5 МПа в присутствии катализаторов основного характера.
В качестве катализаторов используют оксиды и гидроксиды щелочных и щелочноземельных металлов, алкоголяты, соли лактамов, имидов, амидов. В присутствии даже небольших количеств воды процесс не идет. Для винилиро-
вания -пирролидона используют в качестве растворителя тетрагидрофуран, N- метилпирролидон, метилаль, диметоксиэтан, диоксан, диметиловый эфир тетраэтиленгликоля.
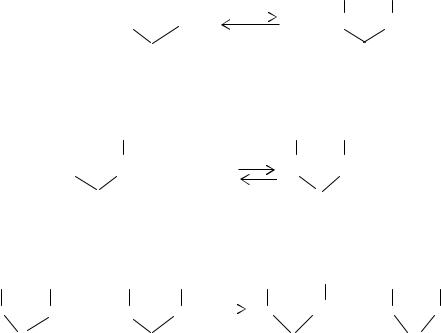
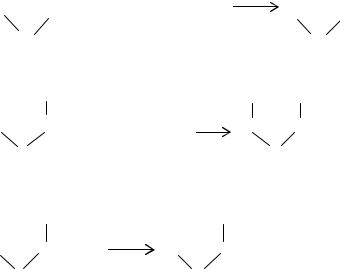
В присутствии щелочного катализатора реализуется следующий ионный механизм реакции:
CH2—CH2 |
CH2—CH2 |
||
|
|
|
Me+ + CH2 C=O |
CH2 C=O |
|||
|
NMe |
N- |
|
CH2—CH2 |
CH2—CH2 |
|
||
|
|
CH2 C=O + HC CH |
CH2 C=O |
(Медленно) |
|
||||
|
|
N- |
NCH=CH- |
|
СH2—CH2 |
CH2—CH2 |
CH2—CH |
2 |
CH2—CH2 |
|
СH2 |
C=O |
+ CH2 C=O |
CH2 C=O + |
CH2 C=O (Быстро) |
|
NCH=CH- |
NH |
NCH=CH2 |
N- |
||
Реакция протекает через промежуточное образование непредельного металлорганического соединения. При последующем взаимодействии его с молекулой исходного реагента образуется винильное производное.
226
6.3.2 Косвенное винилирование -пирролидона
Проблемы технологии прямого винилирования, связанные с применением ацетилена при повышенном давлении, побудили к поиску альтернативных пу-
тей получения -пирролидона. В настоящее время разработаны способы кос-
венного винилирования -пирролидона, т.е. введения винильной группы в результате ряда химических превращений без применения ацетилена.
В промышленности N-винилпирролидон получают дегидрогалогенированием N-( -хлорэтил)пирролидона, пиролизом простых и сложных эфиров N-( - гидроксиэтил)пирролидона, а также дегидратацией N-( - гидроксиэтил)пирролидона.
Дегидрогалогенирование N-( -хлорэтил)пирролидона. Получение N-
винилпирролидона этим методом можно представить следующей общей схемой:
|
|
|
|
CH2—CH2 |
|
|
|
|
|
|
CH2—CH2 |
||||
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
||
|
C=O + H2NCH2CH2OH |
CH2 C=O + H2O |
|||||||||||||
|
|
|
|
O |
|
|
Моноэтаноламин |
|
NCH2CH2OH |
||||||
-Бутиролактон |
|
|
|
|
|
|
|
|
|
||||||
|
|
CH2—CH2 |
|
|
|
|
|
CH2—CH2 |
|||||||
|
|
|
|
|
|
||||||||||
|
|
CH2 |
C=O |
+ SOCl2 |
|
CH2 |
C=O + HCl + SO2 |
||||||||
|
|
|
|
NCH2CH2OH |
|
|
|
|
NCH2CH2Cl |
||||||
|
|
CH2—CH2 |
KOH |
|
|
CH2—CH2 |
|
|
|
||||||
|
|
|
|
|
|||||||||||
|
|
CH2 |
C=O |
|
|
CH2 |
C=O |
|
|
|
|||||
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
-HCl |
|
|
|
|
|
|
|
|
|
|
|
|
NCH2CH2Cl |
|
|
NCH=CH2 |
|
|
|
|||||
Смесь -бутиролактона и моноэтаноламина при 453-463 К превращается в N-( -гидроксиэтил)пирролидон с выходом 90%. Последний реагирует с тионилхлоридом при температуре, не превышающей 308 К, и из смеси выделяют N-( -хлорэтилпирролидон). Его выход составляет 76%.
Отщепление хлорида водорода от N-( -хлорэтил)пирролидона протекает чрезвычайно легко при действии спиртовых растворов щелочей при 293-308 К.
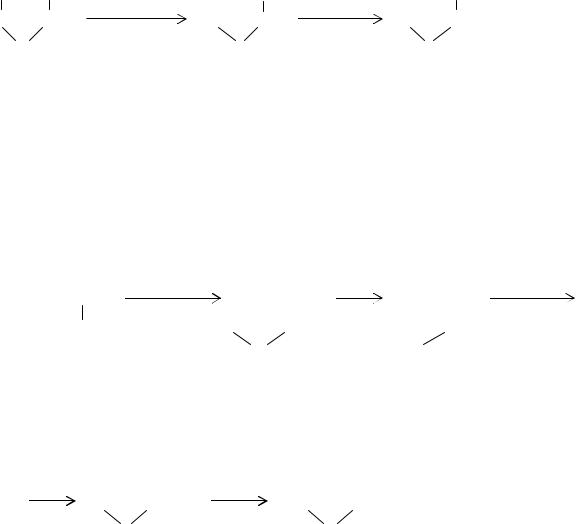
Переход от N-( -хлорэтил)пирролидона к N-винилпирролидону можно осуществить также методом олефинового расщепления через N-( - пирролидонил)этилтриметиламмонийиодат:
227
|
CH2—CH2 |
NaI + (CH3)3N |
|
CH2—CH2 |
Ag2O |
|
|
CH2—CH2 |
|
|
|
|
|||||||
CH2 C=O |
CH2 C=O |
CH2 C=O |
|||||||
|
|
||||||||
|
NCH2CH2Cl |
|
NCH2CH2N(CH3)3I |
|
|
NCH2=CH2 |
|||
Образующуюся четвертичную соль обрабатывают оксидом серебра в растворе метилового спирта. Ее выход составляет 55%. Из смеси выделяют N- винилпирролидон с выходом 81%.
Пиролиз простых и сложных эфиров. N-Винилпирролидон получают также пиролизом ацетата N-( -гидрокси-этил)пирролидона. Процесс можно описать следующей общей схемой:
|
CH2——CH2 |
H2NCH2CH2OH |
|
|
[H] |
|
|
(CH3CO)2O |
|
|
CH2—CH2 |
CH2—CH2 |
|||||||
|
COOH COOH |
|
|
|
|
|
|
|
|
|
|
C=O C=O |
|
CH2 C=O |
|||||
Янтарная кислота |
|
NCH2CH2OH |
|
NCH2CH2OH |
|||||
|
|
|
N-(β-гидроксиэтил)- N-(β-гидроксиэтил)- |
||||||
|
|
|
сукцинимид |
|
|
пирролидон |
|||
CH2—CH2 |
733 К |
|
CH2—CH2 |
|||||
|
|
|
|
|
|
|
||
CH2 C=O |
CH2 |
C=O + CH3COOHю |
||||||
|
||||||||
NCH2CH2OCOCH3 NCH=CH2
N-Винилпирролидон
Взаимодействие янтарной кислоты и моноэтаноламина осуществляют при
423 К, выход N-( -гидроксиэтил)сукцинимида составляет 90-92%. Последний восстанавливают в 50%-ном растворе серной кислоты на свинцовых анодах при
274-278 К. N-( -гидроксиэтил)пирролидон образуется с выходом выше 55%. Его ацетилируют уксусным ангидридом. Выход ацетильного производного составляет ~ 90%. Пиролизом ацетата при 733 К получают N-винилпирролидон с выходом 50%.
Дегидратация N-( -гидроксиэтил)пирролидона. При получении N-
винилпирролидона по этому методу N-( -оксиэтил)пирролидон пропускают в парообразном состоянии при 573-673 К и пониженном давлении над активированным оксидом алюминия (93% Аl2O3, 2% Fe2O3, 5% КОН). Целевой продукт получают с выходом 80%.
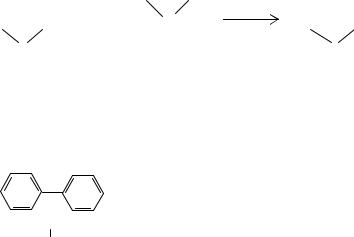
В большинстве методов синтеза N-винилпирролидона основным промежуточным продуктом является N-( -гидроксиэтил)пирролидон. Помимо приве-
228
денных выше способов его можно получить также из -пирролидона и этиленоксида:
CH2—CH2 |
CH2—CH2 |
CH2—CH2 |
||||||||
|
|
CH2 |
|
C=O + |
O |
|
|
CH2 |
|
C=O |
|
|
|
|
|||||||
|
|
NH |
|
|
|
NCH2CH2OH |
||||
6.4. N-ВИНИЛКАРБАЗОЛ
N-Винилкарбазол
 N
N CH=CH2
CH=CH2
применяется для получения поливинилкарбазола. Поли-N-винилкарбазол [поли-(N-карбазолил)этилен] - аморфный прозрачный, бесцветный, хрупкий полимер, растворяется в ароматических углеводородах, сложных эфирах, кетонах, тетрагидрофуране; он гидрофобен, устойчив к кипящей воде, разбавленным щелочам и кислотам.
Впервые поли-N-винилкарбазол был получили Ж. Клемо и У. Перкинмладшим в 1924 г. Промышленное производство поли-N-винилкарбазола стало возможным после разработки В. Реппе в 1937 г. метода синтеза мономера.
Полимеры на основе винилкарбазола известны довольно давно. Так, по- ли-N-винилкарбазол применялся во время Второй мировой войны в Германии и США под торговыми марками "лувикан" и "полектрон" как отличный диэлектрик, превосходящий полистирол.
Поливинилкарбазол обладает высокими механическими и диэлектрическими показателями и значительной теплостойкостью. Его применяют как теплостойкий диэлектрик - заменитель слюды или асбеста - и изолятор в телевизионных и радиоустановках.
Большое значение имело открытие Хеглем в середине 50-х гг. ХХ столетия фоточувствительных свойств поли-N-винилкарбазола. Это открытие позволило создать разнообразные системы записи визуальной информации на основе органических материалов и показало возможность применения полимеров и сополимеров на основе карбазола как фоточувстивительных материалов. Поли- N-винилкарбазол до сих пор остается непревзойденным материалом по комплексу своих эксплуатационных характеристик и используется в различных системах записи информации: электрофотографии, термопластической записи, голографии и др.
Из карбазолилсодержащих мономеров наиболее распространенными мономероми являются N-винилкарбазол и его разнообразные производные:

229
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
N |
|
|
|||||
|
|
|
|
RC=CR'R" |
|||||||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
(CH2)nCH=CH2 |
|
|
|||||
N-Аллилкарбазол и |
N-Алкенилкарбазолы |
||||||||||
его гомологи |
|
|
|||||||||
Сравнительно недавно стали доступными гомологи N-винилкарбазола с заместителями при двойной связи. Такие производные карбазола по неко-
торым свойствам существенно отличаются от N-винилкарбазола. Еще более резкие различия в химическом поведении присущи аллильным производным, у которых двойная связь отделена от атома азота одной или несколькими метиленовыми группами. Находят применение также карбазолилсодержащие виниловые эфиры.
6.4.1. Получение N-винилкарбазола по реакции винилирования ацетиленом
Впервые прямое винилирование карбазола ацетиленом для получения N- винилкарбазола осуществил в Германии перед Второй мировой войной В. Реппе:
|
+ CH CH |
N |
N |
H |
CH=CH2 |
Реакцию проводят под давлением 1,0-2,5 МПа в интервале температур 393-553 К в присутствии в качестве катализатора гидроксидов щелочных и щелочноземельных металлов часто с промотирующими добавками (оксид цинка). В качестве растворителей используют циклогексан, уайт-спирит, N-метил-2- пирролидон и другие.
Метод прямого винилирования карбазолов ацетиленом является достаточно технологичным и экономичным для синтеза N-винилкарбазола и его некоторых производных замещенных в цикле.
Значительные успехи в винилировании карбазола ацетиленом достигнуты при использовании суперосновных сред – сильного основания в диметилсульфоксиде или ином апротонном диполярном растворителе: диметилформамиде, сульфолане, гексаметилтриамидофосфате и т.п. Это объясняется тем, что в результате специфической сольватации катионов происходит резкое повышение концентрации свободных анионов карбазола, осуществляющих нуклеофильную атаку ацетилена.
230
Разработан также эффективный метод синтеза N-винилкарбазола винилированием карбазола ацетиленом при атмосферном давлении под действием гидроксидов щелочных металлов в диметилсульфоксиде в интервале температур 363-433 К с количественным выходом N-винилкарбазола чистотой 99%.
Для прямого винилирования карбазола помимо ацетилена можно использовать винилхлорид и этилен, однако оба реагента проявляют существенно меньшую, чем ацетилен, активность. Этилен винилирует карбазол в присутствии в качестве катализаторов металлов восьмой группы Периодической системы с выходом, не превышающим 40%. Эти методы не получили значительного распространения.
6.4.2. Получение N-винилкарбазола по реакции винилового обмена
Реакция винилового обмена, или транс-винилирование аминов простыми и сложными виниловыми эфирами, является перспективным методом синтеза гетероциклических N-виниламинов:
RR NH + CH2=CH-OR 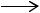 CH2=CH-NRR + R OH.
CH2=CH-NRR + R OH.
В качестве катализаторов используют соли двухвалентной ртути в присутствии протонных или некоторых кислот Льюиса, например ВF3. С помощью транс-винилирования были получены N-винильные производные различных азолов – пиразола, имидазола, триазола - и другие N-виниламины.
Однако взаимодействие карбазола с виниловыми эфирами в присутствии тех же катализаторов не приводит к образованию винилкарбазола. Например, по реакции карбазола с винилацетатом в присутствии каталитической системы, включающей оксид ртути и серную кислоту, образуется не мономер, а олигомерный поли-N-винилкарбазол. Это объясняется тем, что в отличие от перечисленных N-винилазолов, N-винилкарбазол чрезвычайно легко взаимодействует с электрофильными реагентами и мгновенно полимеризуется по катионному механизму. Вот почему невозможно получить N-винилкарбазол в присутствии каталитической системы соль ртути - сильная кислота.
Существует два подхода, позволяющих затормозить полимеризацию N- винилкарбазола под влиянием компонентов катализатора транс-винилирования и сделать эту реакцию пригодной для препаративного получения N- винилкарбазола. Один из них заключается в максимальном уменьшении количества кислоты относительно соли ртути: реализован синтез N-винилкарбазола транс-винилированием карбазола простыми виниловыми эфирами в присутст-
