
- •Государственное бюджетное образовательное учреждение высшего профессионального образования
- •Содержание
- •Список сокращений
- •Введение
- •І. Тема: белки
- •1. Строение и биологическая роль аминокислот, пептидов, белков
- •Аспарагиновая кислота (асп)
- •Лизин (лиз)
- •Серин (сер)
- •1.1. Первичная структура белка
- •1.2. Варианты вторичной структуры белка
- •1.3. Третичная структура белка
- •1.4. Четвертичная структура белка – высший уровень организации
- •Свойства протеинов
- •2.1. Физико - химические свойства биополимеров
- •2.2. Особенности биологических свойств белков
- •3. Методы очистки и выделения белков
- •4. Классификация белков
- •4.1. Простые белки
- •4.1.1. Глобулярные белки
- •4.1. 2. Фибриллярные белки
- •4.2. Сложные белки
- •Характеристика липопротеиновых частиц
- •5. Биологическая роль протеинов
- •Вопросы для самоконтроля:
- •Тестовые задания для оценки уровня знаний:
- •Ситуационные задачи
- •II. Тема: ферменты
- •1. Особенности строения ферментов
- •1.1. Энзим – сложный белок
- •1.1.1. Природа и роль кофермента
- •Витамины – компоненты коферментов
- •1.1.2. Апофермент и его значение
- •1.2. Функциональные центры фермента
- •1.2. Механизм действия ферментов
- •I стадия. Образование es-комплекса
- •II стадия. Активация es-комплекса
- •III стадия. Образование eр-комплекса
- •IV стадия. Распад eр-комплекса
- •1.3. Специфичность действия ферментов
- •1.4. Кинетика ферментативных реакций
- •1.4.1. Зависимость скорости реакции от концентрации субстрата
- •1.4.2. Зависимость скорости реакции от концентрации фермента
- •1.4.3. Зависимость скорости реакции от температуры
- •1.4.4. Зависимость скорости реакции от величины рН среды
- •2. Классификация, номенклатура и регуляция ферментов
- •2.1. Классификация и номенклатура ферментов
- •2.1.1. Характеристика отдельных классов ферментов
- •2.2. Регуляция работы фермента
- •2.2.1. Активация энзима
- •1. Аллостерическая регуляция
- •2.2.2. Особенности строения и функционирования аллостерических ферментов:
- •2.2.4. Регуляция путём ковалентной модификации
- •2.2.5. Частичный протеолиз – как способ активации энзима (активация зимогена)
- •2.3. Ингибирование ферментов
- •2.4. Использование ферментов в медицине.
- •Энзимопатии
- •Энзимодиагностика
- •Энзимотерапия
- •Вопросы для самоконтроля:
- •Тестовые задания для оценки уровня знаний:
- •Ситуационные задачи
2.1. Классификация и номенклатура ферментов
Согласно Международной классификации, биокатализаторы делят на шесть главных классов, в каждом из которых несколько подклассов: 1) оксидоредуктазы; 2) трансферазы; 3) гидролазы; 4) лиазы; 5) изомеразы; 6) лигазы (синтетазы). В основу принятой классификации положен тип катализируемой реакции, который является специфичным для действия любого фермента.
Название энзима строится по следующей схеме:

2.1.1. Характеристика отдельных классов ферментов
1. Оксидоредуктазы. К этому классу принадлежат ферменты, катализирующие окислительно-восстановительные реакции. Как известно, в их основе лежат 3 процесса: присоединение кислорода, отщепление водорода, перенос протонов и электронов.
Это позволило выделить соответствующие подклассы оксидоредуктаз:
а) оксигеназы (гидроксилазы) – производят присоединение к субстрату атома кислорода из молекулы кислорода. Например, реакция синтеза катехоламинов:

б) дегидрогеназы катализируют реакции дегидрирования (отщепления молекулы водорода). В качестве акцепторов электронов используют коферменты НАД+, НАДФ+, ФАД, ФМН. Все ферменты этой группы обладают субстратной спецефичностью. На примере реакции цикла трикарбоновых кислот (ЦТК) получения оксалоацетата из малата:
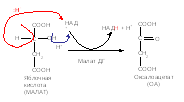
в) оксидазы – переносят электроны и протоны на молекулярный кислород. Такие реакции протекают в процессе клеточного дыхания с участием цитохромов:

2. Трансферазы – отвечают за межмолекулярный перенос функциональных групп. В реакцию вступают 2 субстрата и получается 2 продукта реакции. В зависимости от природы переносимой группы они подразделяются на: аминотрансферазы, ацилтрансферазы, метилтрансферазы, гликозилтрансферазы, фосфотрансферазы (киназы). Пример:
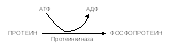
3. Гидролазы – естественно, осуществляют процесс гидролиза различных сложных соединений. Подразделяют их в зависимости от расщепляемой связи: эстеразы, фосфатазы, протеазы (пептидная), гликозидазы (гликозидная), липазы (в липидах сложно-эфирная) и т.д.

4. Лиазы – группа ферментов, представляющих по механизму действия «сборную солянку». Они отщепляют от субстрата низкомолекулярные соединения (Н2О, СО2, NН3, Н2S) или присоединяют молекулу воды по двойной связи. Например:


Кроме того, это единственный класс энзимов, способных разрушить – С–С – связь. Например – альдолаза, производя подобный эффект, разделяет молекулу фруктозо – 1,6 – дифосфата в гликолизе на два триозофосфата.
5. Изомеразы – в отличие от трансфераз, осуществляющих межмолекулярную перестановку атомов, способствуют их внутримолекулярному переносу.

Если переносят группу атомов внутри молекулы, то фермент называют мутазой.

6. Лигазы (синтетазы) катализируют реакции синтеза веществ, которые не обеспечиваются только ферментами, требуется дополнительная энергия АТФ или других макроэргических соединений.

2.2. Регуляция работы фермента
Существует два способа воздействия на деятельность энзима: активация и ингибирование.
2.2.1. Активация энзима
Активирующее влияние на скорость ферментативной реакции оказывают разнообразные вещества органической и неорганической природы, с помощью которых, действуя на ключевые энзимы того или иного биохимического процесса, можно добиваться необходимого эффекта. Для этих целей используются следующие способы:
