
- •Основы термодинамики
- •Глава 1. Основные понятия.
- •Глава 2. Температура. I закон термодинамики.
- •Neкипение 1 27,102 -246,048
- •Если в наличии конечное изменение состояния, то имеем конечный процесс 1→2
- •Для газов величину γ можно определить, измеряя скорость звука в газе :
- •Глава 3. Термохимия.
- •Для облегчения расчетов следует поступать так
- •Глава 4. Второй закон.
- •Легко сообразить, чтобы дать ответ на поставленный вопрос, необходимо взять
- •Глава 5. Процессы в неизолированных системах.
- •Глава 6. Равновесие в однокомпонентных гетерогенных системах. Уравнение Клапейрона – Клаузиуса
- •Глава 7. Термодинамические свойства многокомпонентных систем. Растворы. Химический потенциал.
- •Полный дифференциал внутренней энергии открытой системы можем записать
- •Глава 8. Термодинамика смесей идеальных газов.
- •Глава 9. Смеси жидкостей.
- •Глава 10. Реальные растворы.
- •Как было отмечено ранее, выражение
- •Заметим, что производная от экстенсивной функции по числу молей I–ого компонента является парциальной мольной величиной только в случае постоянства вышеуказанных независимых переменных:
- •Глава 11. Коллигативные свойства растворов.
- •После логарифмирования и дифференцирования имеем
- •Глава 12. Растворы электролитов – термодинамика.
- •Глава 13. Гетерогенное равновесие многокомпонентных систем без химических реакций.
- •Глава 14. Термодинамические свойства реального газа. Летучесть.
- •Если газ реальный и работа его изотермического изменения объема
- •Как мы узнаем ниже, разность е(р) – е(1) умноженная на 2f ( f – число Фарадея, равное 96487 кулонов/г-экв ) как раз равна работе расширения водорода при 25 0с от давления р до 1 атм
- •Глава 15. Термодинамика системы с химической реакцией.
- •Задача легко решается для идеально-газовой смеси, поскольку для нее
- •Глава 16. Тепловая теорема Нернста
- •Проблема возникает при интегрировании уравнения
- •Так как
- •По соотношению Максвелла
- •Глава 17. Элементы термодинамики неравновесных систем.
- •Глава 18. Неравновесные явления в растворах электролитов.
- •Это уравнение Нернста – Эйнштейна связывает коэффициент диффузии иона с его электрической подвижностью.
- •Глава 19. Равновесные электрохимические системы
- •Глава 20. Неравновесные электрохимические системы, основы электрохимической кинетики.
Для облегчения расчетов следует поступать так
если p=Const
![]()
![]()
![]()
![]()
Уравнения химических реакций вместе с тепловыми эффектами называются термохимическими уравнениями и с ними можно оперировать как с алгебраическими уравнениями. Запомним, что если
![]() Qp
выделяется
Qp
выделяется
![]() Qp
поглощается
Qp
поглощается
3.4. Связь между Qp и QV
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() если
реагенты только жидкие или твердые
вещества
если
реагенты только жидкие или твердые
вещества ![]()
![]() ,
где Δn
–изменение числа молей газообразных
участников реакции
,
где Δn
–изменение числа молей газообразных
участников реакции
CO + H2O = CO2 + H2 Δn = 0 Qp = Qv
N2 + 3H2 = 2NH3 Δn = -2 Qp < Qv
Zn (тв) + H2SO4 (ж) = ZnSO4 (p-p) + H2 (газ) Δn = +1 Qp > Qv
Но для реакции в конденсированной системе:
CuSO4 + 5H2O (ж) = CuSO4 5H2O (кр)
![]()
![]() , т.е.
разница между QP
и QV
очень мала, ею можно пренебречь.
, т.е.
разница между QP
и QV
очень мала, ею можно пренебречь.
3.5. Теплота образования химических соединений.
Теплотой образования химического соединения называется тепловой эффект реакции образования одного моля данного соединения из соответствующих чисел молей простых веществ.
Стандартной
теплотой образования
![]() называется теплота образования
химического соединения из простых
веществ, находящихся в стандартных
условиях, причем продукты реакции также
находятся в стандартных условиях.
называется теплота образования
химического соединения из простых
веществ, находящихся в стандартных
условиях, причем продукты реакции также
находятся в стандартных условиях.
За стандартные условия приняты: температура 25 0С (298,15 К) и
1 атм (760 торр).
Замечания
Стандартная теплота образования простого вещества равно нулю
Простое вещество имеет то агрегатное состояние, в котором оно находится в стандартных условиях.
С
(графит) ![]()
С
(алмаз) ![]() = 453,2кал/г-ат
= 453,2кал/г-ат
О2
(кислород) ![]() = 0кал/моль
= 0кал/моль
О3
(озон) ![]() = 34,0ккал/моль
= 34,0ккал/моль
Исключение: для фосфора – белый фосфор
Теплоты образования химических соединений обычно вычисляются по экспериментальным теплотам соответствующих химических реакций, например, для I2O5 :
![]()
![]() ?
?
1.
![]()
![]()
2.
![]()
![]()
3.
![]()
![]()
4.
![]()
![]()
![]()
5.
![]()
![]()
![]()
6.
![]()
![]()
7.
![]()
![]()
8.
![]()
![]()
9.
![]()
![]()
По
закону Гесса :
![]()
Теплоты образования химических соединений приводятся в справочниках физико-химических величин и для вычисления теплового эффекта химических реакций необходимо из суммы теплот образования продуктов реакции вычесть сумму теплот образования исходных веществ:
![]()
Заметим, что в дальнейшем изложении мы введем еще ряд функций состояния и для них закон Гесса также справедлив.
3.6 Зависимость теплового эффекта химической реакции от температуры.
Если Hi мольная энтальпия химического соединения, то
![]()
Очевидно,
что для некоторой химической реакции
![]()
![]()
Дифференцирование по температуре, разделение переменных и интегрирование в интервале от Т1 до Т2 дают (р = const)
![]()
![]()
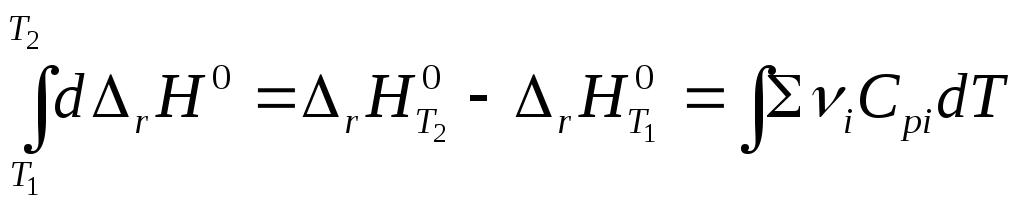
и 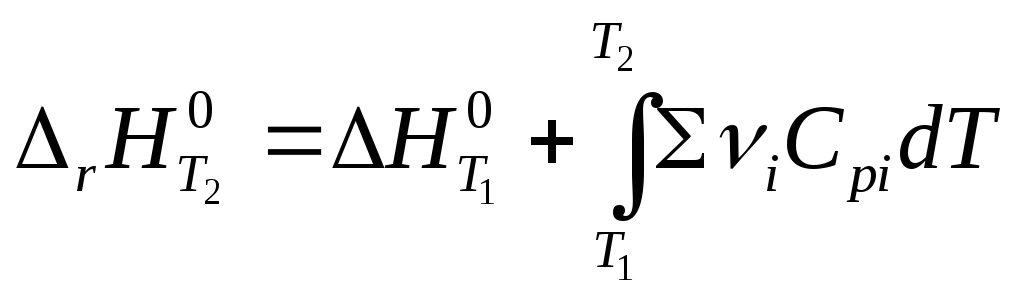 (уравнение
Кирхгоффа)
(уравнение
Кирхгоффа)
Аналогично для ΔU и Cv.
Глава 4. Второй закон.
4.1. Определение.
Каждая термодинамическая система обладает функцией состояния -энтропией. Энтропия прцесса вычисляется следующим образом. Система переводится из начального состояния в соответствующее конечное состояние через последовательность состояний равновесия, вычисляются все подводимые при этом к системе порции тепла dQ, делятся каждая на соответствующую ей абсолютную температуру Т источника теплоты и все полученные таким образом значения суммируются
![]()
![]()
При реальных (не идеальных) процессах энтропия замкнутой (изолированной) системы возрастает
![]() ,
т.е.
,
т.е.![]()
Энтропия – способность к превращению (Клаузиус)
По
I
закону ![]() и
для идеального газа
и
для идеального газа
![]()
![]()
![]() т.е.
для идеального газа
т.е.
для идеального газа ![]() обладает
свойствами полного дифференциала, т.е.S
есть функция состояния.
обладает
свойствами полного дифференциала, т.е.S
есть функция состояния.
|
Распространение
|
4.2. Другие формулировки
Тепло не может само по себе перейти от системы с меньшей температурой к системе с большей температурой (Клаузиус).
Невозможно получать работу, только охлаждая отдельное тело ниже температуры самой холодной части окружающей среды (Кельвин).
4.3. Обратимые и необратимые процессы.
Процесс называется равновесным, если в прямом и обратном направлении проходит через одни и те же состояния бесконечно близкие к равновесию. Работа равновесного процесса имеет максимальную величину по сравнению с неравновесными процессами и называется максимальной работой.
Если равновесный процесс протекает в прямом, а затем в обратном направлении так, что не только система, но и окружающая среда возвращается в исходное состояние и в результате процесса не остается никаких изменений во всех участвовавших в процессе телах, то процесс называется обратимым.
Обратимый процесс – такая же абстракция, что и идеальный газ.
Крайние случаи необратимых процессов : переход энергии от горячего тела к холодному в форме теплоты при конечной разнице температур, переход механической работы в теплоту при трении, расширение газа в пустоту, диффузия, взрывные процессы, растворение в ненасыщенном растворе.
Эти необратимые процессы идут самопроизвольно без воздействия извне и приближают систему к равновесию.
4.4. Изменение энтропии в различных процессах
![]()
причем знак = относится к обратимым процессам, а знак > к необратимым.
Если требуется вычислить энтропию необратимого процесса необходимо провести обратимый процесс между теми же самыми конечным и начальным состоянием (используем тот факт, что энтропия – функция состояния).
а) Изотермический процесс
![]() Q
–часто это скрытая теплота
Q
–часто это скрытая теплота
фазовых переходов.
б)
Изменение температуры при
![]()
![]()
![]()
![]()
![]()
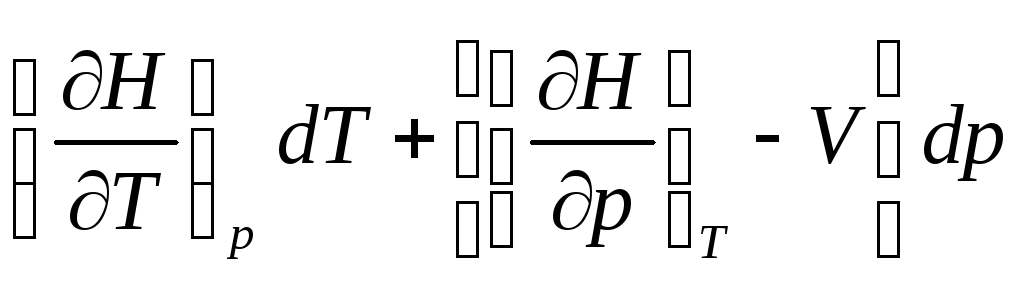 , следовательно
, следовательно  , т.к.
, т.к. ![]()
Энтропия необратимого процесса
![]()
Теплота конденсации при 298 К равна – 10519 кал
![]()
Ответ, очевидно, не верен, поскольку процесс необратимый. Проведем его обратимо :
![]()
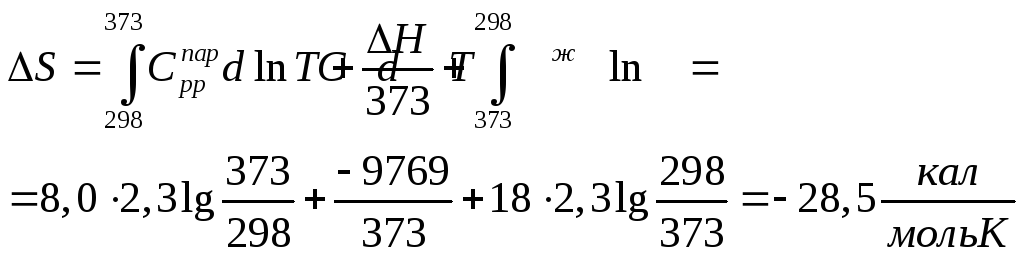
( -9769 – теплота конденсации при 373 К)
![]()
Заметим, что действительно
![]() меньше,
чем
меньше,
чем ![]()
4.5. Закон Джоуля

 это
полный дифференциал, следовательно
это
полный дифференциал, следовательно 

![]()
![]()
![]()
Для
идеального газа ![]()
![]() и
и
![]()
Для
любых систем ![]()
Для
газа Ван-дер-Ваальса ![]() и
и ![]()
4.6. Постулат Планка. Абсолютная энтропия.
Зададимся
вопросом, каково изменение энтропии
некоего процесса, который протекает
при температуре около абсолютного нуля.
Например, имеем две кристаллические
модификации металлического олова:
низкотемпературную, α - Sn,
и высокотемпературную – обычное белое
олово, β – Sn.
Они находятся в равновесии при 14 0С
(287 К),
теплота равновесного превращения 497
кал/моль,
а энтропия его ![]()
