- •Введение
- •Общая классификация топлива
- •1.2. Химический состав топлива.
- •2.2. Возникновение пламени.
- •Температуры воспламенения в воздухе при атмосферном давлении
- •2. 3. Горение газообразного топлива.
- •2. 4. Горение жидкого топлива.
- •2. 5. Горение твердого топлива.
- •3.2. Определение количества и состава продуктов сгорания.
- •Основные формулы для расчета горения топлива
- •3.5. Примеры расчетов горения топлива.
- •Форма таблицы для записи результатов определения расхода воздуха, количества и состава продуктов сгорания
- •5) Для проверки правильности расчета составим материальный баланс. Расчет является верным, если погрешность не превышает 5%.
- •Варианты заданий
- •Средние теплоемкости для воздуха и газов, кДж/м3*˚ с
- •Энтальпия 1 м3 воздуха и газов при различных температурах и постоянном давлении 101,3 кН/м2
Основные формулы для расчета горения топлива
Искомый параметр |
Жидкое и твердое топливо |
Газообразное топливо |
Пересчет на рабочий состав |
ХР=ХО ХР=ХГ
ХР=ХС |
ХВЛ=ХСУХ Н2О=0,1242W
|
Состав смеси |
ХСМ=Х′а+Х″(1-а),
где а= |
|
Низшая теплота сгорания |
-109(ОР-SР)-25WР |
=127СО+108Н2+358СН4++590С2Н4+555С2Н2+635С2Н6+913С3Н8+1185С4Н10+ +1465С5Н12+234Н2S |
Расход кислорода на горение при n=1 |
V(О2)=0,01(1,867СР+5,6НР+ +0,7(SР-ОР)) |
V(О2)=0,01(0,5(СО+Н2+3Н2S)+∑(n+m/4)СnНm) |
Расход сухого воздуха |
VВ=n(1+k)V(О2), где k=79/21=3,76;n – коэффициент расхода воздуха |
|
Объемы компонентов продуктов сгорания |
V(RО2)=0,01(1,867СР+0,7SР) RО2=СО2+SО2 V(Н2О)=0,01(11,2НР+ +1,242WР) V(N2)=0,008NР+nkV(О2) V(О2)'=(n-1)V(О2) |
V(RО2)=0,01(СО2+SО2+СО+ +Н2S+∑nСnНm) V(Н2О)=0,01(Н2О+Н2+ Н2S+ +0,5∑mСnНm) V(N2)=0,01N2+nkV(О2) V(О2)'=(n-1)V(О2) |
Объем продуктов сгорания |
VПС= V(RО2)+ V(Н2О)+ V(N2)+ V(О2)' |
|
Калориметрическая температура горения |
tк=
tк'+ |
|
Энтальпия продуктов сгорания |
Истинная
При температуре tК' I(tК')= |
|
Действительная температура продуктов сгорания |
tД=ηпирtК, где ηпир- пирометрический коэффициент для топочных камер ηпир=0,95 для мартеновских печей ηпир=0,85 – 0,9 для садочных печей ηпир=0,8 – 0,85 для проходных и протяжных печей ηпир=0,7 – 0,75 |
|
3.5. Примеры расчетов горения топлива.
Для расчета горения топлива можно использовать два метода :
-табличный;
-расчетный.
В рассмотренных ниже примерах будем использовать оба метода.
Пример 1.
Определить расход воздуха, состав и количество продуктов сгорания и калориметрическую температуру горения мазута. Его состав следующий, %: CР=85,6, НР=10,5, NР=0,7, ОР=0,5, SР=0,7, АР=0, WР=2. Провести расчет при величине коэффициента избытка воздуха n=1,15. Температура подогрева воздуха tВ=300 ˚ С.
Решение:
Расход воздуха, состав и количество продуктов сгорания определим, пользуясь табличным методом. Для удобства расчет горения жидкого топлива следует вести на 100 кг горючего.
В основу расчета положены реакции полного сгорания отдельных элементов:
С + О2 = СО2
Н2 + ½ О2 = Н2О
S + О2 = SО2
Таблица 4
Форма таблицы для записи результатов определения расхода воздуха, количества и состава продуктов сгорания
Участвуют в горении |
Газообразные продукты, образующие при горении |
||||||||||||||
Топливо |
Воздух |
СО2, кмоль |
Н2О, кмоль |
SО2, кмоль |
О2, кмоль |
N2, кмоль |
всего |
||||||||
Составляющие |
Содержание |
Масса, кг |
Молекулярная масса |
Количество, кмоль |
О2, кмоль |
N2, кмоль |
всего |
||||||||
кмоль |
м3 |
||||||||||||||
кмоль |
м3 |
||||||||||||||
С Н S О N W |
85,6 10,5 0,7 0,5 0,7 2,0 |
85,6 10,5 0,7 0,5 0,7 2,0 |
12 2 32 32 28 18 |
7,13 5,25 0,022 0,016 0,025 0,111 |
7,13 2,625 0,022 -0,016 - - |
9,761∙3,76 |
9,761∙36,7 |
46,462∙22,4 |
7,13 - - - - - |
- 5,25 - - - 0,111 |
- - 0,022 - - - |
- - - - - - |
36,7 (из воздуха) 0,025 - |
|
49,238∙22,4 |
Суммарное значение: при n=1 (%)
при n=1,15 (%)
|
9,761 (21)
11,22 (21) |
36,7 (79)
42,205 (79) |
46,462 (100)
53,43 (100) |
1040,76
1196,87 |
7,13 (14,48)
7,13 (12,68) |
5,361 (10,89)
5,361 (9,54) |
0,022 (0,045)
0,022 (0,039) |
-
1,464 (26,09) |
36,725 (74,58)
42,234 (75,14) |
49,238 (100)
56,211 (100) |
1102,9
1259,1 |
||||
Для определения калориметрической температуры необходимо знать теплоту сгорания топлива. Для жидкого топлива ее можно определить по формуле Д. И. Менделеева (см. табл. 3).
=339 ∙ 85,6 + 1030 ∙ 10,5 – 109 (0,5 – 0,7) – 25 ∙ 2 = 39805,2 кДж/кг
Определим энтальпию продуктов сгорания при условии, что воздух подогрет до 300 ˚ С:
I0=![]() кДж/м3
кДж/м3
Задаемся возможной температурой горения tК = 1800˚ С.
Для этой температуры энтальпия продуктов сгорания (см. приложение 3) будет равна:
СО2 + SО2 . . . . . . . . . (0,1268+0,00039) ∙ 4360,67=553,81
Н2О . . . . . . . . . . . . . . . . . . . . . . . 0,0954 ∙ 3429,9=327,21
О2 . . . . . . . . . . . . . . . . . . . . . . . . .0,2609 ∙ 2800,48=730,65
N2 . . . . . . . . . . . . . . . . . . . . . . . . .0,7514 ∙ 2646,74=1988,76
––––––––––––––––––––––––––––––––––––––––––––––––
Итого . . . . . . . .. . . . . . . . . . . . . . . . . . . . . . . . . . . . 3600,43 кДж/м3
Поскольку I0<I1800 ˚ С, то действительная калориметрическая температура будет ниже 1800 ˚ С.
Примем tК = 1700 ˚ С, тогда энтальпия составит
СО2 + SО2 . . . . . . . . . (0,1268+0,00039) ∙ 4087,1=519,06
Н2О . . . . . . . . . . . . . . . . . . . . . . . 0,0954 ∙ 3203,05=305,57
О2 . . . . . . . . . . . . . . . . . . . . . . . . .0,2609 ∙ 2632,09=686,71
N2 . . . . . . . . . . . . . . . . . . . . . . . . .0,7514 ∙ 2486,28=1868,19
––––––––––––––––––––––––––––––––––––––––––––––––
Итого . . . . . . . .. . . . . . . . . . . . . . . . . . . . . . . . . . . . 3380,05 кДж/м3
Поскольку I1800 ˚ С<I0, действительная калориметрическая температура лежит в пределах 1700 – 1800 ˚ С. Калориметрическую температуру горения определяют интерполяцией:
tК=1700
+
![]() 1775
˚ С.
1775
˚ С.
Пример 2.
Для случая сжигания смешанного газа (смеси коксовального и природного газов) с теплотой сгорания 12 МДж/м3 определить расход воздуха, состав и количество продуктов сгорания, калориметрическую температуру горения при коэффициенте расхода (избытка) воздуха n=1,2. Температура подогрева, воздуха 400 ˚ С. Составить материальный баланс процесса горения.
Состав генераторного газа из тощих топлив (топливо А), %: СО2=6, СО=27, Н2=13, СН4=0,6, N2=53,4. Влажность топлива А WА=24 г/м3.
Состав природного Бугурусланского газа (топливо Б), %: СН4=77,8, С2Н6=4,4, С3Н8=1,7, С4Н10=0,8, СО2=0,2, Н2S=1, N2=14. Влажность топлива Б WБ=4,5 г/м3.
Решение:
1) Производим пересчет с сухой массы на влажную:
![]()
![]()
Расчёт для газа А:
![]()
![]()
![]()
![]()
![]()
![]()
5,83
+ 26,22 + 12,62 + 51,85 + 0,58 + 2,89 = 99,99
![]() 100
100
Расчёт для газа Б:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
0,20 + 77,38 + 1,69 + 0,80 + 13,92 + 0,99 + 4,38 + 0,56 = 99,92 100
2) Определим теплоту сгорания каждого газа:
Qрн
= 127 СО + 108 Н2
+ 358 СН4
+ 590 С2Н4
+ 555 С2Н2
+ 635 С2Н6
+ 913 С3Н8
+1185 С4Н10
+ 1465 С5Н12
+ 234 Н2S![]()
Qрн (А) = 127 · 26, 22 + 108 · 12, 62 + 358 · 0, 58 = 4900, 54 кДж/м3
Qрн (Б) = 358 · 77,38 + 635 · 4,38 + 913 ·1,69 + 1185 · 0,8 + 234 · 0,99 = =33205,97 кДж/м3
3) Определим состав смеси 2-х топлив:
Для этого прежде всего определим долю топлива А в смеси, которую обозначим через а:
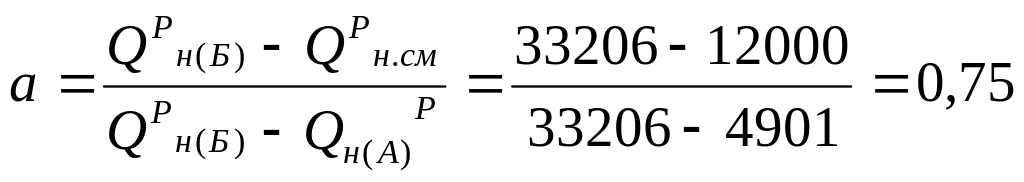
Посчитаем состав смеси:
ХСМ=ХАа+ХБ(1-а)
СО2см = СО2А а + СО2Б (1-а) = 5,83 · 0,75 + 0,20 · 0,25 = 4,42 %
СОсм = 26,22 · 0,75 = 19,67 %
Н2см = 12,62 · 0,75 = 9,47 %
СН4см =0,58 · 0,75 + 77,38 · 0,25 = 19,78 %
N2cм = 51, 85 · 0, 75 + 13, 92 · 0, 25 = 42, 38 %
С3Н8см =1,69 · 0,25 = 0,42 %
С4Н10см =0,8 · 0,25 = 0,20 %
С2Н6см = 4,43 · 0,25 = 1,1 %
Н2Sсм = 0.99 · 0,25 = 0,25 %
Н2Осм = 2,89 · 0,75 + 0,56 · 0,25 = 2,31 %
4,42 + 19,67 + 9,47 + 19,78 + 42,38 + 0,42 + 0,20 + 0,25 + 1,1 + 2,31 = 99,99
4) определить расход воздуха, количество и состав продуктов сгорания:
Определим расход воздуха, состав и количество продуктов сгорания в табличной форме. Расчет ведём на 100 м3 газа.
Участвуют в горении |
Образуется продуктов сгорания, м3 |
|||||||||
Топливо, м3 |
Воздух, м3 |
|||||||||
составляющая |
содержание, м3 |
О2 |
N2 |
всего |
СО2 |
Н2О |
О2 |
N2 |
SO2 |
всего |
СО2 СО Н2 СН4 N2 C3Н8 C4Н10 Н2S C2Н6 Н2О |
4,42 19,67 9,47 19,78 42,38 0,42 0,20 0,25 1,10 2,31 |
-- 9,84 4,73 39,56 -- 2,10 1,30 0,38 3,85 - |
61,75 · 3,76 = 231,20 |
61,753+231,20=294,0 |
4,42 19,67 -- 19,78 -- 1,26 0,80 -- 2,2 -- |
-- -- 9,47 39,56 -- 1,68 1,00 0,25 3,30 2,31 |
-- -- -- -- -- -- -- -- -- -- |
42,38+231,20= 273,58 |
-- -- -- -- -- -- -- 0.25 -- -- |
|
n = 1 |
100 |
61.75
|
231.2
|
292.95
|
48.13
|
57.56
|
-- |
273.6
|
0.25
|
379.52
|
n = 1,2 |
100 |
74.10 (21.0) |
277.4 (79.0) |
351.54 (100) |
48.13 (10.6) |
57.56 (12.64) |
21.18 (4.65) |
328.3 (72.1) |
0.25 (0.06) |
455.42 (100) |