
- •Основы химической кинетики
- •Основы химической кинетики
- •Введение
- •1. Основные понятия химической кинетики
- •2. Скорость химических реакций
- •2.1. Гомогенные химические реакции
- •2.2. Зависимость скорости гомогенной химической реакции от концентрации реагирующих веществ
- •2.3. Графический метод определения констант дифференциального кинетического уравнения
- •2.4. Зависимость концентрации реагирующих веществ от времени для реакции первого порядка. Интегральное кинетическое уравнение
- •2.5. Скорость гетерогенной химической реакции
- •2.6. Зависимость скорости химической реакции от температуры
- •2.6.1. Уравнение Аррениуса
- •2.6.2. Энергия активации
- •Распределение молекул по энергиям
- •2.6.4. Энтропия активации. Стерический фактор
- •2.6.5. Применение уравнения Аррениуса
- •3. Каталитические реакции
- •3.1. Основные понятия
- •3.2. Сущность каталитического действия
- •3.3. Гомогенный катализ
- •3.4. Гетерогенный катализ
- •4. Химическое равновесие
- •4.1. Состояние равновесия
- •4.2. Константа равновесия
- •4.3. Расчет равновесного состава продуктов химической реакции
- •4.4. Смещение химического равновесия. Принцип Ле Шателье
- •4.4.1. Изменение концентраций
- •4.4.2. Изменение давления
- •4.4.3. Влияние температуры
- •5. Цепные реакции
- •5.1. Неразветвленные цепные реакции
- •5.2. Разветвленные цепные реакции
- •6. Индивидуальные задания для самостоятельной подготовки студентов
- •6.1. Примеры решения типовых задач
- •6.2. Задачи для домашнего задания
- •6.3. Варианты домашних заданий
- •6.4. Варианты дополнительных домашних заданий
- •7. Экспериментальная часть Лабораторная работа «Определение дифференциального кинетического уравнения»
- •Выполнение работы
- •Вопросы для самоконтроля
- •Литература
- •Редактор н.П. Лапина
5. Цепные реакции
Цепные реакции – особый класс сложных многостадийных реакций, в которых появление промежуточной активной частицы (атома, содержащего неспаренный электрон, свободного радикала, иона) вызывает цепь превращений исходных веществ в продукты реакции.
К цепным реакциям относятся горение топлива, взрывы, окисление, хлорирование и бромирование соединений, реакции в атмосфере, полимеризация, крекинг нефтепродуктов, ядерные цепные реакции.
В сложном цепном процессе можно выделить следующие стадии:
инициирование (зарождение цепи), при котором образуются активные частицы - переносчики цепи;
рост цепи (продолжение цепи), активные частицы вступают в химическое взаимодействие с исходными веществами, в результате чего образуются новые активные частицы;
обрыв цепи – гибель активных частиц.
Зарождение цепи может происходить в результате диссоциации молекул под действием тепла, излучения или с помощью инициаторов – веществ, которые легко распадаются на свободные радикалы.
Свободным радикалом называется нестойкая частица, образующаяся из молекулы при разрыве одной или нескольких химических связей и обладающая одним или несколькими неспаренными электронами, которые обусловливают высокую химическую активность радикалов (H , Cl, Н3С и др.).
Обрыв цепи может произойти в результате рекомбинации (образования ковалентной связи путем обобществления двух неспаренных электронов, принадлежащих разным частицам), взаимодействия активных частиц со стенками реакционного сосуда (для отвода избыточной энергии) или их взаимодействия со специальными веществами (замедлителями или ингибиторами).
Энергии активации отдельных стадий с участием активных частиц обычно во много раз меньше, чем энергии активации обычных молекулярных реакций, что способствует протеканию цепных реакций с большой скоростью.
5.1. Неразветвленные цепные реакции
Если во время реакции роста цепи не происходит увеличения общего количества радикалов, то цепная реакция называется неразветвленной (рис.12 а).
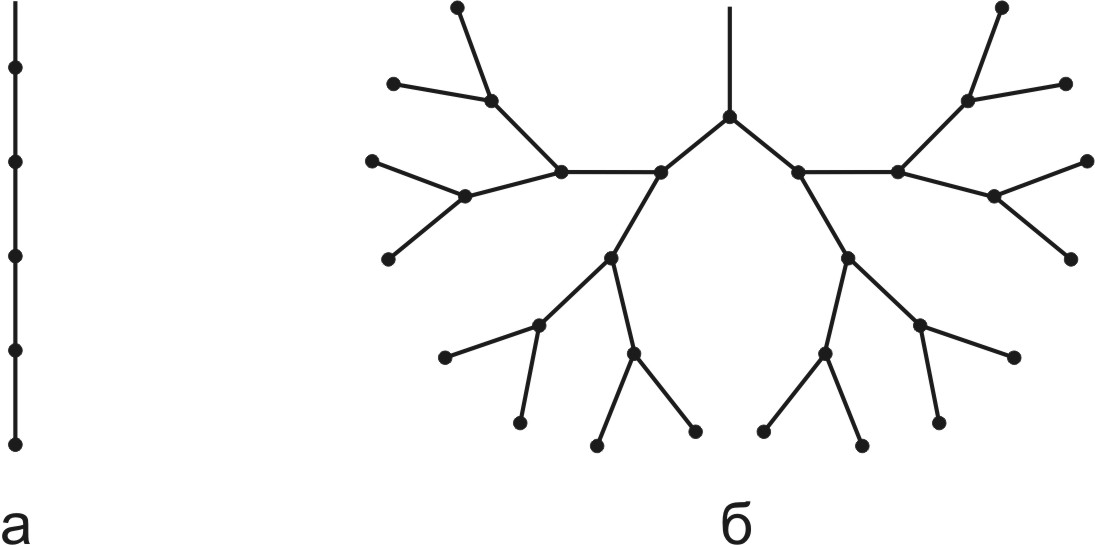
Рис.12. Неразветвленная (а) и разветвленная (б) цепные реакции
Рассмотрим реакцию синтеза хлороводорода под действием света
H 2 + Cl 2 = 2 HCl
1. Зарождение цепи. Поглощая квант лучистой энергии h, молекула хлора распадается. Этот процесс фотохимической диссоциации можно выразить уравнением
Cl 2 + h = 2 Cl
При хлорировании водорода инициирование цепи начинается именно с гомолитического разрыва связей в молекулах хлора (Есв = 243 кДж/моль), так как в молекуле водорода связь между атомами более прочная (Есв = 435 кДж/моль).
2. Рост цепи. В результате взаимодействия радикалов с молекулами образуются продукты реакции и новые активные частицы
Cl + H 2 = HCl + H
H + Cl 2 = HCl + Cl
3. Обрыв цепи. В результате взаимодействия радикалов друг с другом
H + H = H2
Cl + Cl = Cl 2
H· + Cl· = HCl.
Обрыв цепей может произойти в результате столкновения активных частиц со стенкой сосуда или при соударении двух активных частиц и одной неактивной М. Выделяющаяся энергия поглощается стенкой сосуда или уносится неактивной частицей в возбужденном состоянии М:
Cl + Cl + поверхность = Cl 2 адс(поверхность)
Cl + Cl + М = Cl 2 + М.
Этим объясняется влияние объема и природы сосуда, инертных примесей и других факторов, влияющих на скорость цепных реакций.
