- •Рецензент:
- •Общие методические указания
- •Лабораторная работа №1 Тема: Правила безопасности при работе в лаборатории общей химии. Элементы техники лабораторных работ. Весы и взвешивание
- •1.1 Техника безопасности при работе в лаборатории общей химии
- •1.2 Помощь при несчастных случаях
- •1.3 Правила обращения с реактивами
- •1.4 Химическая посуда и оборудование. Элементы техники лабораторных работ
- •1.4.1 Весы и взвешивание
- •1.4.2 Правила обращения с весами
- •1.4.3 Взвешивание цинка на аналитических весах
- •1.5 Необходимый уровень подготовки студентов
- •1.6 Вопросы для самоконтроля
- •Лабораторная работа №2 Тема: Определение молярной массы эквивалента цинка
- •2.1 Теоретические пояснения
- •2.2 Методика проведения опыта
- •2.3 Обработка результатов опыта
- •2.4 Примеры решения задач
- •2.5 Необходимый уровень подготовки студентов
- •2.6 Задания для самоконтроля
- •Тема: Основные классы неорганических соединений: оксиды, основания и амфотерные гидроксиды
- •3.1 Теоретические пояснения
- •3.2 Методика проведения опытов
- •3.2.1 Оксиды их получение и свойства
- •3.2.2 Гидроксиды, их получение и свойства
- •Опыт 2: Получение нерастворимого основания
- •3.3 Необходимый уровень подготовки студентов
- •Уметь писать уравнения реакций, отражающие химические свойства оксидов и гидроксидов.
- •3.4 Задания для самоконтроля
- •Лабораторная работа №4 Тема: Основные классы неорганических соединений: кислоты и соли
- •4.1 Теоретические пояснения
- •4.2 Методика проведения опытов
- •4.2.1 Кислоты, их получение и свойства
- •4.2.2 Соли, их получение и свойства
- •Опыт 5: Получение солей взаимодействием двух солей
- •4.3 Необходимый уровень подготовки студентов
- •4. Уметь писать уравнения реакций, отражающие химические свойства оксидов, гидроксидов, солей. Знать условия протекания до конца реакций ионного обмена
- •4.4 Задания для самоконтроля
- •Лабораторная работа №5 Тема: Кинетика химических реакций
- •5.1 Теоретические пояснения
- •5.2 Методика проведения опытов
- •5.3 Примеры решения задач
- •5.4 Необходимый уровень подготовки студентов
- •5.5 Задания для самоконтроля
- •Лабораторная работа №6 Тема: Химическое равновесие
- •6.1 Теоретические пояснения
- •6.2 Методика проведения опыта
- •6.3 Примеры решения задач
- •6.4 Необходимый уровень подготовки студентов
- •6.5 Задания для самоконтроля
- •Лабораторная работа №7 Тема: Синтез и исследование свойств координационных соединений
- •7.1 Теоретические пояснения
- •7.2 Методика проведения опытов
- •7.3 Необходимый уровень подготовки студентов
- •7.4 Задания для самоконтроля
- •Лабораторная работа №8 Тема: Приготовление растворов заданной концентрации
- •8.1 Теоретические пояснения
- •8.2 Методика проведения опыта
- •8.3 Примеры решения задач
- •8.4 Необходимый уровень подготовки студентов
- •8.5 Задания для самоконтроля
- •Лабораторная работа № 9 Тема: Гидролиз солей
- •9.1 Теоретические пояснения
- •Смещение равновесия в процессах гидролиза солей
- •9.2 Методика проведения опытов
- •8.3 Задания для самоконтроля
- •8.4 Примеры решения задач
- •8.5 Необходимый уровень подготовки студентов
- •Лабораторная работа №10 Тема: Окислительно-восстановительные реакции
- •10.1 Теоретические пояснения
- •10.2 Методика проведения опытов
- •10.3 Необходимый уровень подготовки студентов
- •10.4 Задания для самоконтроля
- •Лабораторная работа №11 Тема: Электрохимический ряд напряжений металлов
- •11.1 Теоретические пояснения
- •11.2 Методика проведения опытов
- •Необходимый уровень подготовки студентов
- •11.4 Задания для самоконтроля
- •Лабораторная работа № 12 Тема:Гальванический элемент
- •12.1 Теоретические пояснения
- •12.2 Методика проведения опыта
- •12.3 Необходимый уровень подготовки студентов
- •12.4 Задания для самоконтроля
- •Лабораторная работа №13 Тема: Изучение свойств азотной, серной и ортофосфорной кислот
- •13.1 Теоретические пояснения
- •13.2 Методика проведения опытов
- •13.3 Необходимый уровень подготовки студентов
- •13.4 Задания для самоконтроля
- •Лабораторная работа №14 Тема: Электролиз солей
- •14.1 Теоретические пояснения
- •14.2 Методика проведения опыта
- •14.3 Необходимый уровень подготовки студентов
- •14.4 Задания для самоконтроля
- •Лабораторная работа № 15 Тема: Коррозия металлов. Защита металлов от коррозии
- •15.1 Теоретические пояснения
- •15.2 Методика проведения опыта
- •Опыт 7: Пассивация алюминия.
- •15.3 Необходимый уровень подготовки студентов
- •15.4 Задания для самоконтроля
- •Содержание
- •Лукашов Сергей Викторович
- •Методические указания по выполнению лабораторных работ
- •241037. Г. Брянск, пр. Станке Димитрова, 3, редакционно-издательский
2.2 Методика проведения опыта
Устройство прибора для определения молярной массы эквивалента металла представлено на рис.1.
Бюретка (1) емкостью 50 мл соединена резиновыми трубками с воронкой (2) и пробиркой (3). В бюретку наливают воду, которая должна также заполнять часть воронки.
Перед началом опыта необходимо убедиться в герметичности прибора. Для этого, пустую пробирку соединяют с бюреткой, и поднимают воронку так, чтобы уровень воды в ней был выше, чем в бюретке. При этом в приборе создается давление, превышающее атмосферное. Если уровень воды в бюретке не изменяется после незначительного первоначального повышения, то прибор герметичен и готов к работе. В противном случае следует исправить дефекты, допущенные при сборке прибора.
При проведении опыта следует придерживаться следующей последовательности действий:
1. Влить в пробирку на 1/5 ее объема через воронку соляную кислоту. Стенки пробирки при этом должны остаться сухими.

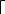






 2
2
3
1

Рис.1. Прибор для определения молярной массы эквивалента металла
2. Держа пробирку в наклонном положении, положить на ее стенку кусочек цинка, взвешенный в лабораторной работе №1 так, чтобы он не соприкасался с кислотой.
3. Присоединить пробирку к прибору, плотно закрыв ее пробкой. Убедиться, что герметичность прибора не нарушена.
4. Передвижением воронки привести воду в ней и бюретке к одному уровню. Отметить и записать уровень воды в бюретке V1, произведя отсчет по нижнему краю мениска (утолщенная поверхностная пленка воды в бюретке). Мениск должен находиться на уровне глаз.
5. Стряхнуть цинк в кислоту. По окончании реакции дать пробирке остыть до комнатной температуры, после чего снова привести воду в бюретке и воронке к одному уровню. Отметить и записать уровень воды в бюретке V2. Разность V1 - V2 равна объему выделившегося водорода в реакции:
Zn + 2 HCl = ZnCl2 + H2↑
6. Отметить показания термометра и барометра.
7. Результаты опыта занести в табл. 1.
Таблица 1. Результаты опыта.
Масса цинка m(Zn), г
|
Условия опыта
|
Уровень воды, мл
|
Объем водорода V(H2), мл
|
|||||
Атмосферное давление Р, мм рт. ст.
|
Давление водяного пара h, мм рт ст.
|
Температура Т, К
|
до опыта V1
|
после опыта V2
|
||||
|
|
|
|
|
|
|
||
2.3 Обработка результатов опыта
1. По разности уровней воды в бюретке до и после протекания реакции вычислить объем выделившегося водорода при температуре и давлении опыта.
2. Так как водород собирается над водой, то он насыщен водяным паром. Общее давление в приборе равно атмосферному и складывается из парциальных давлений водяного пара и водорода. Чтобы вычислить парциальное давление водорода, нужно из атмосферного давления Р вычесть величину давления насыщенного при температуре опыта водяного пара h. Для нахождения h следует воспользоваться данными табл.2.
P(H2)=P-h
Таблица 2. Давление насыщенного водяного пара при различных температурах.
t,0С
|
h, мм рт. ст.
|
t,0С
|
h, мм рт. ст.
|
t,°C
|
h, мм рт. cm.
|
t,°C
|
h, мм рт. cm.
|
10
|
9,2
|
15
|
12.8
|
20
|
17,5
|
25
|
23.8
|
11
|
9,6
|
16
|
13.6
|
21
|
18.6
|
26
|
25,5
|
12
|
10,5
|
17
|
14.5
|
22
|
19.8
|
27
|
26,7
|
13
|
11,2
|
18
|
15,5
|
23
|
21,1
|
28
|
28,3
|
14
|
12,0
|
19
|
16,5
|
24
|
22.4
|
29
|
30.0
|
3.Привести объем выделившегося водорода к нормальным условиям (Р0 -760 мм рт.ст., Т0 = 273 К), используя объединенное уравнение газового состояния:
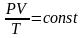
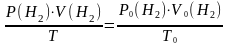
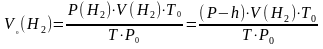
4. Рассчитать экспериментальное значение молярной массы эквивалента цинка в г/моль по закону эквивалентов в соответствии с формулой:
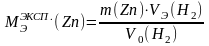
где VЭ(H2) - объем, занимаемый одним моль эквивалента газообразного водорода, равный половине молярного объема водорода, т.е. 11,2 л/моль или 11200 мл/моль.
5. Рассчитать теоретическое значение молярной массы эквивалента цинка, зная молярную массу цинка и эквивалентное число z, численно равное числу электронов, отданных цинком в ходе окислительно-восстановительной реакции с соляной кислотой.
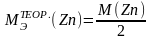
6. Вычислить относительную ошибку опыта по формуле:
ε(%)=