
- •Тверской государственный технический университет в.И. Луцик, а.Е. Соболев, ю.В. Чурсанов физико-химические методы анализа
- •Предисловие
- •Классификация физико-химических методов анализа
- •Метрологические характеристики и статистическая обработка результатов анализа
- •1. Спектральные и оптические методы анализа
- •1.1. Эмиссионный спектральный анализ. Фотометрия пламени
- •1.2. Атомно-абсорбционный анализ
- •1.3. Молекулярно-абсорбционный анализ
- •Метода дифференциальной фотометрии
- •1.3.3. Фотометрическое титрование
- •1.4. Фотометрия светорассеивающих систем
- •1.5. Люминесцентный анализ
- •1.6. Другие оптические методы
- •2. Электрохимические методы анализа
- •2.1. Электрогравиметрия
- •2.1.1. Электродные реакции
- •2.1.2. Электролиз с контролируемым током
- •2.1.3. Электролиз с контролируемым потенциалом
- •2.1.4. Выход по току
- •2.1.5. Электрогравиметрическое определение меди (работа № 10)
- •2.2. Потенциометрия
- •2.2.1. Потенциометрическая ячейка
- •2.2.2. Типы индикаторных электродов в потенциометрии
- •2.2.3. Типы ион-селективных электродов
- •2.2.4. Прямая потенциометрия
- •2.2.5. Потенциометрическое титрование
- •2.2.6. Потенциометрическое определение хлорид-ионов (работа № 11)
- •2.2.7. Определение концентрации фторид-ионов (работа № 12)
- •2.2.8. Потенциометрическое опреление рН и жесткости воды (работа № 13)
- •2.2.9. Определение концентрации хлороводородной и борной кислот методом потенциометрического титрования (работа № 14)
- •2.2.10. Определение концентрации анилина методом потенциометри-ческого титрования (работа № 15)
- •2.3. Кондуктометрический анализ
- •2.3.1. Электрическая проводимость растворов
- •2.3.2. Методы измерения электрической проводимости
- •2.3.3. Прямая кондуктометрия
- •2.3.4. Кондуктометрическое титрование
- •2.3.5. Кондуктометрическое титрование смеси хлороводородной и уксусной кислот (работа № 16)
- •2.3.6. Определение концентрации серной кислоты и сульфата меди методом кондуктометрического титрования (работа № 17)
- •2.4. Полярографический анализ
- •2.4.1. Постояннотоковая (классическая) полярография
- •2.4.2. Вольтамперометрия с линейной разверткой потенциала на стационарных электродах
- •2.4.3. Переменнотоковая полярография
- •2.4.4. Дифференциально-импульсная полярография
- •2.4.5. Амперометрия и амперометрическое титрование
- •2.4.6. Полярографическое определение меди и никеля при совместном присутствии (работа № 18)
- •2.4.7. Амперометрическое определение кадмия (работа № 19)
- •3. Хроматографические методы анализа
- •3.1. Введение в хроматографию
- •3.2. Классификация хроматографических методов анализа
- •3.3. Жидкостная ионообменная хроматография
- •3.4. Плоскостная жидкостная распределительная хроматография
- •3.5. Газовая хроматография
- •4. Термические методы анализа
- •4.1. Общая характеристика методов
- •4.2. Дериватография
- •4.3. Термогравиметрическое определение кальция в виде оксалата (работа № 27)
- •Библиографический список
- •Приложения
- •Организация экспериментальной работы студентов
- •Требования, предъявляемые для допуска к лабораторной работе
- •Порядок выполнения лабораторных работ
- •Требования к оформлению лабораторного отчета
- •Содержание отчета о лабораторной работе
- •Порядок защиты результатов лабораторных работ
- •Статистическая обработка результатов анализа Статистическая обработка градуировочной зависимости
- •Порядок вычисления погрешности и представление аналитических данных
- •Определение точки эквивалентности по кривой титрования
- •Приложение 4 Порядок проведения измерений на приборах, используемых в нескольких лабораторных работах Проведение измерений на потенциометре рН-340
- •Проведение измерений на иономере и-160ми
- •Проведение измерений на иономере эв-74
- •Проведение измерений на рН-метре-милливольтметре рН-410
- •Справочные таблицы Стандартные буферные растворы для рН-метрии
- •Стандартные электродные потенциалы в водных растворах при 25 оС
- •Предельная эквивалентная электрическая проводимость ионов при 25 оС
- •Фотометрия пламени
- •Вопросы зачетного коллоквиума по курсу фхма
- •170026 Г. Тверь, наб. А. Никитина, 22
4. Термические методы анализа
4.1. Общая характеристика методов
В исследовательской практике широко применяется группа методов изучения свойств и состава веществ, объединяемых под общим названием «термический анализ». Методы основаны на взаимодействии вещества с тепловой энергией. В них какой-либо параметр исследуемой системы из-меряют в зависимости от температуры. Наибольшее применение в анали-тической химии находят тепловые эффекты, которые являются причиной или следствием химических реакций. В меньшей степени применяются методы, основанные на выделении или поглощении теплоты в результате физических процессов. Это процессы, связанные с переходом вещества из одной модификации в другую, с изменением агрегатного состояния и дру-гими изменениями межмолекулярного взаимодействия, например, проис-ходящими при растворении или разбавлении. В табл. 4.1 приведены наибо-лее распространенные методы термического анализа.
Таблица 4.1
Методы термического анализа
Название метода |
Регистрируемый параметр |
Измерительный прибор |
Термогравиметрия (ТГА) |
Изменение массы |
Термовесы |
Термогравиметрия по производной (ДТГ) |
Скорость изменения массы |
Термовесы |
Термический (ТА) и дифференциальный термический анализ (ДТА) |
Выделяемая или поглощаемая теплота |
Аппаратура дифференциального термического анализа |
Дифференциальная сканирующая калориметрия (ДСК) |
Выделяемая или поглощаемая теплота |
Дифференциальный сканирующий калориметр |
Термометрическое титрование |
Изменение температуры |
Адиабатический калориметр |
Энтальпиметрия |
Выделяемая или поглощаемая теплота |
Адиабатический калориметр |
Дилатометрия |
Изменение температуры |
Дилатометры |
Катарометрия |
Изменения температуры |
Катарометры |
Наибольшее распространение получили динамическая термограви-метрия (ТГ) и дифференциальный термический анализ (ДТА).
В большинстве случаев измерения проводят при заданной скорости повышения температуры образца, помещенного в специальную печь. В термогравиметрии (ТГ) регистрируют массу образца m, а в ее разновид-ности – термогравиметрии по производной (ДТГ) – скорость изменения массы dm/dt в зависимости от температуры Т. Дополнительную информа-цию о превращениях в веществе при его нагревании (или охлаждении) с заданной скоростью получают, записывая кривую ДТА, отражающую раз-ность температур ΔТ между образцом и инертным эталоном (обычно Al2O3). Для получения кривой ДТА применяют специальное устройство, схема которого изображена на рис. 4.1.
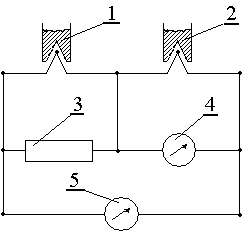
Рис. 4.1. Принципиальная схема установки для записи кривых ДТА и Т:
1 – тигель с инертным веществом; 2 – тигель с образцом; 3 – сопротивление; 4 – гальванометр для измерения ΔТ; 5 – гальванометр для измерения Т
Изображенное соединение термопар двух тиглей (дифференциальная термопара) позволяет четко определять превращения в образце, связанные с изменением его энтальпии. Экзо- и эндоэффекты различаются по направ-лению пиков на кривой ДТА (рис. 4.2).
Традиционный метод ДТА позволяет качественно определить температуры и знаки перехода, но этим способом трудно получить количественную информацию об образце или теплоте того или иного превращения. Подобные трудности обусловлены тем, что остаются неизвестными такие важные факторы, как удельная теплоемкость и теплопроводность образца до и после перехода. На величину площади под эндотермой или экзотермой влияют также скорость нагревания, расположение термопар и другие экспериментальные параметры.
Для того чтобы получить количественные результаты, необходимо превратить отделение для размещения образцов в приборе для ДТА в дифференциальный калориметр. Для этой цели обычно используют дифференциальный сканирующий калориметр (ДСК) с калориметром изотермического типа. Разновидность термического анализа в этом случае называют дифференциальной сканирующей калориметрией.
Методом термометрического титрования изучают зависимость температуры анализируемой системы (обычно это раствор исследуемого вещества) от объема титранта, добавляемого в адиабатических условиях, т.е. когда выделение теплоты происходит значительно быстрее, чем обмен ею с внешней средой. Для титрования используют автоматические бюрет-ки, для измерения температуры – чувствительные термопары и термис-торы, показания регистрируют с помощью самописца.
Энтальпиметрия основана на определении количества вещества по разностям температур, соответствующим изменениям энтальпии ∆Н. Избы-ток концентрированного раствора реагента сразу вводят в раствор пробы, находящейся в адиабатическом калориметре. Такую методику называют прямой инжекционной энтальпиметрией (ПИЭ). Величина изменения температуры ∆Т пропорциональна количеству выделившейся теплоты:
![]()
где К – теплоемкость сосуда и его содержимого, кДж/К. Если теплоем-кость системы К известна, то по изменению температуры и стандартной энтальпии ∆Н0 можно найти количество вещества. Метод отличается высо-кой чувствительностью. Например, им можно определить 3·10–9 моль/дм3 нитрит-иона по реакции с сульфаминовой кислотой.
Метод, в основе которого лежит изменение линейных или объемных размеров в зависимости от температуры, называют дилатометрией. Это термический метод анализа, с помощью которого определяют преимущест-венно структурные изменения. При фазовых переходах меняется коэффи-циент линейного расширения α и вследствие этого относительное увеличе-ние объема или длины:
![]()
Дилатометрия применяется главным образом для исследования полимеров и дает информацию о тепловом расширении, степени их полимеризации и кристалличности. Дилатометрически определяют также изменение объема растворов и конечную точку при титровании (дилатометрическое титро-вание). В ходе такого вида титрования прослеживают изменение объема анализируемого раствора ∆V или пропорционального ему изменения длины ∆l в зависимости от объема титранта.
Еще один метод термического анализа – катарометрия – основан на измерении теплопроводности газовых смесей как функции их состава. В присутствии различных газообразных веществ в потоке газа теплопровод-ность смеси отличается от теплопроводности чистого газа-носителя. Если на пути потока газа поместить нагретую нить, то степень ее охлаждения будет зависеть от состава газовой смеси. Катарометрия широко применяет-ся для анализа технических газовых смесей, например газов, выбрасыва-емых в атмосферу промышленными предприятиями.
