
- •Тверской государственный технический университет в.И. Луцик, а.Е. Соболев, ю.В. Чурсанов физико-химические методы анализа
- •Предисловие
- •Классификация физико-химических методов анализа
- •Метрологические характеристики и статистическая обработка результатов анализа
- •1. Спектральные и оптические методы анализа
- •1.1. Эмиссионный спектральный анализ. Фотометрия пламени
- •1.2. Атомно-абсорбционный анализ
- •1.3. Молекулярно-абсорбционный анализ
- •Метода дифференциальной фотометрии
- •1.3.3. Фотометрическое титрование
- •1.4. Фотометрия светорассеивающих систем
- •1.5. Люминесцентный анализ
- •1.6. Другие оптические методы
- •2. Электрохимические методы анализа
- •2.1. Электрогравиметрия
- •2.1.1. Электродные реакции
- •2.1.2. Электролиз с контролируемым током
- •2.1.3. Электролиз с контролируемым потенциалом
- •2.1.4. Выход по току
- •2.1.5. Электрогравиметрическое определение меди (работа № 10)
- •2.2. Потенциометрия
- •2.2.1. Потенциометрическая ячейка
- •2.2.2. Типы индикаторных электродов в потенциометрии
- •2.2.3. Типы ион-селективных электродов
- •2.2.4. Прямая потенциометрия
- •2.2.5. Потенциометрическое титрование
- •2.2.6. Потенциометрическое определение хлорид-ионов (работа № 11)
- •2.2.7. Определение концентрации фторид-ионов (работа № 12)
- •2.2.8. Потенциометрическое опреление рН и жесткости воды (работа № 13)
- •2.2.9. Определение концентрации хлороводородной и борной кислот методом потенциометрического титрования (работа № 14)
- •2.2.10. Определение концентрации анилина методом потенциометри-ческого титрования (работа № 15)
- •2.3. Кондуктометрический анализ
- •2.3.1. Электрическая проводимость растворов
- •2.3.2. Методы измерения электрической проводимости
- •2.3.3. Прямая кондуктометрия
- •2.3.4. Кондуктометрическое титрование
- •2.3.5. Кондуктометрическое титрование смеси хлороводородной и уксусной кислот (работа № 16)
- •2.3.6. Определение концентрации серной кислоты и сульфата меди методом кондуктометрического титрования (работа № 17)
- •2.4. Полярографический анализ
- •2.4.1. Постояннотоковая (классическая) полярография
- •2.4.2. Вольтамперометрия с линейной разверткой потенциала на стационарных электродах
- •2.4.3. Переменнотоковая полярография
- •2.4.4. Дифференциально-импульсная полярография
- •2.4.5. Амперометрия и амперометрическое титрование
- •2.4.6. Полярографическое определение меди и никеля при совместном присутствии (работа № 18)
- •2.4.7. Амперометрическое определение кадмия (работа № 19)
- •3. Хроматографические методы анализа
- •3.1. Введение в хроматографию
- •3.2. Классификация хроматографических методов анализа
- •3.3. Жидкостная ионообменная хроматография
- •3.4. Плоскостная жидкостная распределительная хроматография
- •3.5. Газовая хроматография
- •4. Термические методы анализа
- •4.1. Общая характеристика методов
- •4.2. Дериватография
- •4.3. Термогравиметрическое определение кальция в виде оксалата (работа № 27)
- •Библиографический список
- •Приложения
- •Организация экспериментальной работы студентов
- •Требования, предъявляемые для допуска к лабораторной работе
- •Порядок выполнения лабораторных работ
- •Требования к оформлению лабораторного отчета
- •Содержание отчета о лабораторной работе
- •Порядок защиты результатов лабораторных работ
- •Статистическая обработка результатов анализа Статистическая обработка градуировочной зависимости
- •Порядок вычисления погрешности и представление аналитических данных
- •Определение точки эквивалентности по кривой титрования
- •Приложение 4 Порядок проведения измерений на приборах, используемых в нескольких лабораторных работах Проведение измерений на потенциометре рН-340
- •Проведение измерений на иономере и-160ми
- •Проведение измерений на иономере эв-74
- •Проведение измерений на рН-метре-милливольтметре рН-410
- •Справочные таблицы Стандартные буферные растворы для рН-метрии
- •Стандартные электродные потенциалы в водных растворах при 25 оС
- •Предельная эквивалентная электрическая проводимость ионов при 25 оС
- •Фотометрия пламени
- •Вопросы зачетного коллоквиума по курсу фхма
- •170026 Г. Тверь, наб. А. Никитина, 22
2.4.3. Переменнотоковая полярография
В целях расширения аналитических возможностей метода поляро-графии широко используют различные модификации сигнала напряжения, поляризующего индикаторный электрод. В одной из них линейно меняю-щееся напряжение Еп модулировано переменной составляющей Ем, имею-щей незначительную амплитуду (не выше 60 мВ в случае реакции с одноэлектронным переходом). Форма переменного напряжения может быть различной – синусоидальной, прямоугольной, трапециевидной, тре-угольной. Частота переменного напряжения может меняться в широких пределах от Гц до кГц. Рассмотрим переменнотоковую полярографию, в которой постоянная составляющая модулирована синусоидальным напряжением.
Зависимость напряжения от времени в переменнотоковой синусои-дальной полярографии и переменнотоковая полярограмма на фоне клас-сической постояннотоковой полярограммы представлены на рис. 2.24.
Ток в цепи электролизера при наложении синусоидально модулиро-ванного напряжения, меняющегося по закону
E = Eп + ∆Eм · sin ωt,
имеет три составляющих:
– диффузионный ток, связанный с электродной реакцией, протекаю-щей под воздействием медленно меняющегося напряжения;
– ток заряда-разряда двойного электрического слоя (ДЭС) под воздей-ствием синусоидального напряжения;
– ток, вызванный изменением скорости электродной полуреакции под воздействием синусоидального напряжения.
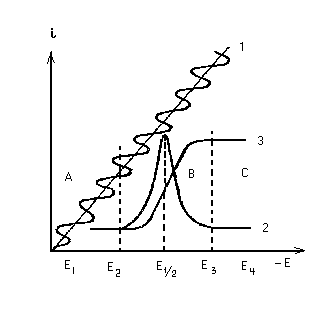
Рис. 2.24. Зависимость напряжения от времени (1);
переменнотоковая (2) и постояннотоковая (3) полярограммы
одного и того же раствора
В цепь регистрирующего прибора переменнотокового полярографа включен трансформатор, вследствие чего постоянная составляющая не регистрируется и в цепи протекает лишь сумма токов, а именно: тока ДЭС (от дозаряда-подразряда конденсатора (ДЭС)) и фарадеевского (от восста-новления-окисления электродноактивного вещества). Фарадеевская состав-ляющая значительно больше двойнослойной, поэтому именно она опреде-ляет вид зависимости силы тока от потенциала.
В области потенциалов, где электродноактивное вещество еще не восстанавливается (рис. 2.24, область А), незначительные изменения потенциала не вызывают возникновения фарадеевского тока. Сила пере-менного тока определяется емкостной составляющей и по принятому условию незначительна. В области предельного тока постояннотоковой полярографии (область С) незначительные изменения потенциала не вызывают сдвига его до значений, при которых продукты восстановления могли бы вновь окислиться, т.е. нет условий для возникновения обратного тока и переменная составляющая фарадеевского тока также отсутствует. В области развития постояннотоковой полярографической волны (область B) при полной обратимости электродного процесса и достаточно высокой (по сравнению со скоростью диффузионного отвода продуктов реакции) частотой изменения потенциала имеются условия и для восстановления, и для окисления вещества.
При этом на участке до E½ сила тока определяется дополнительным количеством восстановленной формы, созданной предыдущим импульсом, а на участке после E½ – долей катодноактивного вещества, изымаемого из общего диффузионного потока переменной катодной составляющей тока. По мере роста потенциала до потенциала полуволны доля восстановленной формы возрастает, а после него доля катодноактивного вещества убывает, что ведет к возрастанию и последующему убыванию силы тока. Максимум последнего соответствует потенциалу полуволны, т.е. переменный ток имеет вид пика с максимумом при E½. В случае частично или полностью необратимого процесса картина осложняется, не меняя, впрочем, общего закона изменения силы тока.
Существенный фактор, влияющий на силу тока пика, его потенциал и форму, – это степень обратимости электродной реакции анализируемого вещества. При одной и той же концентрации сила тока пика обратимой электродной реакции значительно (до 20 раз) превышает силу тока пика полностью необратимой реакции. Таким образом, в анализе предпочти-тельны обратимые реакции.
Сила тока пика пропорциональна квадрату числа электронов, принимающих участие в полуреакции, так что многовалентные ионы опре-делимы при меньших концентрациях. Сила тока пика возрастает с ростом амплитуды Ем в пределах Ем < RT/nF. Потенциал пика совпадает с потен-циалом полуволны в постояннотоковой полярографии в случае обратимой реакции, существенно сдвинут от него в случае необратимой. Ширина пика (чаще говорят о полуширине) больше для необратимой реакции, а для обратимой – обратно пропорциональна числу электронов.
Таким образом, в аналитической практике наиболее удачно приложе-ние метода к определению многовалентных, обратимо восстанавливаю-щихся ионов. Для них и сила тока пика выше, и сам пик острее, лучше очерчен.
Аналитические возможности переменнотоковой полярографии сравнимы с постояннотоковой полярографией и по чувствительности (Спр = 10–5 моль/дм3), и по скорости получения результатов. Время полу-чения результатов может быть существенно снижено применением быстрой развертки постоянной составляющей напряжения. Верхний предел определяемой концентрации в этом методе лежит на уровне 10–2 – 10–3 моль/дм3.
