
- •Изменение состава кислотной смеси с ф.Н.А 80%.
- •Кислотооборот
- •Технология мононитротолуола,
- •Состав и основные физико-химические свойства нитротолуола.
- •Состав побочных продуктов нитрования толуола
- •Описание технологического процесса получения мнт.
- •Технология получения 2.4-динитротолуола и смеси 2.4-/2.6-динитротолуолов (65/35%).
- •Описание технологического процесса получения 2.4-днт.
- •Состав «сырого» мнт, %.
- •Состав «черной» отработанной кислоты, %.
- •Основные физико - химические свойства несимметричных изомеров тринитротолуола
- •Требования к качеству тротила
- •Описание технологического процесса.
Описание технологического процесса.
Установка состоит из нескольких (в зависимости от производительности) нитраторов, работающих параллельно. Реакторы снабжены мощными мешалками типа гребного винта и несколькими секциями змеевиков. В каждый нитратор дозируются толуол, 45-60% азотная кислота и 2-я отработанная кислота с температурой 55-750С по обогреваемому коллектору через распределительную коробку. Фактор нитрующей активности кислотной смеси Ф=69-73%. Избыток азотной кислоты 3-5% сверх теоретически необходимого. Оптимальная температура нитрования 30-400С. Предельная 50-550С. В случае повышения температуры до 1000С содержимое аппаратов перекачивается ц/б насосами в сепарационную колонну. Процесс протекает в отработанной кислоте состава ~ 66-70% серной кислоты, ~ 0.2-1.2% азотной кислоты и ~ 3.0-6.0% окислов азота., которая содержит до 0.5-1.0% растворенного нитротолуола. Поскольку для приготовления кислотной смеси используется 2-ая отработанная кислота, то полученный МНТ содержит до 10-30% ДНТ. Коэффициент распределения азотной кислоты между органической и кислотной фазами = ~ 2.
Из нитраторов реакционная масса по общему коллектору самотеком поступает в один аппарат – разбавитель, где разбавляется кислой промывной водой после промывки ТНТ (содержащей 10-30% серной кислоты) до концентрации по серной кислоте 66-70%. Разбавление преследует следующие цели:
1. снизить растворимость МНТ в отработанной кислоте;
2. подготовить отработанную кислоту к денитрации (разрушить нитрозилсерную кислоту);
3. утилизировать кислую промывную воду.
Из разбавителя масса через буферную емкость насосом подается в сепарационную колонну, затем отделившаяся отработанная кислота направляется в отстойные колонны и далее на регенерацию. Отделившийся МНТ, содержащий до 3.0-3.5% толуола, поступает на вторую стадию.
Тепловой эффект реакции мононитрования толуола достаточно высок и составляет 38 ккал/моль или 414 ккал/кг. толуола. Вследствие большой скорости реакции нитрования толуола и, следовательно, значительного количества тепла, выделяющегося в единицу времени, производительность нитратора зависит от его теплотехнических характеристик. Производительность нитратора при этом пропорциональна количеству тепла, которое может быть отведено теплообменной поверхностью от реакционной массы в единицу времени. В этом случае желательно иметь нитраторы такой конструкции, чтобы они имели наибольшую поверхность охлаждения. Таким образом, производительность реакторов на стадии получения МНТ определяется исключительно скоростью теплоотвода. Применение для проведения нитрования реакторов с трубчатыми теплообменниками (циркуляционные и кожухотрубчатый реакторы) позволяет значительно интенсифицировать процесс нитрования как за счет увеличения поверхности теплообмена, так и повышения интенсивности перемешивания (увеличения поверхности контакта двух фаз). Однако приведенные в таблице время пребывания отражает не скорости химической реакции, а отвод реакционного тепла при данной скорости дозировки реагирующих компонентов.
Наименование показателя |
Циркуляционный реактор |
Кожухотрубчатый реактор |
Змеевиковый реактор |
Объем рабочий, м3 |
2.0 |
3.0 |
5.6 |
Поверхность охлаждения, м2 |
74.0 |
145.0 |
69.7 |
Частота вращения мешалки, мин. |
980 |
735 |
200 |
Производительность по толуолу, кг/ |
1610 |
2030 |
1200 |
Время пребывания, мин. |
12.5 |
17.0 |
48.0 |
Как отмечалось выше, содержание примесей в готовом продукте определяется условиями получения МНТ. Проведение процесса при 50-550С не является оптимальным и содержание несимметричных изомеров ТНТ составляет 4-5%. Однако снижение температуры при сохранении существующего аппаратурного оформления возможно лишь при использовании более эффективного хладагента; этот путь усовершенствования процесса экономически невыгоден.
НИТРОВАНИЕ МОНОНИТРОТОЛУОЛА ДО ДИНИТРОТОЛУОЛА
Динитротолуол (ДНТ) получают нитрованием МНТ серно-азотными смесями:
СH3C6H4(NO2) + HNO3 CH3C6H3(NO2)2 + H2O
Вследствие тормозящего влияния электроноакцепторной нитрогруппы в ароматическом ядре на скорость электрофильных реакций, нитрование МНТ до ДНТ проводят кислотными смесями с более высоким фактором нитрующей активности Ф, равным 78-80 %, при температуре 60-750С.
Более высокий по сравнению с первой стадией избыток азотной кислоты (15-20% сверх теоретически необходимого) требуется для компенсации ее потерь, вызванных окислительными процессами, а также термическим разложением и испарением, скорость которых увеличивается с повышением температуры.
Поскольку технический МНТ является смесью трех изомеров, то при его нитровании образуются все шесть изомеров ДНТ:
При нитровании орто-МНТ, вследствие согласованной ориентации имеющихся в нем заместителей в положения кольца 4 и 6, образуются преимущественно 2,4-динитротолуол (выход 66%) и 2,6-динитротолуол (выход 33%) с незначительной примесью (до 0,5%) 2,3- и 2,5- динитротолуолов.
По той же причине при нитровании пара-МНТ образуется почти исключительно 2,4-динитротолуол, содержащий в качестве примеси до 0,4% 3,4-динитротолуола.
При нитровании мета-МНТ из-за несогласованной ориентации заместителей получается четыре изомера ДНТ в следующих количествах:

Технический ДНТ имеет примерно следующий состав:
2,4-ДНТ...........75,6%; 2,3-ДНТ.............1,44%;
2,6-ДНТ...........19,7%; 2,5-ДНТ.............0,61%;
3,4-ДНТ............2,5%; 3,5-ДНТ.............0,08%.
Образовавшиеся на стадии мононитрования в качестве побочных продуктов нитропроизводные крезолов в условиях динитрования частично нитруются до тринитросоединений и частично окисляются. Образование динитро- и тринитрокркзолов имеет место и на 2-й стадии: из о-МНТ образуются 2.3-динитро- и 2.5.6-тринитропаракрезолы, из м-МНТ – 2.6-динитропаракрезол и 4.6-динитроортокрезол, из п-МНТ - 4.5.6-тринитрокрезол.
Технический ДНТ представляет собой маслянистое кристаллическое вещество желтого цвета с температурой затвердевания 50-540С.
ДНТ практически нерастворим в воде, хорошо растворяется в органических растворителях. Растворимость ДНТ в серной кислоте возрастает с повышением концентрации кислоты и температуры, что видно из приведенных ниже данных.
-
Концентрация H2SO4,%.
200C
500C
700C
80,0
1,2
2,5
3,8
90,0
8,5
16,8
20,0
99,8
46,0
144,0
1121,0
В применяемых для получения моно - и динитротолуолов кислотных смесях скорость нитрования изомеров МНТ примерно в 106 ниже, чем скорость нитрования толуола. Поэтому можно было ожидать, что определяющую роль в процессе нитрования МНТ будет играть кинетика реакции. Однако в индустриальных условиях скорость нитрования МНТ в гетерогенных условиях, также как и скорость нитрования толуола, зависит от интенсивности перемешивания, что позволяет сделать вывод о влиянии массопереноса на суммарную скорость нитрования МНТ. Хотя установленная зависимость выражена менее резко, чем при нитровании толуола, однако это свидетельствует о том, что нитрование МНТ в значительной степени протекает в кислотном слое вблизи поверхности раздела фаз.
Описание технологического процесса
Высокая скорость нитрования МНТ позволяет организовать процесс получения ДНТ как в режиме прямотока, так и в режиме противотока.
Прямоточная схема. Нитрование осуществляется в прямоточной системе, состоящей из одного или двух основных и одного буферного аппаратов, причем в качестве дореактора используется совмещенный аппарат со шнековым подъемником и спиральным сепаратором. В основные аппараты дозируются МНТ, меланж и 3-я отработанная кислота из сепаратора первого аппарата третьей фазы. Из основного реактора реакционная масса самотеком поступает в реакционную часть буферного совмещенного аппарата, в сепараторе которого происходит отделение ДНТ от отработанной кислоты. Отработанная кислота по обогреваемому коллектору поступает в аппараты первой фазы, а ДНТ самотеком идет в реакционное отделение первого аппарата третьей фазы.
Противоточная схема. Процесс проводится в нитрационной системе, состоящей из 2-3 нитрационных агрегатах совмещенного типа, работающих параллельно по подаче МНТ и меланжа и последовательно по потоку третьей отработанной кислоты. МНТ и меланж дозируются в каждый нитратор. Отработанная кислота из сепаратора первого нитрационного агрегата третьей фазы с температурой 80-900С и ф.н.а. не ниже 92% поступает в нитрационную часть последнего аппарата второй фазы и проходит последовательно все аппараты. Реакционная масса из нитрационной зоны шнековым подъемником подается в сепарационную, где расслаивается. ДНТ из сепаратора поступает в общий обогреваемый коллектор и оттуда в нитрационное отделение первого аппарата третьей фазы, а отработанная кислота самотеком идет в следующий по ходу кислотной смеси аппарат. Из сепаратора первого нитрационного агрегата отработанная кислота по обогреваемому коллектору поступает в нитраторы первой фазы.
НИТРОВАНИЕ ДИНИТРОТОЛУОЛА ДО ТРИНИТРОТОЛУОЛА
Тринитротолуол (ТНТ) получают нитрованием динитротолуола серно-азотными кислотными смесями:
CH3C6H3(NO2)2 + HNO3 CH3C6H2(NO2)3 + H2O
Нитрование динитротолуола–наиболее медленная стадия получения тротила. Вследствие резкого торможения скорости вступления третьей нитрогруппы двумя другими нитрогруппами, уже имеющимися в бензольном ядре, нитрование ДНТ до ТНТ проводят кислотными смесями с фактором нитрующей активности Ф выше 88 - 90%, при температуре более 100 - 1050С и большом избытке азотной кислоты (избыток азотной кислоты зависит от способа проведения процесса.
При нитровании технического ДНТ получаются все шесть возможных изомеров ТНТ.
|
|
|
2,4,6 - ТНТ |
2,3,4 - ТНТ |
2,4,5 - ТНТ |
|
|
|
2,3,6 - ТНТ |
2,3,5 - ТНТ |
3,4,5 - ТНТ |
При нитровании 2,4- и 2,6-динитротолуолов образуется исключительно 2,4,6-тринитротолуол.
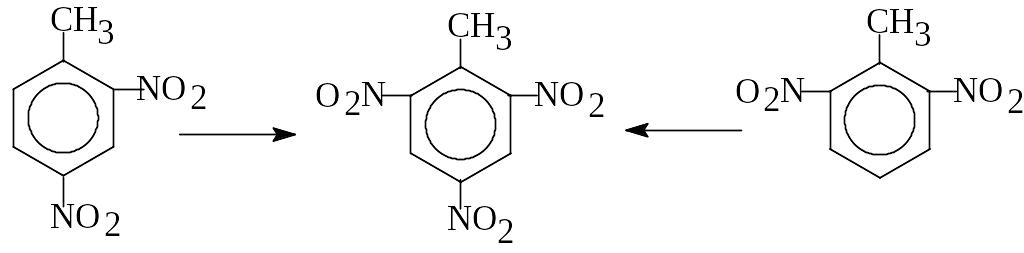
Все другие пять изомеров ТНТ образуются из остальных изомеров ДНТ. Технический ТНТ имеет примерно следующий состав (%):
Изомер ТНТ |
% |
Изомер ТНТ |
% |
Изомер ДНТ |
% |
2.4.6-ТНТ |
95.5 |
2,3,6-ТНТ |
0,29 |
2,3-ДНТ |
0,33 |
2,3,4-ТНТ |
1,36 |
2,3,5-ТНТ |
0,009 |
2,5-ДНТ |
0,15 |
2,4,5-ТНТ |
2,69 |
3,4,5-ТНТ |
0,002 |
3,5-ДНТ |
0,06 |
Все изомеры ТНТ являются кристаллическими веществами от белого до светло-желтого цвета с температурами затвердевания от 80 до 1320С.
Растворимость в воде изомеров ТНТ незначительна. Наибольшей растворимостью обладает 2,4,6-ТНТ (0,15% при 100 0С). В органических растворителях ТНТ растворяется достаточно хорошо.
ТНТ довольно хорошо растворяется в серной кислоте. Так, в 90% серной кислоте при 800С растворимость составила 10%. Растворимость ТНТ в азотной кислоте, даже разбавленной, очень высока. Так, в 100 г. 80% азотной кислоты при 500С растворяется 150 г ТНТ.
Растворимость ДНТ и ТНТ в серной и азотной кислотах резко возрастает с увеличении их концентрации. Поэтому можно было ожидать, что в условиях нитрования ДНТ крепкими кислотными смесями и при повышенных температурах, весь нитропродукт будет находится в растворе. Однако в действительности реакционная смесь является гетерофазной, т.к. добавление азотной кислоты к серной приводит к снижению растворимости нитросоединений. Так, растворимость 2,4,6-ТНТ в 95% серной кислоте при 700С составляет 13,5%, а при добавлении 5% азотной кислоты снижается до 7,5%.
Из-за низкой реакционной способности ДНТ в реакции электрофильного замещения, гетерогенное нитрование этого соединения протекает в кинетическом режиме в объеме минеральной фазы, что подтверждается независимостью скорости процесса от интенсивности перемешивания. В данном случае перемешивание необходимо для распределения компонентов в реакционном объеме.
Необходимость использования из-за низкой скорости нитрования ДНТ повышенных температур и больших избытков высококонцентрированных кислотных смесей приводит в процессе получения ТНТ к протеканию интенсивных окислительных процессов. Окисление как ДНТ, так и ТНТ, протекает по двум направлениям: по метильной группе с образованием соответствующих нитробензойных кислот, так и деструктивное нитрование, приводящее к образованию газообразных продуктов (N2O3, СО, СО2) и тетранитрометана C(NO2)4. В условиях реакции скорость окисления ДНТ выше, чем ТНТ. Причем основным направлением является полная деструкция ДНТ (содержание 2,4- и 3,4-динитробензойных кислот в тротиле-сырце не превышает 0,006%).
Напротив, ТНТ в условиях нитрования образует преимущественно продукты окисления по метильной группе: тринитробензиловый спирт, тринитробензальдегид, тринитробензойную кислоту и тринитробензилнитрат, количество которых в тротиле-сырце достигает 1,5%.

При декарбоксилировании 2,4,6-тринитробензойной кислоты образуется до 0,4% тринитробензола.
Образовавшиеся на стадиях моно- и динитрования нитропроизводные крезолов в условиях третьей стадии практически полностью окисляются и не обнаруживаются среди продуктов реакции.
Описание технологического процесса.
Процесс нитрования ДНТ в ТНТ может быть осуществлен как в режиме прямотока реагирующих компонентов, так и в режиме их противотока.
Прямоточная схема нитрования ДНТ. Особенность процесса нитрования в режиме прямотока ДНТ и кислотной смеси состоит в том, что при движении реакционной массы по каскаду аппаратов концентрация нитруемого соединения падает, но нитрующая активность кислотной смеси также уменьшается вследствие разбавления реакционной массы водой, выделяющейся в процессе нитрования, «раскисления» (термического разложения) азотной кислоты и в результате протекания окислительных процессов, что в конечном итоге приводит к снижению скорости нитрования. Поэтому для повышения скорости реакции при проведении процесса в режиме прямотока ДНТ и кислотной смеси необходимо использовать кислотные смеси с высоким Ф.Н.А, очень большой (по-видимому, более 300% от теоретически необходимого) избыток азотной кислоты и высокие (свыше 1000С) температуры реакции. Указанные условия приводят к протеканию интенсивных экзотермических окислительных процессов, что при наличии в реакционной массе продуктов высокой степени нитрования повышает опасность процесса. С целью снижения опасности процесс нитрования ДНТ в ТНТ был разбит на две стадии с получением на первой стадии в более мягкие условиях нитрования сплава ДНТ с ТНТ (частичное нитрование ДНТ) с последующим превращением не вступившего в реакцию ДНТ в конечный продукт на второй стадии.
Первая стадия проводилась в каскаде из 4 аппаратов (1 основной и 3 буферных). В основной аппарат одновременно дозировались ДНТ, меланж и отработанная кислота с последующей стадии с Ф=96-98%. Ф кислотной смеси 87-91%. Избыток азотной кислоты 150-175% от теоретически необходимого для нитрования 50% ДНТ. Температура реакции постепенно повышалась от 80-850С в первом аппарате до 105-1100С в последнем. Время пребывания компонентов в нитрационной системе 2 час
Из четвертого аппарата реакционная масса направлялась в сепаратор. Отсепарированный ДНТ поступал на донитровывание, а отработанная кислота шла на стадию получения ДНТ.
Вторая стадия осуществлялась в системе из 5 аппаратов (1 основной и 4 буферных), соединенных последовательно. В первый (основной) аппарат дозировались сплав ДНТ с ТНТ и кислотная смеси, содержащая 89% серной кислоты и 14% азотной кислоты (Ф=99%). Избыток азотной кислоты 175% для донитровывания оставшихся 50% ДНТ. Температура реакции постепенно повышалась от 80-850С в первом аппарате до 115-1200С в последнем. Время пребывания компонентов в реакционной системе 3-3.5 час. Таким образом общее время нитрования ДНТ до ТНТ на двух стадиях 5-5.5 час. Отсепарированный ТНТ поступал далее на промывку и очистку, а отработанная кислота направлялась на стадию получения сплава ДНТ с ТНТ.
Противоточная система нитрования ДНТ.
Анализ работы системы. Как уже отмечалось, вследствие низкой растворимости в кислотных смесях нитрование ДНТ до ТНТ протекает гетерофазной системе, состоящей из двух слоев – органического и минерального. Однако сама реакция нитрования из-за низкой реакционной способности ДНТ протекает в объеме минерального слоя между азотной кислотой и растворенным в кислотной смеси ДНТ, и ее скорость определяется законами химической кинетики, т.е. зависит в первую очередь от концентрации реагирующих компонентов – ДНТ и азотной кислоты.
Органический слой представляет собой сплав ДНТ и ТНТ. Данные по растворимости ДНТ и ТНТ в серной кислоте приведены в таблице
Растворимость ДНТ и ТНТ в 90% серной кислоте (%)
Температура, 0С |
ДНТ |
ТНТ |
50 |
16.8 |
3.5 |
70 |
20.0 |
7.0 |
90 |
20.6 |
11.0 |
Как видно из приведенных данных, ДНТ значительно лучше растворим в серной кислоте, чем ТНТ. Тем не менее, концентрация ДНТ в кислотной смеси мала, о чем свидетельствует низкий коэффициент распределения ДНТ между минеральной и органической фазами (0.3-0.4). Зависимость коэффициента распределения ДНТ между кислотной и органической фазами от концентрации серной кислоты и температуры приведена на рис. А и В. РисункиОрлова,стр.198
Как видно, увеличение концентрации серной кислоты приводит к повышению растворимости ДНТ и, соответственно, увеличению скорости нитрования, а повышение температуры – к некоторому снижению растворимости.
Однако по мере течения реакции и накопления (увеличения содержания) в органическом слое ТНТ растворимость (или концентрация!) ДНТ в кислотной смеси падает, что ведет к снижению скорости нитрования. В этом случае ДНТ распределяется между органическим и минеральным слоями в соответствии с растворимостью в них. Но, тем не менее ДНТ, как продукт, обладающий большей растворимостью, в большем количестве переходит в минеральный слой, чем ТНТ.
Таким образом, накопление ТНТ в органическом слое оказывает отрицательное влияние на процесс нитрования вследствие перехода ДНТ в органический слой и снижения его концентрации в кислотном слое. Однако это отрицательное влияние ТНТ на скорость нитрования несколько снижается в конце процесса при содержании ТНТ в органическом слое 90 и более %. По-видимому, при малой концентрации ДНТ в органическом слое и большей растворимостью его (по сравнению с ТНТ) в кислотной смеси последняя становится ненасыщенной по отношению к ДНТ.
Наиболее благоприятные условия нитрования ДНТ создаются в начале процесса, когда органический слой состоит из чистого ДНТ. Скорость процесса при этом максимальная.
Наименее благоприятные условия – в конце процесса, когда концентрация ДНТ в минеральном слое мала. Чтобы увеличить скорость нитрования в конце процесса, необходимо применять более концентрированную кислотную смесь (с большим ф.н.а.) и проводить его при более высокой температуре. В то же время в начале процесса, благодаря значительной концентрации ДНТ в кислотной смеси, можно применять более слабые кислотные смеси (с меньшим ф.н.а.) и проводить процесс при более низкой температуре. Таким образом, при организации процесса нитрования ДНТ до ТНТ целесообразно использовать противоток между нитруемым соединением и нитрующей кислотной смесью.
При изучении процесса нитрования ДНТ до ТНТ было установлено, что органический слой – сплав ДНТ с ТНТ – обладает высокой растворяющей способностью по отношению к азотной кислоте, что ведет к уменьшению концентрации HNO3 в минеральном слое и снижению скорости нитрования ДНТ. Этим объясняется и кажущееся снижение скорости нитрования при переходе от гомогенного процесса к гетерогенному. Коэффициент распределения азотной кислоты между минеральным и органическим слоями близок к единице, что указывает на большую степень поглощения (экстракции) азотной кислоты органическим слоем. С увеличением избытка азотной кислоты скорость нитрования ДНТ сначала увеличивается за счет повышения концентрации HNO3 в минеральном слое, а затем падает вследствие снижения степени превращения азотной кислоты в катион нитрония (уменьшение величины ф.н.а.).
При использовании в промышленных процессах в качестве серного компонента купоросного масла, тротил, поступающий на промывку, содержит значительное количество азотной кислоты (содержит преимущественно азотную кислоту) из-за низкой степени ионизации ее в минеральной фазе в нитрующий агент. Напротив, в олеумных процессах значительно большая часть азотной кислоты находится в ионизированном состоянии, что приводит к снижению ее содержания в органической фазе. В то же время применение для нитрования олеумных систем приводит к повышению растворимости в органической фазе серной кислоты. (О.к.: азотная кислота до 0.5%, серная кислота до 3.5%).
Описание процесса нитрования ДНТ до ТНТ в противоточном режиме
Процесс осуществляется в противоточно-прямоточной системе, содержащей до 11 реакторов. Реакторы с1 по 8 являются реакторами совмещенного типа со шнековыми подъемниками и спиральными сепараторами, нитрование в которых осуществляется в режиме противотока нитруемого ДНТ и кислотной смеси. Последние аппараты работают в режиме прямотока. Азотная кислота (меланж или концентрированная азотная кислота) дозируется во все аппараты с общим избытком 75 - 80% сверх теоретически необходимого. Серный компонент (безводная серно-азотная смесь, например, 95% H2SO4 и 5% HNO3, или 101.5-102 % олеум) дозируются в конец противоточной системы и частично в ее середину для выравнивания фактора нитрующей активности по аппаратам. Объемный модуль в нитраторах поддерживается не ниже 2.0-2.5 за счет рециркуляции отработанной кислоты. В реакционное отделение первого аппарата третьей фазы поступают ДНТ из сепаратора последнего аппарата второй фазы, меланж (конц. азотная кислота) и отработанная кислота из сепаратора второго аппарата третьей фазы. Реакционная масса шнековым подъемником передается в сепарационное отделение, где расслаивается. Третья отработанная кислота, содержащая растворенные ДНТ и ТНТ, поступает на вторую стадию, а нитропродукт самотеком направляется в реакционное отделение второго аппарата. Таким образом, ДНТ, постепенно нитруясь, приходит всю противоточную часть системы до 8 аппарата включительно.
Вследствие того, что в каждом аппарате происходит разбавление реакционной массы водой, выделяющейся при нитровании ДНТ, его окислении и «раскислении» (термическом разложении) азотной кислоты, фактор нитрующей активности кислотной смеси постепенно уменьшается от конца системы к ее началу от 96-98% (99-100%) до 89-90% (90-92%). Поэтому для выравнивания фактора нитрующей активности по аппаратам осуществляют дозировку серного компонента в середину системы. Поскольку по мере течения реакции концентрация ДНТ в растворе падает, то для повышения скорости реакции температура реакционной массы постепенно повышается от 75-850С в первом аппарате до 90-1000С в восьмом аппарате. С той же целью содержание азотной кислоты в аппаратах повышается от 2-4% в начале системы до 3.5-5.0% – в конце. Приведенные данные свидетельствуют о том, что в отличие от прямоточного процесса при нитровании ДНТ в режиме противотока нитруемого соединения и кислотной смеси по мере движения реакционной массы по системе аппаратов концентрация ДНТ подает, но одновременно возрастает и нитрующая активность кислотной смеси, что позволяет уменьшить избыток азотной кислоты, снизить температуру реакции по аппаратам, сократить время реакции и, наконец, за счет уменьшения скорости побочных окислительных реакций повысить выход целевого продукта.
Процесс нитрования ДНТ до ТНТ завершается в прямоточной части системы. Из последнего аппарата 8 противоточной части вся реакционная масса по перетоку самотеком поступает в 9-ый и далее в 10-ый и 11-ый аппараты. Температура в аппаратах прямоточной части постепенно повышается до 110-1150С. Одновременно происходит и увеличение концентрации азотной кислоты в реакционной массе до 6-7%, что способствует максимальной конверсии ДНТ в ТНТ. В сепараторе последнего совмещенного аппарата 11 отработанная кислота самотеком по перетоку направляется в последний аппарат 8 противоточной части системы, а кислый ТНТ поступает в аппарат промывки. Среднее время реакции составляет ~ 2 часа.
При повышении температуры до 1400С или загорании продукта содержимое аппаратов сбрасывается в аварийные емкости, заполненные водой.
Влияние окислов азота на процесс нитрования.
Организация противотока в последних аппаратах третьей фазы позволяет решить проблему борьбы с «белым веществом». Впервые образование «белого вещества» заметили при эксплуатации установок, полностью работающих в режиме противотока в кислотных смесях с ф.н.а. более 94%, содержащих менее 0.3-0.4% окислов азота. «Белое вещество» плохо растворимо в серной кислоте и отработанных кислотах и поэтому оседает в аппаратах в виде шлама, забивая перетоки и ухудшая теплопередачу в нитраторах. Являясь хорошим эмульгатором, поступая с отработанной кислотой, «белое вещество» может привести к нарушению сепарации на 2-й и 1-й стадиях.
При работе всей системы в режиме противотока и при дозировке серного компонента в конец системы серная кислота взаимодействует с окислами азота с образованием растворимой нитрозилсерной кислоты, «вымывая» их из реакционной массы. Таким образом, в последних аппаратах противоточной системы образуются безводные кислотные смеси, не содержащие окислов азота. Изменение состава реакционной массы оказывает влияние на характер протекающих окислительных процессов. Как уже отмечалось, при наличии в реакционной массе окислов азота происходит межмолекулярное окисление образующийся на первой стадии 2.4.6-тринитробензальдегида в 2.4.6-тринитробензойную кислоту. (которая затем декарбоксилируется в тринитробензол). При отсутствии окислов азота в практически безводной среде с низким содержанием азотной кислоты наряду с межмолекулярным окислением происходит внутримолекулярный окислительно-восстановительный процесс, приводящий к образованию 2-нитрозо - 4.6-динитробензойной кислоты, которая превращается в 3.3',5.5'-тетранитроазоксибензол–2.2'-дикарбоновую кислоту – «белое вещество».


Таким образом, образованию этого вещества препятствует быстрое превращение первичных продуктов окисления в карбоновые кислоты.
При наличии в реакционной массе достаточных количеств азотной кислоты и окислов азота вклад реакций, ведущих к образованию «белого вещества», снижается. Техническим приемом, который позволяет этого достичь, является перевод последних аппаратов нитрационной системы в режим прямотока. В этом случае за счет термического разложения реакционной массы содержание окислов азота поддерживается на необходимом уровне (не ниже 0.4%) и образование «белого вещества» почти не происходит.
Отделенный от отработанной кислоты тротил содержит значительное количество растворенной и эмульгированной кислоты и поэтому первоначально подвергается водной промывке, в процессе которой в водный слой наряду с минеральными кислотами частично переходят и органические соединения, растворимые в воде. Образующаяся при промывке «кислая» вода, содержащая 15-30% серной кислоты, поступает на разбавление отработанной кислоты 1 стадии, что позволяет полностью исключить сброс «кислых» вод в производстве ТНТ.
Очистка ТНТ-сырца
Тротил-сырец после промывки содержит до 6% примесей, состав которых приведен ниже.
2,4,6-тринитротолуол |
94,0 – 95,0% |
несимметричные изомеры ТНТ |
3.40 – 4.56 |
динитротолуолы |
0.75 – 1.10 |
1.3-динитробензол |
0.05 –0.1. |
1.3.5-тринитро м-ксилол |
0.05 – 0.1. |
1.3.5-тринитробензол |
0.20 – 0.40 |
2.4.6-тринитробензилнитрат |
0.25 – 0.35 |
2.4.6-тринитробензальдегид |
0.20 – 0.25 |
2.4.6-тринитробензойная кислота |
0.20 – 0.25 |
тетранитрометан |
0.2 – 0.40 |
пикриновая кислота |
0.50 –0.90 |
«белое вещество» |
0.30 – 0.35 |
Тротил-сырец перед очисткой имеет температуру затвердевания, равную 77,5-78,50С. Наличие до 6% примесей делает невозможным использование его в боеприпасах, т.к. при длительном хранении или при небольшом нагревании в нем происходит образование низкоплавкой эвтектической смеси («тротилового масла»), которое вытекает из изделия на его поверхность. При этом происходит нарушение сплошности заряда и, как следствие, отказы при использовании или преждевременные взрывы при выстреле.
Задачей очистки является удаление:
–– несимметричных изомеров ТНТ.
–– органических примесей кислого характера (тринитробензойной кислоты, пикриновой кислоты и т.д.), которые ухудшают качество продукта при хранении (разрушают мешки) и могут образовывать вещества повышенной опасности при взаимодействии с металлами,
–– полное удаление тетранитрометана, присутствие которого в товарном продукте не допускается из-за высокой токсичности.
Краткая характеристика методов очистки ТНТ
Все методы очистки ТНТ можно подразделить на физические и химические методы.
Физические методы. Первоначально широкое применение нашли физические методы очистки, основной их которых – перекристаллизация из растворителей. Сущность метода состоит в том, что при растворении при повышенной температуре получают раствор, насыщенный по отношению к -ТНТ, и не насыщенный по отношению к примесям. Поэтому при охлаждении такого раствора основная масса ТНТ выпадает из раствора, а примеси остаются в растворе.
Перекристаллизация из спирта. По этому методу ТНТ-сырец растворяли в этаноле в соотношении 1:4 при 70-800С, полученный раствор пропускали через druck-фильтр (фильтровали под давлением) для удаления нерастворенных примесей и далее охлаждали в кристаллизаторе при перемешивании и охлаждении. Кристаллический ТНТ отфильтровывали на центрифуге, промывали водой и высушивали. Маточный раствор разбавляли водой и выделившееся «тротиловое масло» использовали для приготовления аммиачно-селитренных ВВ. Выход 80-85%.
Достоинства метода. 1. Высокое качество ТНТ. 2. Отсутствие неутилизируемых отходов, т.к. «тротиловое масло» использовалось для приготовления аммонитов, а этиловый спирт направлялся на регенерацию.
Недостатки метода. 1. Низкая производительность метода. 2. Низкий выход (не более 85%) ТНТ из-за высокой растворимости ТНТ в спирте. 3. Повышенная пожароопасность процесса очистки. 4. Большие потери растворителя.
Позднее чистый этиловый спирт для снижения растворимости в нем ТНТ был заменен смесью этанол-толуол (1:2-3).
Рассматривалась замена этанола на толуол или ксилол. При этом за счет лучшей растворимости ТНТ уменьшался расход растворителя, регенерацию которого проводили перегонкой с паром.
В опытных масштабах было реализовано предложение о частичной или полной замене огнеопасных растворителей непожароопасными, например, четыреххлористым углеродом или треххлористым этиленом. Однако введение хлорсодержащих растворителей резко повысило токсичность процесса, требовало применения особостойких сталей для аппаратуры, и несмотря на на высокий выход (с учетом «тротилового масла») 98% способы не нашли применения.
Оригинальной является попытка кристаллизовать -ТНТ из водной эмульсии тротила-сырца. По этому методу процесс осуществлялся при соотношении ТНТ-сырец : вода, равным 2.25:1, в каскаде из двух кристаллизаторов. Отделение -ТНТ от тротилового масла происходило на центрифуге. Выход целевого продукта с Т затв.= 80.45 – 80.550С составлял 75%.
Перекристаллизация из азотной кислоты (разбавленного меланжа). Процесс непрерывной кристаллизации проводили в каскаде из 4-5 аппаратов, первый из которых предназначен для получения раствора ТНТ-сырца в 63% азотной кислоте или разбавленном меланже с концентрацией по азотной кислоте 50-58% при 55-600С. Из аппарата-растворителя раствор поступал в последовательно расположенные кристаллизаторы, в которых охлаждался до 30-350С. Из последнего кристаллизатора суспензия ТНТ поступала на одну из параллельно работающих вакуум- воронок. Продукт отфильтровывали, промывали разбавленной азотной кислотой (меланжем), затем водой и направляли на окончательную промывку и сушку. Маточный раствор охлаждали до 15-200С или разбавляли кислой промывной водой. Выделившиеся нитропродукты (состав смеси: 50% 2.4.6-ТНТ, 30% несимметричных изомеров ТНТ, 20% изомеров ДНТ), на долю которых приходится до 15% исходного ТНТ-сырца, отфильтровывали, а разбавленная азотная кислота поступала на регенерацию. Метод обеспечивает выход очищенного ТНТ с Т. затв.= 80.2-80.30 до 88%
Недостатки способа. 1. Сложность аппаратурного оформления. 2. Большая продолжительность операций растворения, кристаллизации и промывки. 3. Недостаточно высокий выход продукта.
Использование этого метода целесообразно в том случае, когда высаженные из азотной кислоты продукты находят практическое применение.
Разновидностью физических методов очистки является очистка ТНТ, предварительно закристаллизованного под водой. По этому методу эмульсия ТНТ-сырца в горячей воде при перемешивании мощной рамной мешалкой медленно охлаждали до 30-350С. Особенность кристаллизации под водой состоит в том, что сначала при охлаждении расплава из массы ТНТ-сырца выкристаллизовывается -ТНТ, и на поверхности образовавшихся гранул осаждаются примеси, образуя низкоплавкие смеси. Кристаллизованный (гранулированный) ТНТ-сырец отфильтровывали на вакуум-воронке и промывали растворителями или горячей водой для удаления примесей.
Химические методы. С целью удаления примесей в настоящее время в промышленности используют химические методы очистки, основанные на переводе примесей в растворимые в воде соединения путем воздействия на них различными реагентами. Наиболее широкое применение получили сульфитная и перекисная очистки тротила-сырца.
Сульфитная очистка
При взаимодействии водного раствора сульфита натрия с «несимметричными» изомерами тринитротолуола нитрогруппа, стоящая в мета-положении к метильной и в орто-положении к другой нитрогруппе, замещается сульфогруппой с образованием растворимых в воде натриевых солей динитротолуолсульфокислот
Достаточно легко взаимодействует с сульфитом натрия тетранитрометан, образуя хорошо растворимую в воде натриевую соль тринитрометана.
С(NO2)4 + 2 Na2SO3 + H2O = Na+ C—(NO2)3 + NaNO2 + 2 NaHSO4
С 1,3,5 - тринитробензолом сульфит натрия образует аддитивные соединения, переходящие в водную фазу.
С6H3(NO2)3 + Na2SO3 = C6H3(NO2)3.3 Na2SO3
В условиях очистки тротила-сырца изомеры динитротолуола, и продукты нитрования спутников толуола (в первую очередь ДНБ) с сульфитом натрия практически не взаимодействуют.
Водный раствор сульфита натрия имеет щелочную реакцию. Поэтому образовавшиеся в процессе окисления органические примеси кислого характера (пикриновая кислота, тринитробензойная кислота, тринитрокрезол, «белое вещество» и т.д. ), а также тринитробензальдегид и тринитробензилнитрат, растворяются в разбавленных водных растворах сульфита натрия. Одновременно происходит и нейтрализация остатков минеральных кислот.
Сам -тринитротолуол
при низких температурах взаимодействует
с водными растворами сульфита натрия
очень медленно с образованием растворимых
в воде комплексов, которые распадаются
на исходные продукты при разбавлении
водой или подкислении. Так, при 200C
в 3% растворе сульфита натрия растворяется
0,3% -тринитротолуола,
в 6% растворе–0,6% и в 12% растворе–2,3%
![]() -тринитротолуола.
С повышением концентрации раствора и
температуры скорость взаимодействия
возрастает и сопровождается химической
реакцией, в результате которой
-тринитротолуол
полностью превращается в водорастворимое
соединение. Разбавление водой или
подкисление подобных растворов уже не
приводит к регенерации исходного
соединения.
-тринитротолуола.
С повышением концентрации раствора и
температуры скорость взаимодействия
возрастает и сопровождается химической
реакцией, в результате которой
-тринитротолуол
полностью превращается в водорастворимое
соединение. Разбавление водой или
подкисление подобных растворов уже не
приводит к регенерации исходного
соединения.
В существующих методах сульфитной очистки потери -тринитротолуола составляют 3-4%, т.е. по абсолютной величине близки к сумме удаляемых «несимметричных» изомеров тринитротолуола.
Таким образом, в результате сульфитной очистки получают тротил, содержащий в качестве примесей динитротолуолы и продукты нитрования спутников толуола—динитробензол, тринитроксилолы и тринитроэтилбензол.
Количество неудаляемых в процессе очистки примесей (главным образом, динитротолуолов и динитробензола) зависит от качества исходного толуола и совершенства технологического процесса нитрования, и их содержание в товарном продукте строго регламентировано.
В зависимости от концентрации этих соединений в тротиле-сырце для достижения необходимого качества товарного продукта можно использовать различные варианты сульфитной очистки.
Сульфитная очистка тротила, предварительно закристаллизованного под слоем воды. При содержании неудаляемых примесей, превышающем допустимую норму в товарном продукте, для очистки применяют ТНТ-сырец, предварительно закристаллизованный под слоем воды. Сущность метода состоит в следующем: в процессе медленной кристаллизации расплавленного тротила под водой примеси осаждаются на поверхности кристаллов тротила и таким образом становятся доступны действию сульфита натрия. Очистка закристаллизованного под водой продукта производится в два этапа: сначала при 56-580С водную суспензию гранулированного тротила обрабатывают 2,5-3,0% раствором сульфита натрия для удаления основной части примесей, реагирующих с сульфитом натрия; затем очищенный продукт отфильтровывают и промывают на фильтре горячей (60-650С) водой для того, чтобы смыть с поверхности кристаллов легкоплавкой смеси, содержащей примеси, не взаимодействующие с сульфитом натрия (ДНТ и продукты нитрования спутников толуола, прежде всего ДНБ).
Стадия кристаллизации ТНТ под слоем воды определила основные недостатки этого способа – большую продолжительность процесса, громоздкость и каскадность аппаратуры.
Применение столь сложной технологии было вызвано низким качеством толуола и несовершенством процесса нитрования. Эти факторы привели к тому, что тротил-сырец содержал значительные количества ДНТ и ДНБ (не удаляются в процессе очистки), которые снижали качество ТНТ и являлись препятствием на пути внедрения очистки в расплаве.
Повышение качества толуола и создание олеумного процесса, при котором снизилось до ….суммарное содержание ДНТ в тротиле-сырце создало предпосылки для внедрения непрерывной очистки в расплаве.
Необходимость проведения медленной кристаллизации, многочисленных промывок растворами сульфита натрия и водой делали стадию очистки малопроизводительной и трудноподдающейся автоматизации. Однако разрабатываемые в 40-х и 50-х годах методы непрерывной очистки в расплаве не позволяли внедрить этот способ в промышленность из-за больших потерь ТНТ и неудовлетворительного качества продукта. Только в начале 60-х годов был разработан и внедрен усовершенствованный вариант процесса сульфитной очистки в расплаве, чему способствовало создание олеумного процесса нитрования, при котором содержание ДНТ в ТНТ-сырце снизилось до 0.3%.
Сульфитная очистка расплавленного тротила. Если количество динитробензола и динитротолуолов в тротиле-сырце соответствует требованиям ГОСТ по содержанию этих примесей в товарном продукте, то для очистки используют водную эмульсию расплавленного продукта. Установлено, что сульфитная очистка расплавленного тротила протекает в минеральном слое на границе раздела фаз и ее скорость зависит от интенсивности перемешивания (т.е. поверхности контакта реагирующих компонентов). В условиях очистки взаимодействие сульфита натрия с -тринитротолуолом протекает в кинетическом режиме (т.е. процесс лимитируется скоростью химического взаимодействия), в то время как реакция с «несимметричными» изомерами, тринитробензолом и тетранитрометаном происходит настолько быстро, что суммарная скорость их взаимодействия лимитируется скоростью диффузии компонентов в зону реакции. С целью уменьшения продолжительности процесса и снижения потерь -тринитротолуола из-за высокой температуры реакции очистку проводят в тонко эмульгированной реакционной массе и при температуре 78-790С, близкой к температуре затвердевания тротила (как известно, температура затвердевания под водой на 3,50С ниже температуры затвердевания сухого очищенного тротила).
Маточный сульфитный щелок и промывные воды после сульфитной очистки нельзя смешивать с кислыми промывными водами.
Сульфитные воды содержат натриевые соли динитротолуолсульфокислот, нитрит натрия NaNO2 и сульфит натрия Na2SO3. При смещении этих вод с кислой промывной водой, содержащей серную кислоту, образуются NaHSO3 и SO2, которые восстанавливают динитротолуолсульфокислоты; при этом образуются нитроаминосульфокислоты, которые в избытке минеральной кислоты и нитрита натрия диазотируются с образованием нитродиазотолулосульфокислоты:
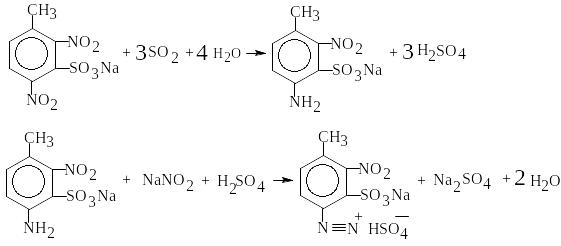
Образование этой кислоты в производстве тротила является очень опасным. Нитродиазотолуолсульфокислота нестойка к температурным воздействиям и очень чувствительна к удару.
Описание технологического процесса сульфитной очистки ТНТ в расплавленном состоянии.
Промытый от кислот расплавленный ТНТ подвергается очистке сульфитом натрия на установке непрерывного действия, которая состоит из основного и буферного аппаратов очистки и нескольких промывных аппаратов совмещенного типа. Основной реактор представляет собой цилиндрический аппарат со сферическим днищем и крышкой, снабженный рубашкой и мешалкой (n=450 об/мин.).
Эмульсия расплавленного ТНТ в горячей оборотной воде из мастерской нитрации инжектируется в сепаратор мастерской очистки. Оборотная вода далее поступает в приемник и возвращается в мастерскую нитрации, а ТНТ через расходомер дозируется в основной реактор очистки. Одновременно с ТНТ в реактор дозируются 15-20% раствор сульфита натрия промывная вода из сепаратора первого промывного аппарата и часть маточного щелока из буферного аппарата для создания необходимого модуля 1:1–2. Процесс очистки протекает в минеральной фазе, поэтому с технологической точки зрения выгодно иметь относительно высокий модуль. Реакционная масса из основного реактора самотеком поступает в реакционную зону буферный аппарат, где смешивается с водой, поступающей из сепаратора первого промывного аппарата. Из реакционной зоны реакционная масса (эмульсия ТНТ) шнековым подъемником передается в сепаратор, где происходит отделение ТНТ и маточного щелока. Из сепаратора ТНТ по перетоку поступает в зону промывки первого промывного аппарата, а сульфитный щелок, проходя через дополнительный сепаратор, частично направляется в основной реактор для создания необходимого модуля, а остальная часть в ловушку, откуда перекачиваются на установку сжигания.
В сепараторе буферного аппарата реакционная масса разделяется. Сульфитные щелока, проходя через дополнительный сепаратор, частично направляются в основной реактор для создания необходимого модуля, а остальная часть в ловушку, откуда перекачиваются на установку сжигания. Очищенный ТНТ из буферного реактора проходит систему промывных аппаратов, где в противотоке промывается горячей водой с температурой 85-950С
Одновременно с ТНТ в зону промывки первого промывного аппарата поступает вода из сепаратора второго промывного аппарата. В последний промывной аппарат дозируется вода с температурой 85-950С. Вода противотоком к ТНТ проходит все промывные аппараты и поступает в реактор. Из сепаратора последнего промывного аппарата ТНТ поступает в приемник готового продукта, откуда инжектируется оборотной водой в мастерские чешуирования или гранулирования. Поскольку водный раствор сульфита натрия имеет щелочную реакцию, для инжектирования применяют подкисленную воду, содержащую 0.1-0.3% серной кислоты, для предотвращения образования «тротилатов» при сушке продукта.
Температурный режим по аппаратам: основной и буферный реакторы –– 78-820С, промывные аппараты – 85-950С. Повышение температуры в аппаратах очистки приводит к увеличению потерь -ТНТ за счет необратимого взаимодействия его с сульфитом натрия.
Содово-сульфитный метод очистки. При получении ТНТ для пром. ВВ в настоящее время используется содово-сульфитный метод очистки, в котором часть сульфита натрия, расходуемая на нейтрализацию минеральных и органических кислот, заменена карбонатом натрия. (Карбонат-ион по сравнению с сульфит-ионом является более сильным основанием, но он не способен взаимодействовать с несимметричными изомерами ТНТ и может заменить сульфит натрия только в реакции с кислыми примесями).Сода является более дешевым продуктом, что позволяет снизить стоимость затрат на сырье.
Недостатки сульфитной очистки.
1. Значительные потери -ТНТ.
2. Безвозвратные потери несимметричных изомеров ТНТ.
3. Образование высокотоксичных сульфитных щелоков и проблема их утилизации.
Перекисная очистка.
Все содержащиеся в ТНТ-сырце примеси могут быть подразделены на две группы.
В первую группу входят несимметричные изомеры ТНТ, динитротолуол, тринитробензол и продукты нитрования спутников толуола, содержание которых может достигать 5%. По химической стойкости и взрывчатым характеристикам они близки к -ТНТ.
Вторая группа примесей – органические соединения кислого характера, куда входят 2.4.6-тринитробензойная кислота, 2.4.6- тринитробензальдегид, нитрофенолы, нитрокрезолы и другие окси- и карбокси производные толуола и бензола. Они отличаются от -ТНТ меньшей химической и термической стойкостью и могут образовывать (при взаимодействии с оболочкой боеприпаса) металлические производные, обладающие высокой чувствительностью к механическим воздействиям и низкой температурой вспышки.
Кроме указанных соединений в ТНТ-сырце присутствует тетранитрометан (до 1%), присутствие которого в товарном продукте недопустимо из-за высокой токсичности.
Поэтому при получении ТНТ для пром ВВ основной задачей очистки является удаление из тротила-сырца тетранитрометана и органических примесей кислого характера. Эта задача была решена применением для очистки перекиси водорода.
Перекись водорода (точнее, гидропероксид-ион ООН) количественно реагирует с тетранитрометаном, содержащемся в тротиле-сырце, и не взаимодействует с другими примесями. Реакция протекает в минеральном слоена границе раздела фаз и общая скорость процесса определяется скоростью диффузии компонентов в зону реакции. Продуктами реакции являются хорошо растворимая в воде соль нитроформа, неорганический нитрит и кислород.
C(NO2)4
+ H2O2
= HC(NO2)3
+ HNO2
+ O2![]()
Процесс перекисной очистки осуществляют в расплаве при 78-800С и рН среды 6,9-7,2, которая поддерживается дозировкой к водной эмульсии тротила-сырца раствора соды для нейтрализации и перевода в раствор кислых примесей минерального и органического характера.
Тротил после перекисной очистки содержит «несимметричные» изомеры тринитротолуола, динитротолуолы, тринитробензол, продукты нитрования спутников толуола ( бензола, ксилолов и этилбензола ) и после стабилизации «тротилового масла» может быть использован для приготовления промышленных взрывчатых веществ.
Описание технологического процесса перекисной очистки ТНТ.
Перекисная очистка осуществляется на том же оборудовании, что и сульфитная очистка. В основной реактор очистки дозируются водная перекись водорода и водный раствор соды. Поскольку процесс очистки протекает в диффузионном режиме, то поддерживается относительно высокий модуль 1–2:1 за счет подачи части маточника из буферного реактора (а также промывной воды из первого аппарата промывки). Концентрация перекиси водорода в реакционной массе 0.2-0.3%. Процесс очистки завершается в буферном реакторе, куда дозируется промывная вода из сепаратора первого промывного аппарата. Промывка ТНТ проводится по той же схеме, что и при сульфитной очистке. С цель снижения количества щелоков, направляемых на сжигание, часть промывных вод (до 20%) может быть использована для кислой промывки ТНТ или разбавления реакционной массы на первой стадии. Содержащийся в промывных водах нитроформ в значительной части разлагается, а оставшаяся часть (0.01-0.02%) не оказывает влияния на процесс регенерации первой отработанной кислоты.
После очистки ТНТ инжектируется в мастерскую сушки. Процесс стабилизации совмещен с сушкой продукта и проводится в сушильной ванне, куда добавляется измельченный стабилизатор (например триацетат целлюлозы, ТАЦ), который хорошо растворим в расплавленном ТНТ. Из сушильной ванны стабилизированный и высушенный ТНТ поступает на чешуирование или грануляцию. Содержание ТАЦ в ТНТ составляет 0.7%. Фактическое увеличение выхода ТНТ (за счет присутствия в нем неудаляемых примесей, главным образом несимметричных изомеров ТНТ) составляет 3-4%.
Механизм стабилизирующего действия ТНЦ. При повышенных температурах внутри заряда появляется жидкое «тротиловое масло», которое хорошо растворяет ТАЦ. Повышенная вязкость «тротилового масла», содержащего ТАЦ, препятствует эксудации его на поверхности заряда. При понижении температуры «тротиловое масла» и ТАЦ выкристаллизовываются и система возвращается в первоначальное состояние. Таким образом, при нормальных условиях ТАЦ выполняет роль обычного наполнителя, несколько армируя заряд и повышая его прочность, а при повышенной температуре является (выполняет роль) температурного демпфера, снижая подвижность жидкой фазы.
Сравнительный анализ маточников сульфитной и перекисной очистки.
Тип очистки |
Удельный объем маточников, л/т |
Концентрация, % |
Плотный остаток после выпарки, кг/ |
Шлак после сжигания, кг/т |
Сульфитная |
250-300 |
30.0-35.0 |
75.0-90.0 |
100 |
Перекисная |
130-150 |
8.0-10.0 |
15.0 |
10 |
Состав газовой фазы
Тип очистки |
Окислы в |
продуктах |
сжигания, г/м3 |
|
SO2 |
SO3 |
NO |
Сульфитная |
0.56 |
0.51 |
0.32 |
Перекисная |
–– |
–– |
0.08 |
Очистка ТНТ перекисью водорода значительно снижает экологическую опасность производства. Основное отличие состоит в том,
––объем токсичных выбросов снижается в 18 раз, в том числе полностью исключается выброс оксидов серы;
––количество шлака после сжигания уменьшается в 10 раз.
Из кольца инжектирования ТНТ из мастерской нитрации в мастерскую очистки – вода для кислой промывки ТНТ. Из кольца инжектирования ТНТ из мастерской очистки в мастерскую сушки – вода для промывки ТНТ после очистки.
Технология получения ТНТ фирмы «Bofors»
Один из наиболее известных процессов фирмы «Бофорс» включает следующие стадии: нитрование толуола до тротила, промывка продукта от кислот, сульфитная очистка тротила, промывка после очистки, сушка и чешуирование.
Процесс нитрования толуола до тротила полностью противоточный. Нитрационная система состоит из семи аппаратов совмещенного типа, снабженных динамическими сепараторами (центрифугами), расположенными на валу мешалки, и змеевиками. Условно можно принять, что процесс мононитрования протекает в первом и втором аппаратах, динитрование завершается в третьем и четвертом аппаратах, а образование тринитротолуола завершается в аппаратах с пятого по седьмой. В качестве серного компонента используется олеум, который дозируется в последний (седьмой) аппарат системы и проходит противотоком к нитруемому продукту до первого аппарата включительно. Фактор нитрующей активности кислотной смеси постепенно повышается от 70% в первом аппарате до 96-98% в последнем аппарате. 98% азотная кислота дозируется во все аппараты кроме первого. Процесс характеризуется очень высоким содержанием азотной кислоты в отработанной кислоте по аппаратами (по-видимому, для интенсификации процесса нитрования), что приводит к значительной растворимости в ней нитропродуктов и обуславливает ряд его особенностей, в частности, введение стадии экстракции отработанной кислоты толуолом.
В нитратор 1 первой стадии дозируются толуол (85% от общего количества), 55% азотная кислота и отработанная кислота из сепаратора второго аппарата. Температура 30-400С. Из сепаратора этого аппарата нитропродукт, (содержащий, по-видимому, наряду с толуолом и МНТ также ДНТ и ТНТ) поступает во второй аппарат первой фазы, а отработанная кислота – в экстрактор, куда одновременно дозируется толуол (15% от общего количества.).
Отработанная кислота имеет следующий состав: серная кислота 70 2%, азотная кислота 8 1%, азотистая кислота 4 05%, вода 18%.
Экстракция производится при 20-300С. Из сепаратора экстрактора проэкстрагированная отработанная кислота, содержащая 68 1% серной кислоты, 5 1% азотной кислоты, 4.0 0.5% азотистой кислоты и 22% воды, поступает в приемник. Как видно, при 20-300С только часть азотной кислоты из о.к. расходуется на нитрование толуола, что предотвращает протекание процессов, ведущих к получению «черной» кислоты.
В реакционную зону второго аппарата кроме нитропродукта дозируются 55% азотная кислота, 98% азотная кислота и отработанная кислота из сепаратора третьего аппарата. После отделения в сепараторе отработанная кислота направляется для приготовлении кислотной смеси в первый аппарат, а нитропродукт – в реакционное отделение третьего аппарата и далее проходит в режиме противотока до седьмого аппарата. В каждый реактор подают отработанную из сепаратора последующего реактора и нитропродукт из сепаратора предыдущего аппарата. Т.к. реакция нитрования осуществляется в минеральной фазе, то увеличение объема последней способствует росту скорости процесса. Для этого в системе предусмотрен возврат части о.к. от линии о.к. в реакционную часть аппарата.
Температура нитрования постепенно повышается от 550С во втором аппарате до 1030С – в седьмом аппарате.
Процесс протекает при большом избытке азотной кислоты. Концентрация азотной кислоты в отработанной кислоте аппаратов 2-7 составляет 8-9%, концентрация азотистой кислоты в аппаратах 1-4 примерно 4-5%, в аппаратах 5-7 снижается с 2% до 0.5%. По-видимому, высокая концентрация азотной кислоты и окислов азота в последних аппаратах системы направляет окислительные процессы в сторону от образования «белого вещества».
Промывка ТНТ. «Кислая» промывка тротила производится в двух аппаратах в режиме противотока при 80-860С. Вода с температурой 90-950С подается во второй аппарат. Кислая вода, содержащая примерно 15% серной кислоты и 2% азотной кислоты, из сепаратора первого аппарата поступает на разбавление реакционной массы в аппарат первой фазы 2, а промытый тротил из сепаратора второго промывного аппарата по перетоку самотеком направляется на сульфитную очистку.
Сульфитная очистка ТНТ. Сульфитная очистка тротила производится в системе из двух аппаратов в режиме противотока. В первый аппарат очистки поступают тротил после кислой промывки и маточный сульфитный щелок из второго аппарата очистки. После разделения в сепараторе первого аппарата маточный сульфитный щелок поступает на уничтожение, а тротил по перетоку самотеком направляется в реакционное отделение второго аппарата, куда также дозируются водный раствор сульфита натрия и промывная вода со стадии окончательной промывки. Из сепаратора второго аппарата очищенный тротил поступает на стадию окончательной промывки, а сульфитный щелок в первый аппарат очистки. В первом аппарате очистки 86-880С, во втором – 86-900С.
Окончательная промывка. Окончательная промывка производится в двух аппаратах в противоточном режиме при 86-900С. Промывная вода направляется по перетоку самотеком в реакционное отделение второго аппарата очистки, расплавленный тротил – по обогреваемому трубопроводу в сушильную ванну и далее на барабан чешуирования.






