
- •Изменение состава кислотной смеси с ф.Н.А 80%.
- •Кислотооборот
- •Технология мононитротолуола,
- •Состав и основные физико-химические свойства нитротолуола.
- •Состав побочных продуктов нитрования толуола
- •Описание технологического процесса получения мнт.
- •Технология получения 2.4-динитротолуола и смеси 2.4-/2.6-динитротолуолов (65/35%).
- •Описание технологического процесса получения 2.4-днт.
- •Состав «сырого» мнт, %.
- •Состав «черной» отработанной кислоты, %.
- •Основные физико - химические свойства несимметричных изомеров тринитротолуола
- •Требования к качеству тротила
- •Описание технологического процесса.
Основные физико - химические свойства несимметричных изомеров тринитротолуола
При нитровании толуола до тринитротолуола наряду с 2,4,6 - тринитротолуолом образуется ряд (пять) несимметричных изомеров тринитротолуола, содержащих нитрогруппу в мета - положении по отношению к метильной группе. Содержание несимметричных тринитротолуолов в тротиле - сырце достигает 4,5% - 5,0%.Физические свойства этих соединений подобны свойствам -тринитротолуола. Все они представляют собой кристаллические вещества светло - желтого цвета, негигроскопичны, легко растворимы в большинстве органических растворителях и практически не растворимы в воде.
Подобно -тринитротолуолу несимметричные изомеры окисляются при повышенной температуре азотной кислотой или серно-азотными смесями с образованием тринитробензойных кислот, но в отличие от 2.4.6-тринитробензойной кислоты при нагревании с горячей водой превращаются в динитрооксибензойные кислоты:
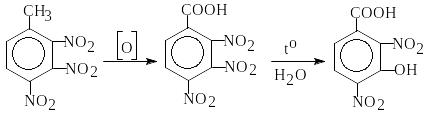
Несимметричные тринитротолуолы легко реагируют с водными растворами КОН или NaOH, при этом происходит нуклеофильное замещение нитрогруппы, находящейся в мета - положении к метильной группе, на гидроксильную группу и образование динитрокрезола:
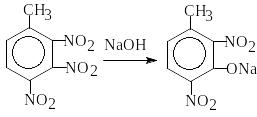
При действии алкоголятов натрия или калия в спиртовом растворе нитрогруппа замещается на алкоксигруппу:

Реакция с аммиаком и аминами также приводит к аналогичной замене подвижной нитрогруппы и получению динитротолуидина или его производного, замещенного по атому азота:

Несимметричные тринитротолуолы легко взаимодействуют даже при низкой температуре с водным раствором сульфита натрия Na2SO3, превращаясь в растворимые в воде натриевые соли динитротолуолсульфокислот:
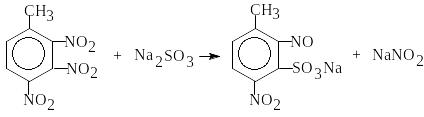
Образующийся раствор натриевой соли динитротолуолсульфокислоты имеет характерный розовый цвет. Эта реакция имеет большое практическое значение и используется для удаления несимметричных тринитротолуолов из тротила - сырца.
По своим взрывчатым характеристикам несимметричные изомеры близки к 2,4,6 - тринитротолуолу, но отличаются от него более низкой химической и термической стабильностью. Кроме того, они образуют с - тринитротолуолом низкоплавкие эвтектические смеси (тротиловое масло), которые ухудшают служебные качества тротила.
Требования к качеству тротила
Основными примесями тротила, содержащимися в нем в значительных количествах, являются несимметричные изомеры тринитротолуола и недонитрованные динитротолуолы. Кроме того, технический тротил содержит в небольших количествах продукты окисления (включая тетранитрометан), а также продукты нитрования спутников толуола.
Содержащиеся в тротиле - сырце примеси снижают температуру затвердевания тротила до 75 - 770С и, кроме того, образуют с - тринитротолуолом многокомпонентные эвтектические сплавы с низкой температурой плавления, называемые «тротиловым маслом». При долговременном хранении снарядов, снаряженных тротилом - сырцом, особенно в условиях жаркого климата из них вытекает маслообразная жидкость - тротиловое масло. При стрельбе снарядами, снаряженными тротилом - сырцом и хранившимися некоторое время, наблюдается значительное количество неполных взрывов, отказов, а также преждевременных разрывов. Неполные взрывы и отказы связаны с тем, что тротиловое масло, имея меньшую плотность, чем тротил, и заполняя зазор между взрывателем и разрывным зарядом, весьма сильно флегматизирует последний, а в случае проникновения во взрыватель пропитывает промежуточный детонатор и делает его невосприимчивым к капсюлю - детонатору. Преждевременные разрывы обусловлены тем, что при вытекании из снарядов тротилового масла нарушается монолитность разрывного заряда, вследствие чего при выстреле могут произойти опасные перемещения взрывчатого вещества. Кроме того, причиной преждевременных разрывов может явится попадание тротилового масла в резьбовые соединения. («Течь» снарядов, снаряженных тротилом - сырцом, в условиях Средней Азии обнаруживается через 8 месяцев хранения.)
Готовый тротил должен удовлетворять определенным техническим условиям. Несмотря на имеющиеся в отдельных странах различия, большинство требований носят общий характер. Главными из них являются следующие.
Внешний вид: однородная масса в виде чешуек или гранул светло - желтого цвета, без посторонних механических включений.
Температура затвердевания: не менее 80,20С (характеристика содержания основного вещества)
Содержание влаги и летучих: не более 0,07%. Повышенное содержание влаги снижает восприимчивость тротила к детонации
Кислотность по серной кислоте: не более 0,01%. Повышенная кислотность снижает химическую стойкость тротила и вызывает коррозию оболочки боеприпаса.
Содержание веществ, нерастворимых в бензоле или толуоле: не более 0,1%, Повышенное содержание твердых нерастворимых примесей (например, песка или окалины) увеличивает чувствительность тротила к механическим воздействиям.
Содержание золы: не более 0,1%. Характеризует содержание твердых примесей, которые повышают чувствительность тротила к механическим воздействиям.
Содержание сульфита натрия: отсутствие.
Маслянистость: не более, чем у эталонного образца. Для определения маслянистости помещают цилиндр из тротила на фильтровальную бумагу и выдерживают определенное время при заданной температуре. Определяют диаметр пятна и потерю в массе образца.
ПРИМЕНЕНИЕ ТРОТИЛА
Тротил является самым распространенным бризантным взрывчатым веществом. В чистом виде он применяется для снаряжения артиллерийских снарядов, мин, авиабомб, а также для изготовления различных подрывных средств и промежуточных детонаторов. Методы снаряжения: прессование, шнекование, заливка. Весьма широко применяются различные смеси и сплавы тротила с аммиачной селитрой (аммотолы), гексогеном и др.
НИТРОВАНИЕ ТОЛУОЛА ДО МОНОНИТРОТОЛУОЛА
Мононитротолуол (МНТ) получают нитрованием толуола серно-азотными смесями по уравнению:
СН 3С6Н5 + НNО3 СН3С6Н4(NO2) + Н2О
Для получения МНТ используют кислотные смеси с фактором нит-рующей активности Ф, равном 70-73%. Учитывая высокую реакционную способность толуола и сравнительно низкую температуру нитрования, азотная кислота берется с избытком 3-5% сверх теоретически необходимого. Дальнейшее уменьшение избытка азотной кислоты приводит не только к снижению скорости образования МНТ, но и к заметному падению выхода продукта, вследствие протекания побочной реакции толуола с нитрозилсерной и серной кислотами с образованием «комплекса Баттге».
(СН3С6Н5) (NOSO4H)2 (H2SO4)3
Последний хорошо растворим в отработанной кислоте и при температуре выше 60-65оС легко окисляется и осмоляется, вызывая потемнение реакционной массы. При наличии в реакционной среде азотной кислоты и температуре ниже 600 С комплекс Баттге, если и образуется, то необратимо превращается в мононитротолуол.
При нитровании толуола образуются все три возможные изомеры МНТ:
-
орто-МНТ
мета-МНТ
пара-МНТ
На изомерный состав МНТ значительное влияние оказывает температура нитрования: при ее повышении содержание мета- и орто-изомеров увеличивается, а содержание пара- изомера — уменьшается, что видно из приведенных ниже данных.
Кроме температуры реакции на количественное соотношение образующихся изомеров МНТ оказывает влияние состав кислотной смеси. Так, увеличение фактора нитрующей активности кислотной смеси с 70% до 76% при 200С сопровождается снижением содержания мета- изомера с 4,5% до 3,9%.
Из орто и пара МНТ получ ТНТ. Из мета МНТ несимметричные изомеры ТНТ, что вызывает необходимость спец. очистки.
Продукт нитрования толуола до мононитротолуола содержит в качестве основных примесей 2,6-динитро-р-крезол, 2,4-динитро-о-крезол, 2,4-динитрофенол, 3-нитро-4-гидроксибензойную кислоту
Содержание этих примесей в техническом продукте достигает 0.3-0.7%. Основной 2.6-динитро-п-крезло (70-80%).
МНТ практически не растворим в воде и хорошо растворяется в органических растворителях. Растворимость МНТ в серной кислоте возрастает с увеличением ее концентрации и температуры, и в 75% серной кислоте составляет 0,81%.
Нитрование толуола до МНТ является гетерофазным процессом, что связано с низкой растворимостью толуола в применяемых серно-азотных смесях. Так, растворимость толуола в 70–75% серной кислоте при 200С составляет 0,021–0,027%, и присутствие в кислоте такой концентрации даже небольших количеств азотной кислоты и окислов азота приводит к дальнейшему снижению растворимости. Минеральный слой этой гетерофазной системы наряду с серной и азотной кислотами и водой содержит растворенные органические вещества. Органический слой представляет собой гомогенную смесь толуола, МНТ и азотной кислоты, причем с повышением содержания МНТ количество азотной кислоты, перешедшее в органическую фазу, возрастает. В реальных системах в органический слой переходит значительная (вплоть до половины) часть азотной кислоты, в то время как серная кислота в нем практически отсутствует.
Наличие большого количества азотной кислоты в органическом слое позволило предположить, что в нем также должен протекать процесс нитрования. Однако установлено, что скорость реакции в органическом слое на несколько порядков ниже, чем в минеральном, и доля процессов, в нем протекающих, не превышает 0,001% от суммарного превращения.
Скорость нитрования толуола в этой гетерофазной системе резко возрастает с увеличением интенсивности перемешивания (т.е. увеличением поверхности раздела фаз). Эти данные свидетельствуют о том, что суммарная скорость нитрования определяется скоростью массопереноса с последующей быстрой химической реакцией.
Приведенные выше данные показывают, что нитрование толуола серно-азотными смесями в гетерогенных условиях протекает в минеральном слое и зона реакции расположена вблизи поверхности раздела фаз. В этом случае суммарный процесс включает следующие стадии:
1. диффузию компонентов в зону реакции;
2. быструю химическую реакцию между толуолом и азотной кислотой с образованием МНТ;
3. диффузию образовавшихся продуктов (в т.ч. мононитротолуола) из зоны реакции к поверхности раздела фаз и затем вглубь капли органической фазы;
