
- •2. Навчальні цілі:
- •3.Матеріали доаудиторної та аудиторної самостійної роботи
- •Ііі етап – закріплення знань та навичок
- •4.Додаткові завдання (матеріали позааудиторної роботи)
- •2. Навчальні цілі :
- •3.Матеріали доаудиторної та аудиторної самостійної роботи
- •Ііі етап – закріплення знань та навичок
- •4.Додаткові завдання (матеріали позааудиторної роботи)
- •2. Нуклеїнові кислоти.
- •2. Навчальні цілі :
- •3.Матеріали доаудиторної та аудиторної самостійної роботи
- •Ііі етап – закріплення знань та навичок
- •4.Додаткові завдання (матеріали позааудиторної роботи)
- •Навчальні цілі:
- •3.Матеріали доаудиторної та аудиторної самостійної роботи
- •Ііі етап – закріплення знань та навичок
- •4.Додаткові завдання (матеріали позааудиторної роботи)
- •2. Задачі на дигібридне та полігібридне схрещювання не зцеплених генів.
- •2. Навчальні цілі:
- •3.Матеріали доаудиторної та аудиторної самостійної роботи
- •Ііі етап – закріплення знань та навичок
- •4.Додаткові завдання (матеріали позааудиторної роботи)
- •2. Навчальні цілі :
- •3.Матеріали доаудиторної та аудиторної самостійної роботи
- •Ііі етап – закріплення знань та навичок
- •4.Додаткові завдання (матеріали позааудиторної роботи)
- •2. Навчальні цілі :
- •3.Матеріали доаудиторної та аудиторної самостійної роботи
- •Ііі етап – закріплення знань та навичок
- •4.Додаткові завдання (матеріали позааудиторної роботи)
- •2. Навчальні цілі :
- •3.Матеріали доаудиторної та аудиторної самостійної роботи
- •Ііі етап – закріплення знань та навичок
- •4.Додаткові завдання (матеріали позааудиторної роботи)
- •2. Навчальні цілі :
- •3.Матеріали доаудиторної та аудиторної самостійної роботи
- •Ііі етап – закріплення знань та навичок
- •4.Додаткові завдання (матеріали позааудиторної роботи)
- •2. Навчальні цілі :
- •3.Матеріали доаудиторної та аудиторної самостійної роботи
- •Ііі етап – закріплення знань та навичок
- •4.Додаткові завдання (матеріали позааудиторної роботи)
- •2. Навчальні цілі :
- •3.Матеріали доаудиторної та аудиторної самостійної роботи
- •Ііі етап – закріплення знань та навичок
- •4.Додаткові завдання (матеріали позааудиторної роботи)
- •2 Години
- •2. Навчальні цілі :
- •3.Матеріали доаудиторної та аудиторної самостійної роботи
- •Ііі етап – закріплення знань та навичок
- •4.Додаткові завдання (матеріали позааудиторної роботи)
- •1. Методи лабораторної діагностики захворювань викликаних
- •2. Амеба кишкова ( Entamoeba coli )
- •3. Амеба ротова (Entamoeba gingivalis).
- •2 Години
- •2. Навчальні цілі :
- •3.Матеріали доаудиторної та аудиторної самостійної роботи
- •Ііі етап – закріплення знань та навичок
- •4.Додаткові завдання (матеріали позааудиторної роботи)
- •1. Збудник метагонімозу (Меtаgопітиs уоkоgаwаi)
- •2. Збудник нанофієтозу ( Nапорhіеtиs sаlтіпсоlа )
- •1. Збудник альвеококозу (Аlvеососсиs тиltіlосиlаris)
- •2. Збудник дифілоботріозу (Dірhуllоbоtrіum lаtит).
- •2. Навчальні цілі :
- •3.Матеріали доаудиторної та аудиторної самостійної роботи
- •Ііі етап – закріплення знань та навичок .Після вивчення теми необхідно:
- •4.Додаткові завдання (матеріали позааудиторної роботи)
- •1 Година
- •2. Навчальні цілі :
- •3.Матеріали доаудиторної та аудиторної самостійної роботи
- •Ііі етап – закріплення знань та навичок
- •4.Додаткові завдання (матеріали позааудиторної роботи)
- •1 Година
- •2. Навчальні цілі :
- •3.Матеріали доаудиторної та аудиторної самостійної роботи
- •Ііі етап – закріплення знань та навичок
- •4.Додаткові завдання (матеріали позааудиторної роботи)
Ііі етап – закріплення знань та навичок
Після вивчення теми необхідно
Знати
|
Вміти |
Як здійснюється хімічний та фермента-тивний синтез генів. Яке значення рекомбінантної ДНК – технології. Значення міжнародної програми «Геном людини» та як це вплинуло на вивчення геному людини. Геннотерапія , її завдання та деякі успіхи в лікуванні хвороб людини. |
Давати пояснення основним етапам хімічного та ферментативного синтезу генів які використовують в біотехнологічних дослідженнях. Визначати значення програми «Геном людини». Пояснювати, як використовують гену терапію для лікування деяких хвороб.
|
Значення картування хромосом. Основні методи , які використовують для картування хромосом. |
Пояснювати як складають генетичні карти хромосом, та розв’язувати задачі завдяки яким визначають порядок розміщення генів на хромосомі.
|
Заходи, які спрямовані на відслідко- вування виникнення і поширення спадкової патології . Речовини, які підвищують ефекти середовищних мутагенів. Речовини які здатні до захисту Геному людини від дії мутагенів. |
Відокремлювати серед речовин та сполук , ті які є антимутагенами , а які є комутагенами. Давати загальну характеристику генетич- ному моніторингу. |
4.Додаткові завдання (матеріали позааудиторної роботи)
БИОТЕХНОЛОГИЯ (мовою оригіналу)
( статья из БОЛЬШОЙ ЭНЦИКЛОПЕДИИ КИРИЛЛА И МЕФОДИЯ – 2003Г.)
( Дивись додаток № 4 .)
Додатки до СПРС № 6 :
Додаток № 1
Генна інженерія . Біотехнології.
Біотехнологія - використання живих організмів та біологічних процесів в промисловому виробництві. Напрямки : мікробіологічний синтез ферментів, вітамінів, амінокислот, антибіотиків та т. п. Перспективне промислове одержування інших біологічно – активних речовин (гормональних препаратів, сполук стимулюючих імунітет, та т. п.) за допомогою методів генної інженерії та культур тваринних та рослинних клітин.
Генна інженерія - галузь молекулярної біології і генетики, завдання якої - конструювання генетичних структур за заздалегідь наміченим планом, створення організмів із новою генетичною програмою. Виникнення генної інженерії стало можливим завдяки синтезу ідей і методів молекулярної біології, генетики, біохімії і мікробіології. Основні принципи генної інженерії були розроблені в 60-70-х роках XX сторіччя. Вони включали три основних етапи: а) отримання генетичного матеріалу (штучний синтез або виділення природних генів); б) включення цих генів у генетичну структуру, яка реплікується автономно (векторну молекулу ДНК), тобто створення рекомбінантної молекули ДНК; в) введення векторної молекули (з включеним у неї геном) у клітину-реципієнта, де вона вмонтовується в хромосомний апарат).
Експериментальне перенесення генів в інший геном називається трансгенезом. Він ґрунтується на технології рекомбінантної ДНК. В основі генної інженерії лежать різні методи маніпуляцій із молекулами ДНК.
Отримання генетичного матеріалу. У сучасній генетиці використовуються два способи синтезу генів поза організмом - хімічний і ферментативний. Для хімічного синтезу необхідно мати повністю розшифровану послідовність нуклеотидів ДНК. Вперше штучний ген синтезував індійський вчений Г. Корана (1970) . Це був ген аланінової тРНК дріжджів, який складався з 77 нуклеотидів.
Іншим прикладом хімічного синтезу є синтез гена, який кодує фермент розщеплення лактози. Синтезований у пробірці ген був вмонтований у плазміду і введений у бактерію; кишкова паличка набула здатності засвоювати лактозу.
Ген, отриманий внаслідок ферментативного синтезу, може функціонувати в бактеріальній клітині. На ньому синтезується iРНК, а потім білок. Під керівництвом
В. Енгельгардта був отриманий ген, який визначає синтез ферменту галактозидази. Цей ген вводили у фаг, при розмноженні якого в клітині одержали безліч копій, що забезпечило синтез великої кількості ферменту. Це має не тільки теоретичне, але й практичне значення, тому що галактозидаза застосовується в харчовій промисловості.
Синтезовано гени глобіну людини, кроля, голуба, деякі гени мітохондрій печінки пацюків і багато інших.
Так були синтезовані два гени, відповідальні за синтез ланцюгів інсуліну, їх уводили в геном кишкової палички, яка почала продукувати інсулін. Важливим досягненням генної інженерії є синтез гена соматостатину, який може функціонувати у мікробній клітині. Таким же методом під керівництвом Ю. О. Овчиннікова і М. П. Дубініна здійснений синтез генів, які кодують нейрогормони людини (лейцин-енкефалін і брадикінін).
Ферментативний синтез генів має велике значення, тому що принципово можливо проводити штучний синтез будь-яких індивідуальних генів шляхом транскрибування їх із відповідних матричних РНК. Основною перешкодою є синтез не структурних, а регуляторних частин генів, необхідних для їх нормальної роботи. Це здебільшого обмежує використання штучно синтезованих генів.
Клонування генів - це процес, що включає виділення й ампліфікацію (дублювання великої кількості) окремих генів у реципієнтних про- й еукаріотичних клітинах. Ці клітини, які містять потрібний нам ген, можна використовувати для одержання: а) великої кількості білка, що кодується даним геном, або б) великої кількості самого гена у високоочищеному вигляді.
Рекомбінантна ДНК-технологія має як наукове значення (дозволяє виділити окремий ген складного організму і вивчити його функцію на молекулярному рівні), так і практичне застосування. За допомогою рекомбінантної ДНК-технології можна виробляти різні білки для медичної практики. Такі ліки більш безпечні, ніж аналогічні білки, отримані безпосередньо з організмів. Першим таким рекомбінантним препаратом став інсулін.
Інший важливий напрямок біотехнології - виробництво вакцин. Такі вакцини не можуть викликати хвороб, тому що виготовляються з одного із поверхневих білків. Ген такого білка використовується для біореконструкції бактерії. Так створена вакцина проти гепатиту В. Успішно ведеться робота над вакцинами для гепатитів А, С, хламідіозів, герпесу й інших захворювань.
Ведуться роботи зі створення біоінженерних рослин, що могли б мати наступні властивості: 1) високу пристосованість до умов зовнішнього середовища; 2) містити більшу кількість необхідних для людини поживних речовин; 3) тривалий час зберігатися без псування.
Розробляються трансгенні рослини, здатні продукувати в інтересах людини хімічні речовини й ліки. Реконструйовано картоплю для продукції альбуміну людини. Передбачається, що в майбутньому рослини зможуть утворювати у своїх насінинах такі білки, як гормони людини.
Швидкими темпами розвивається біоінженерія тварин. Яйцеклітину поміщають у спеціальну мішалку разом з чужорідною ДНК і дрібними силікон-карбідними голками. Голки роблять множинні отвори в оболонці, крізь які ДНК попадає в клітину. За допомогою цієї технології бичачий гормон росту був введений у яйцеклітини багатьох видів тварин. Завдяки цій технології отримані великі риби, корови, свині, кролики, вівці. Трансгенні тварини створені для виробництва продуктів медичного значення.
Геном миші. Розшифровка геному людини в лютому 2001 року не дала відповіді на всі питання антропогенетики. Незважаючи на секвенування геному і визначення приблизної кількості генів, що кодують білки, функція більшості з них залишається невідомою. На даний час не ідентифіковано всі гени, що відповідають за розвиток спадкових хвороб і хвороб зі спадковою схильністю.
Розшифровка геному миші, яку використовували в лабораторних дослідженнях з 1900 р., у грудні 2002 року дала нові можливості для вивчення геному людини.
Кількість генів миші складає 27000-30500, що приблизно відповідає кількості генів людини. Близько 99 % цих генів мають нуклеотидну послідовність, властиву людському геному і 96 % із них знаходяться в "синтенних" ділянках хромосом миші і людини.
На даний час можливе виведення трансгенних мишей з точним "вимиканням" (делецією) генів, проводити аналіз змін фенотипу, що виникають внаслідок цього, і згодом шукати подібні нуклеотидні послідовності в геномі людини. Це прискорить ідентифікацію генів, що відповідають за розвиток певних нормальних і патологічних ознак у людини.
Аналіз нуклеотидної послідовності миші дозволить точно "націлювати" гени людини у схожі нуклеотидні послідовності миші і створювати "людські" ознаки у лабораторних трансгенних мишах. Наприклад, включені в геном миші людські гени білків цитохромів, що беруть участь у метаболізмі ліків, дозволять точно моделювати дію ліків.
Сучасний стан дослідження генома людини.
Міжнародна програма "Геном людини" була сформульована на початку 90-х років XX ст. Внаслідок копіткої роботи до початку 2003 р. геном людини повністю секвенований, тобто повністю прочитана послідовність трьох мільярдів пар основ, з яких побудована ДНК всіх 23 пар хромосом людини. Генетична довжина геному людини складає 3000 сМ (сантиморганіда, генетична відстань, яка дорівнює 1 % кросинговеру). Розв'язання програми "Геном людини" сприяло створенню генетичної карти, відтворенню цитогенетичної карти геному .
Генетична карта передбачає встановлення послідовності розміщення генетичних маркерів з відстанню не більше 1 см вздовж усіх хромосом. Така генетична карта дозволяє картувати будь-який ген, встановити відносну відстань між локусами.
Винятковим успіхом програми "Геном людини" було створення інтегральних (фізичних) карт геному.
Картовано близько 40000 кодуючих послідовностей. Загальне число генів, очевидно, складатиме 30500-40000.
На сьогодні весь геном людини клонований у вигляді великих фрагментів, які перекривають один одного. Розташування кожного з цих фрагментів на хромосомі визначено з високою точністю.
Термін клонування означає, що ген картований, виділений, вивчена його структура, знайдена мутація, яка викликає те чи інше захворювання.
Розкриття геному людини сприятиме розвитку нових напрямків медицини, вивченню природи спадкових і злоякісних хвороб, розробці генної і клітинної терапії.
Поняття про генну терапію .
Генна терапія - заміна дефектних генів нормальними. Вона включає також використання генів для лікування цукрового діабету і СНІДу. Питання про можливість лікування спадкових захворювань виникло відразу ж, як тільки вчені розробили шляхи
перенесення генів у визначені клітини, де вони транскрибуються і транслюються. Виникло також питання: яких хворих у першу чергу лікувати - яких більше чи хвороби яких більш вивчені? Більшість схилялися до того, що генна терапія повинна бути створена для тих хвороб, про які більше відомо: відомий уражений ген, білок, тканини їх локалізації. Так, зокрема, сталося з тяжким імунодефіцитом, що пов'язаний з відсутністю в організмі ферменту аденозиндезамінази (АДА). Внаслідок дефіциту АДА порушується формування в дитини Т- і В-лімфоцитів і вона стає зовсім беззахисною перед бактеріями і вірусами. На фоні великих фінансових витрат отримано терапевтичний ефект у хворих дітей внаслідок введення їм гена АДА. Однак таких дітей щорічно народжується кілька десятків. На даний час велика увага надається дослідженням з генотерапії хвороб, що уражають багатьох людей: гіпертонія, високий рівень холестерину, діабет, деякі форми раку та ін.
Зважаючи на те, що генотерапія пов'язана зі зміною спадкового апарату людини, потрібні особливі вимоги при клінічному дослідженні: 1) чітке знання дефекту гена і яким чином формуються симптоми хвороби; 2) відтворення генетичної моделі у тварин; 3) відсутність альтернативної терапії, або існуюча терапія неможлива або неефективна; 4) безпека для хворого.
При розробці генотерапії також вирішуються такі питання: 1) які клітини необхідно використовувати?
яку частину клітин необхідно вилікувати, щоб зменшити або зупинити прогресування хвороби?
чи буде небезпечна зверхекспресія введеного гена?
чи є безпечним потрапляння реконструйованого гена в інші тканини?
як довго буде функціонувати змінена клітина?
6) чи будуть атаковані нові клітини імунною системою?
Спадкова генотерапія є трансгенною і змінює всі клітини організму. У людини вона не використовується. Неспадкова (соматична) генна терапія корегує тільки соматичні клітини, уражені внаслідок генетичного дефекту. Неспадкова генотерапія може допомогти індивідууму, але вона не покращить стан майбутніх поколінь, тому що мутантний ген не змінений у гаметах.
На жаль, про більшість спадкових хвороб поки мало що відомо. У тих випадках, коли відомо, які тканини уражені, введення нормального гена в них ускладнено. Незважаючи на це, медична генетика досягла значних успіхів у лікуванні окремих захворювань. При цьому використовуються два підходи. Перший із них передбачає виділення клітин із тіла пацієнта для введення в них необхідного гена (генна терапія ех vivo ), після чого вони повертаються в організм хворого. Як вектор використовують ретровіруси, що містять генетичну інформацію у вигляді РНК. Ретровірус забезпечується рекомбінантною РНК (РНК вірусу + РНК копія гена людини). Після надходження рекомбінантної РНК у клітину людини, наприклад, у стовбурову клітину червоного кісткового мозку, відбувається зворотна транскрипція і рекомбінантна ДНК, що несе нормальний ген, попадає в хромосому людини.
Так було проведено лікування зазначеного вище тяжкого імунодефіциту, внаслідок відсутності АДА, у декількох дітей. Паралельно вони отримали виділений у корів фермент АДА як лікувальний препарат.
Використовуючи як вектор аденовірус (АVV), вчені розробили метод генної терапії серпоподібно-клітинної анемії. За природних умов АVV уражає тільки ті клітини червоного кісткового мозку, які є попередниками еритроцитів. Функціональний ген ( β-глобіну ввели в АVV, а вірус переніс його в незрілі еритроцити. Останні наповнюються нормальним гемоглобіном і спрямовуються у кровотік.
Інший підхід у гемотерапії передбачає використання вірусів, вирощених у лабораторії клітин і навіть штучних носіїв для введення генів безпосередньо в організм хворого. Наприклад, позбавлений хвороботворних властивостей аденовірус міститься у флаконі з аерозолем. При вдиханні хворим аерозольної суспензії вірус проникає в клітини легень і приносить до них функціональний ген муковісцидозу.
Якщо клітини стійкі до генетичних маніпуляцій, вчені впливають на клітини, що знаходяться поруч. Останні мають вплив на дефектні за визначеним геном клітини. Так, апробується генна терапія мишей, в яких ушкоджена та ж ділянка мозку, що й у хворих з хворобою Альцгеймера. У фібробласти проникає ген фактора росту нервів. Ці клітини імплантуються у розріз мозку і секретують фактор росту, що необхідний нейронам. Нейрони починають рости і продукувати відповідні нейромедіатори. Передбачається, що схожий тип генної терапії може бути використаний для лікування хвороби Гентінгтона, хвороби Паркінсона, депресії та ін.
Певні успіхи досягнуті при використанні генної терапії в лікуванні злоякісних новоутворень. Виділяється пухлинна клітина, в яку вводяться гени, що кодують такі протиракові речовини імунної системи, як інтерферони, інтерлейкіни. Введені заново у пухлину, клітини починають продукувати ці речовини, вбивають і себе і навколишні злоякісні клітини.
Додаток № 2
Генетичні карти. Методи картування хромосом людини.
Г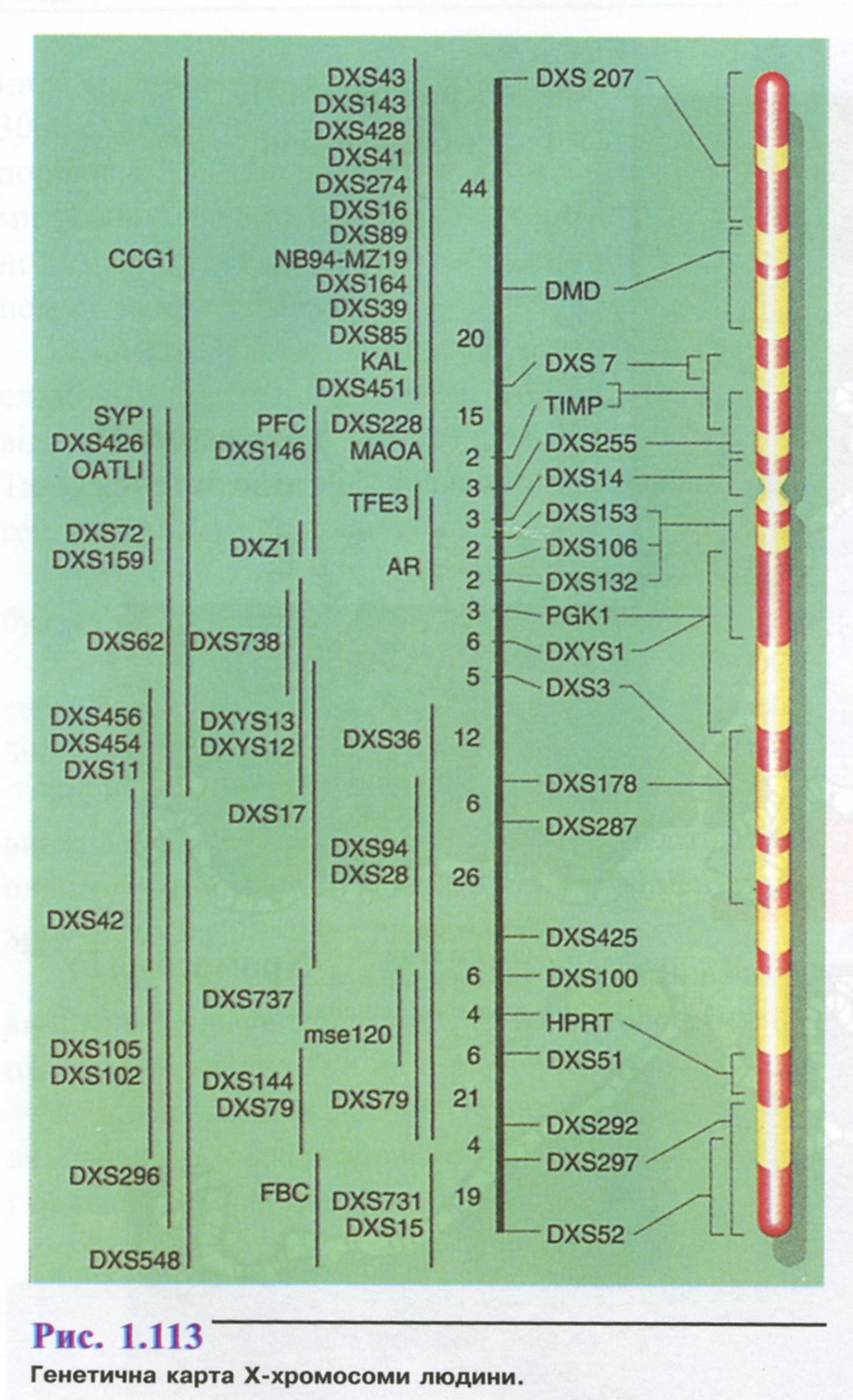 енетична
карта
- це відрізок прямої, на якій позначено
порядок розташування генів і вказано
відстань між ними у відсотках кросинговеру.
Вона будується на основі результатів
аналізуючого схрещування.
енетична
карта
- це відрізок прямої, на якій позначено
порядок розташування генів і вказано
відстань між ними у відсотках кросинговеру.
Вона будується на основі результатів
аналізуючого схрещування.
Картування проводиться, щоб дізнатися, в якій парі хромосом і на якій генетичній відстані (коефіцієнт рекомбінації), або в якій частині хромосоми розташовані гени.
Побудовано генетичні карти для багатьох об'єктів. Серед покритонасінних рослин краще за все вивчено генетичні карти кукурудзи, ячменю, рису, томатів та ін. У тварин такі карти складено для дрозофіли, а серед ссавців - для миші. Доведено, що такий розподіл генів у хромосомах є загальнобіологічною закономірністю.
У людини аналіз зчеплення генів класичними методами, розробленими на дрозофілі, неможливий внаслідок неможливості експериментальних шлюбів. В останні роки розроблено комплекс методів картування генів на хромосомах людини. Так, для вивчення груп зчеплення і складання карт хромосом використовують понад 15 методів.
Картування хромосом у людини проводиться шляхом аналізу родоводів та генетичного аналізу гібридних соматичних клітин.
Тривалий час були відомі тільки три аутосомні групи зчеплення і Х-хромосомна. Новий період розпочався з 1968р.коли вдалося встановити локалізацію гена групи крові Даффі у хромосомі 1. У людини відомі всі 24 групи зчеплення.
З загальної кількості генів геному людини 16000 тепер картовані на скелетній карті геномад, складеній за допомогою 1000 високополімерних ДНК-маркерів.
Виявлення груп зчеплення у хромосомах дає можливість побудови хромосомних карт, коли на хромосомі розміщення генів позначають у вигляді цяточок. Найбільш повно побудована карта Х-хромосоми. Локуси, зчеплені з Х-хромосомою (а їх понад 200), віднесені до цієї хромосоми спираючись на аналіз родоводів (багато з них підтверджені методами гібридизації соматичних клітин).
Методи побудови карт хромосом ґрунтуються на передбаченні ймовірності кросинговеру по всій довжині хромосоми і випадкових обмінах між різними хроматидами.
Для картування хромосом застосовують гібридизацію соматичних клітин людини з клітинами різних тварин, переважно з клітинами миші. При культивуванні таких гібридних клітин на живильному середовищі відбувається постійна втрата хромосом людини. Коли в гібридній клітині залишається тільки одна хромосома від каріотипу людини, її можна ідентифікувати шляхом диференціального забарвлення. Визначивши потім вміст певного ферменту в даній клітині, можна стверджувати, що локус гена до цього ферменту розташований в цій хромосомі.
Незважаючи на певні труднощі при побудові генетичних карт і на їх відносність, детальна розробка карт - один з провідних методів аналізу поведінки і тонкої будови хромосом.
На рис. 1.113 зображено генетичну карту X-хромосоми. Символами позначено картовані гени з указанням ділянок їх локалізації.
Складання точних карт хромосом є необхідною передумовою подальшого прогресу теоретичної генетики людини. Це має виняткове значення для виявлення та диференціальної діагностики спадкових хвороб плода, для ранньої діагностики цих хвороб, встановлення носіїв генетичних зрушень, які перебувають у безсимптомній фазі, для визначення медико-генетичного прогнозу.
Задачі на визначення порядку розміщення генів на хромосомі:
Задача №1. гени А,В,С містяться в одній групі зчеплення. Кросинговер між генами А і В відбувається з частотою 22% , між В і С 6%, між С і А 16%. Визначте порядок розміщення генів уздовж хромосоми.
Розв’язування : _____________________________________


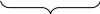 А
С В
А
С В
16% 6%
22%
Відповідь: гени розміщені на хромосомі в послідовності : АСВ
Розв’яжіть задачу : Задача № 2 .Гени А,В, та С належать до однієї групи зчеплення. Експериментально виявлено , що відстань між генами С і В становить 20 морганід, між С і А – 25, між А і В 5 морганід. Визначте порядок розміщення генів уздовж хромосоми.
Додаток № 3
Генетична небезпека забруднення середовища .
Генетична небезпека забруднення середовища. Моніторинг генетичний - заходи, спрямовані на відслідковування виникнення і поширення спадкової патології. Це комплексне обстеження певних груп населення, спрямоване на реєстрацію подій генетичного характеру, виявлення нових мутацій (анеуплоїдії і тяжких форм домінантних мутацій), успадкованих від попередніх поколінь (генних і хромосомних захворювань), виявлення тимчасових тенденцій або відмінностей у просторовому розподілі хвороб із спадковою схильністю, пошук можливих причин зв'язку між збільшенням частот цих подій з факторами довкілля.
Можна проводити моніторинг великих популяцій для пошуку нових мутацій. У процесі такого обстеження застосовують скринінг на домінантні мутації, які дають специфічні фенотипи. Виконують скринінг на геномні і хромосомні мутації. Для цього необхідно здійснювати скринінг популяцій цілих країн. Проведення таких заходів забезпечує отримання інформації про мутаційні частоти та їх зміну в залежності від умов середовища та генетичної компоненти.
Мутаційний процес - явище, властиве всій живій природі. Людина не є винятком. Цей процес проходить постійно й інтенсивно на генному, хромосомному і геномному рівнях. Близько 20 % всіх спадкових хвороб у кожному з поколінь після народження - хвороби, зумовлені новими мутаціями (М. П. Бочков, 2001), тобто внесок мутацій у спадкову патологію вагомий. Відомо, що індукований мутагенез, зокрема вплив радіації і хімічних мутагенів завдає тільки шкоди, викликають спадкові дефекти.
До заходів, спрямованих на запобігання розвитку індукованих мутацій, належить тестування на мутагенність фармацевтичних препаратів, які вже використовуються або плануються до впровадження в клініку. Існують мікробні тест-системи з використанням мікросом печінки ссавців.
Дослідженню на мутагенність підлягають пестициди, які застосовуються або плануються до впровадження в сільське господарство.
Відомо понад 500 сполук, які мають антимутагенні властивості. До них належать вітаміни С, Е, А, інтерферон, бемитил, томерзол та ін. Механізми дії цих речовин досить складні і передбачають залучення їх у ферментативнозалежний антирадикальний ланцюг і здатність до зв'язування супероксидного аніон-радикалу кисню. Вітамінопрофілактика мутагенезу передбачає призначення вітамінних комплексів різного кількісного й якісного складу, що призводить до зниження числа пошкоджених мутагеном клітин, зменшує чутливість лімфоцитів до мутагену.
Встановлено, що рівень окислювальних пошкоджень ДНК зменшується при споживанні низькокалорійної дієти, багатої на каротиноїди.
За умов наявності мутацій (фенілкетонурія, галактоземія та ін.) з метою зменшення негативного впливу на плід призначають внутрішньоутробне лікування. Так, вагітним з ризиком народження дитини з уродженою гіперплазією кори наднирників до 10-20 тижня вагітності призначають дексаметазон (20 мкг/кг) незалежно від стану плоду. При загрозі розвитку ацидурії вагітним призначають вітамін В. З виникненням аритмії у плоду вагітні отримують кардіологічні препарати. Якщо провести лікування жінок протягом 3-6 міс до запліднення та впродовж перших місяців вагітності вітамінами (С, Е, фолієва кислота), то імовірність розвитку в дитини аномалій нервової трубки істотно зменшується (М. П. Бочков, 2001).
Поняття про антимутаген та комутаген.
Комутагени. Комутагени - це речовини, які підвищують ефекти середовищних мутагенів, хоча самі по собі не здатні до мутагенної дії, не мають власної мутагенної активності. Такий ефект мають сполуки природного і штучного походження, неорганічної і органічної природи. Комутагенез - зростання пошкоджувального ефекту мутагенів під дією не мутагенних сполук. Так, аскорбінова кислота (вітамін С) підсилює цитогенетичні ефекти мутагенів, зокрема циклофосаміду, в культурі лімфоцитів людини: збільшує пошкодження ДНК і т. п.
Іншим комутагеном вважається кофеїн, який впливає на спонтанний та індукований мутагенез. Кофеїн збільшує індукцію метотрексатом сестринських хроматидних обмінів, утворення мікроядер тощо.
Комутагенну дію мають деякі фармакологічні засоби. Так, верапаміл та фендилін підсилюють бластогенну дію блеоміцину, пепломіцину. Таким же ефектом володіють нестероїдні протизапальні препарати (лорноксикам, теноксикам та ін).
Присутність у середовищі комутагенів може підвищувати негативні ефекти фізичних, хімічних, біологічних, лікарських та інших мутагенів, з якими контактує людина.
Антимутагени. Відомо понад 500 сполук, в яких доведено антимутагенний вплив, - здатність їх до захисту геному від дії мутагенів. Речовини з таким спрямуванням підвищують стійкість клітин до негативного впливу мутагенів, знижують кількість пошкоджених мутагеном клітин. Так, прийом (3-каротину (25 мг), вітаміну С (100 мг) і вітаміну Е (280 мг) зменшує спонтанне пошкодження ДНК у лімфоцитах периферичної крові. Поліфенольні антиоксиданти, які містяться у зеленому чаї, значно зменшують частоту сестринських хроматидних обмінів у лімфоцитах периферичної крові людей, що курять. Прийом аскорбінової кислоти з розрахунку 1 таб/добу значно зменшує рівень хромосомних аберацій в лімфоцитах периферичної крові у робітників, які контактують з кам'яновугільними смолами та вугільним пилом. Встановлено, що прийом вітамінів А (33000 МО/добу) і С (500 мг/добу) впродовж 1 міс знижують аномально високий рівень спонтанного мутагенезу в робітників, які працюють в умовах виробництва молібдену.
Доведено, що захисний антимутагенний ефект тих чи інших речовин залежить від часу їх введення відносно мутагену, від стадії клітинного циклу. Цей ефект специфічний для різних хвороб людини і тому не має універсального характеру.
Застосування антимутагенів спрямоване на максимальну стійкість клітин людини та захист геному людини від мутагенних впливів.
Таблиця на зразок :
Таблиця №1. Сполуки , антимутагеної та мутагеної дії
Р е ч о в и н и , я к і є : |
|
А н т и м у т а г е н а м и |
К о м у т а г е н а м и |
|
|
|
|
Додаток № 4
БИОТЕХНОЛОГИЯ
( статья из БОЛЬШОЙ ЭНЦИКЛОПЕДИИ КИРИЛЛА И МЕФОДИЯ – 2003Г.)
БИОТЕХНОЛОГИЯ (от греч. bios — жизнь, techne — искусство, мастерство и logos — слово, учение), использование живых организмов и биологических процессов в производстве. Биотехнология — междисциплинарная область, возникшая на стыке биологических, химических и технических наук. С развитием биотехнологии связывают решение глобальных проблем человечества — ликвидацию нехватки продовольствия, энергии, минеральных ресурсов, улучшение состояния здравоохранения и качества окружающей среды.
История биотехнологии
С древнейших времен человек использовал биотехнологические процессы при хлебопечении, приготовлении кисломолочных продуктов, в виноделии и т. п., но лишь благодаря работам Л. Пастера в середине 19 в., доказавшего связь процессов брожения с деятельностью микроорганизмов, традиционная биотехнология получила научную основу. В 40-50-е годы 20 в., когда был осуществлен биосинтез пенициллинов методами ферментации, началась эра антибиотиков, давшая толчок развитию микробиологического синтеза и созданию микробиологической промышленности. В 60-70-е гг. 20 в. начала бурно развиваться клеточная инженерия. С созданием в 1972 группой П. Берга в США первой гибридной молекулы ДНК in vitro формально связано рождение генетической инженерии, открывшей путь к сознательному изменению генетической структуры организмов таким образом, чтобы эти организмы могли производить необходимые человеку продукты и осуществлять необходимые процессы. Эти два направления определили облик новой биотехнологии, имеющей мало общего с той примитивной биотехнологией, которую человек использовал в течение тысячелетий. Показательно, что в 70-е гг. получил распространение и сам термин «биотехнология». С этого времени биотехнология неразрывно связана с молекулярной и клеточной биологией, молекулярной генетикой, биохимией и биоорганической химией. За краткий период своего развития (25-30 лет) современная биотехнология не только добилась существенных успехов, но и продемонстрировала неограниченные возможности использования организмов и биологических процессов в различных отраслях производства и народного хозяйства.
Биотехнология в медицине
В медицине биотехнологические приемы и методы играют ведущую роль при создании новых биологически активных веществ и лекарственных препаратов, предназначенных для ранней диагностики и лечения различных заболеваний. Антибиотики — самый большой класс фармацевтических соединений, получение которых осуществляется с помощью микробиологического синтеза. Созданы генно-инженерные штаммы кишечной палочки, дрожжей, культивируемых клеток млекопитающих и насекомых, используемые для получения ростового гормона, инсулина и интерферона человека, различных ферментов и противовирусных вакцин. Изменяя нуклеотидную последовательность в генах, кодирующих соответствующие белки, оптимизируют структуру ферментов, гормонов и антигенов (так наз. белковая инженерия). Важнейшим открытием явилась разработанная в 1975 Г. Келером и С. Мильштейном техника использования гибридом для получения моноклональных антител желаемой специфичности. Моноклональные антитела используют как уникальные реагенты, для диагностики и лечения различных заболеваний.
Биотехнология в сельском хозяйстве
Вклад биотехнологии в сельскохозяйственное производство заключается в облегчении традиционных методов селекции растений и животных и разработке новых технологий, позволяющих повысить эффективность сельского хозяйства. Во многих странах методами генетической и клеточной инженерии созданы высокопродуктивные и устойчивые к вредителям, болезням, гербицидам сорта сельскохозяйственных растений. Разработана техника оздоровления растений от накопленных инфекций, что особенно важно для вегетативно размножаемых культур (картофель и др.). Как одна из важнейших проблем биотехнологии во всем мире широко исследуется возможность управления процессом азотфиксации, в том числе возможность введения генов азотфиксации в геном полезных растений, а также процессом фотосинтеза. Ведутся исследования по улучшению аминокислотного состава растительных белков. Разрабатываются новые регуляторы роста растений, микробиологические средства защиты растений от болезней и вредителей, бактериальные удобрения. Генно-инженерные вакцины, сыворотки, моноклинальные антитела используют для профилактики, диагностики и терапии основных болезней сельскохозяйственных животных, В создании более эффективных технологий племенного дела применяют генно-инженерный гормон роста, а также технику трансплантации и микроманипуляций на эмбрионах домашних животных. Для повышения продуктивности животных используют кормовой белок, полученный микробиологическим синтезом.
Биотехнология в производстве
Биотехнологические процессы с использованием микроорганизмов и ферментов уже на современном техническом уровне широко применяют в пищевой промышленности. Промышленное выращивание микроорганизмов, растительных и животных клеток используют для получения многих ценных соединений — ферментов, гормонов, аминокислот, витаминов, антибиотиков, метанола, органических кислот (уксусной, лимонной, молочной) и т. д. С помощью микроорганизмов проводят биотрансформацию одних органических соединений в другие (например, сорбита во фруктозу). Широкое применение в различных производствах получили иммобилизованные ферменты. Для выделения биологически активных веществ из сложных смесей используют моноклональные антитела. А. С. Спириным в 1985-88 разработаны принципы бесклеточного синтеза белка, когда вместо клеток применяются специальные биореакторы, содержащие необходимый набор очищенных клеточных компонентов. Этот метод позволяет получать разные типы белков и может быть эффективным в производстве. Многие промышленные технологии заменяются технологиями, использующими ферменты и микроорганизмы. Таковы биотехнологические методы переработки сельскохозяйственных, промышленных и бытовых отходов, очистки и использования сточных вод для получения биогаза и удобрений. В ряде стран с помощью микроорганизмов получают этиловый спирт, который используют как горючее для автомобилей (в Бразилии, где топливный спирт широко применяется, его получают из сахарного тростника и других растений). На способности различных бактерий переводить металлы в растворимые соединения или накапливать их в себе основано извлечение многих металлов из бедных руд или сточных вод.
***
Дальнейший прогресс человечества во многом связан с развитием биотехнологии. Вместе с тем необходимо учитывать, что неконтролируемое распространение генно-инженерных живых организмов и продуктов может нарушить биологический баланс в природе и представлять угрозу здоровью человека.
В.А Аветисов.
Методична розробка для організації самостійної роботи студентів № 7
години
Дисципліна : Медична біологія
Тема: Методи генетики людини : дерматогліфічний, імунологічний,
гібридизація соматичний клітин.
Викладач: Рибальченко Віталій Валентинович
Курс, група: І курс, групи 11, 12, 13 спеціальність: 5.110.102 «сестринська справа»
1. Актуальність теми: всі експерименти над людиною заборонені, тому вчені шукають методи, які можуть відповісти на питання пов’язані з генетикою людини (медична генетика). До методів медичної генетики відносять такі , як : дерматогліфіка – вивчення рельєфу шкіри на пальцях рук, долонях та підошвах. Цей метод використовують в комплексі з імунологічним та методом гібридизації соматичних клітин для діагностики спадкових хвороб, та для індифікування особи в судовій медицині.
