
- •Тема 2.
- •Биохимические реакции цтк( для ознакомления записи биохимических реакций)
- •Энергетический баланс одного оборота цтк
- •Березов т.Т., Коровкин б.Ф. Биологическая химия: Учебник.-3-е изд.-м.: Медицина. 2004.- 704 с. С. 298 – 318.
- •Биохимия. Учебник/ Под ред. Е.С.Северина.-м.: гэотар-мед, 2004.-
- •Лекции по курсу биохимии. Тема: Энергетический обмен. Биологическое
Биохимические реакции цтк( для ознакомления записи биохимических реакций)
1). Цитратсинтаза локализуется в матриксе митохондрий, ее активируют ЩУК, НАД+; ингибируют АТФ, НАДН2, Сукцинил-КоА, цитрат.

2). Аконитаза локализуется в матриксе митохондрий.

3). Окислительно-восстановительная реакция, самая медленная в ЦТК.
Изоцитратдегидрогеназа локализуется в матриксе митохондрий, ее активируют АМФ, Са2+, АДФ, НАД+; ингибируют АТФ, НАДН2.
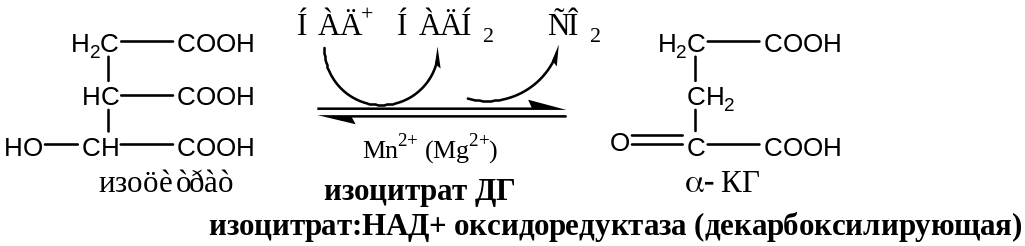
4). Окислительно-восстановительная реакция.
α-кетоглутаратдегидрогеназный комплекс состоит из 3 ферментов и содержит 5 коферментов: тиаминдифосфат, кофермент А, липоевая кислота, НАД+, ФАД.
α-КГ ДГ активируется Са2+, ингибируется сукцинил-КоА, АТФ, НАДН2.

5). Реакция субстратного фосфорилирования

6). Окислительно-восстановительная реакция.
Сукцинатдегидрогеназа, флавопротеин содержащий Fe2S2, связана с внутренней мембраной митохондрии. СДГ ингибирует ЩУК и Сукцинил-КоА,

7). Фумараза локализуется в матриксе митохондрий.

8). Окислительно-восстановительная реакция.
Малат ДГ локализуется в матриксе митохондрий.

Образовавшиеся молекулы ЩУК реагируют с новой молекулой Ацетил-КоА и цикл повторяется вновь.
Энергетический баланс одного оборота цтк
В 4 окислительно-восстановительных реакциях ЦТК образуются 3 НАДН2 и 1 ФАДН2, которые направляются далее в дыхательную цепь окислительного фосфорилирования. В процессе окислительного фосфорилирования ДЦ из 1 НАДН2 образуется 3 АТФ, из 1 ФАДН2 - 2 АТФ. Из 1 ГТФ, образующейся в ЦТК за счет субстратного фосфорилирования, синтезируется 1 АТФ. Таким образом, за 1 цикл ЦТК из 3 НАДН2, 1 ФАДН2 и 1 ГТФ получается 12 АТФ.
Электронтранспортная цепь митохондрий ( дыхательная цепь)
Первичные акцепторы водорода НАД+ и ФАД образуют в процессе реакций цикла Кребса восстановленные формы НАДН и ФАДН2 , которые далее окисляются на внутренней мембране митохондрии, передавая, в конечном счете, электроны кислороду.
Передачу электронов осуществляет электронтранспортная цепь (дыхательная цепь). Движущей силой процесса является возникновение разности потенциалов между восстановителем и окислителем.
В соответствие с изменением редокс – потенциала переносчики электронов
располагаются в последовательности
( комплекс 1 ) ( комплекс 3 ) ( комплекс 4)
субстратН2 –НАД+--ФМН—FeS --Q----цит в---цит с1-- FeS --цит с---цит а/а3---1/2О2
-0, 32 v | + 0,8v
изоцитрат ФАД ( комплекс 2) сукцинат ДГ
кетоглутарат |
малат субстратН2
сукцинат
В цепи возникает разность потенциалов Е=(+0.80 – (-0.32)) = 1, 12 в, ей соответствует изменение свободной энергии 52 ккал/моль ( 220 кДж / моль).
Примерно 40 -45 % этой энергии, около 24 ккал/моль, расходуется на синтез АТФ.
Учитывая, что энергия макроэргической связи АТФ равна 7,3 ккал/ моль, количество используемой энергии позволяет синтезировать максимально 3 моль АТФ при переносе двух электронов по дыхательной цепи.( реально считают 2,5 АТФ )
Обсудим электронтранспортную цепь митохондрий.
Ферменты тканевого дыхания располагаются на внутренней мембране митохондрии.
Все компоненты электронтранспортой цепи ( за исключением коэнзима Q) - белки , которые содержат коферменты, способные участвовать в окислительно-восстановительных реакциях: ФМН, железосульфидные белки, гем, содержащий ионы железа ( цитохромы в, с1 , с, а , а3 ) и меди ( цит.а3 ).
НАДН свободно перемещается в матриксе митохондрии, передает электроны
комплексу переносчиков 1, который прочно связан с мембраной и включает в себя ФМН, железосульфидный белок и коэнзим Q. Коэнзим Q принимает электроны не только от НАД - зависимых дегидрогеназ, но и от ФАД- содержащих ДГ, в частности, сукцинат ДГ
Комплекс 111, включающий в себя цит. а/а3, передает электроны кислороду, происходит восстановление кислорода.
Перенос электронов по дыхательной цепи сопровождается синтезом АТФ из
АДФ и Ф.
Этот путь синтеза АТФ называется окислительным фосфорилированием.
Если перенос электронов сопровождается синтезом АТФ, то имеет место сопряжение дыхания и фосфорилирования.
Выделяют три участка дыхательной цепи (три точки фосфорилирования), на которых происходит процесс окислительного фосфорилирования.
Разность потенциалов на участке- как рассчитали - должна быть не менее 0.17 в.
1 точка – между ФМН и коэнзимом Q
2 точка – между Цит. в и Цит. с
3 точка - при переносе электронов от Цит а/а3 на кислород.
Перенос электронов от НАДН сопровождается синтезом 3 АТФ.
Коэффициент сопряжения Р : О = 3 : 1
Перенос электронов от ФАДН2 сопровождается синтезом 2 АТФ.
Коэффициент Р : О = 2 : 1.
Если перенос электронов по дыхательной цепи и восстановление кислорода не сопровождается синтезом АТФ, то возникает разобщение дыхания и фосфорилирования.
Рис. Мембрана митохондрии и расположение переносчиков электронов
Механизмы сопряжения и разобщения можно объяснить на основании
хемиосмотической теории П.Митчелла (1961 г.) :
перенос электронов по дыхательной цепи сопровождается «выкачиванием»
протонов из матрикса в межмембранное пространство
внутренняя мембрана непроницаема для протонов, протоны не могут вернуться в
матрикс, создается разность величин рН и разность зарядов.
эта разность создает электрохимический потенциал – источник энергии для синтеза АТФ.
энергия электрохимического потенциала используется для синтеза АТФ только
в том случае, если протоны возвращаются в матрикс через ионные каналы АТФ- -азы (АТФ-синтетазы).
Электрохимический потенциал активирует АТФ-азу, происходят конформаци-
онные изменения составляющих ее субъединиц, осуществляется реакция синтеза
АДФ + Ф = АТФ
Если исчезает электрохимический потенциал, то синтез АТФ прекращается , возникает разобщение. Особые вещества – разобщители - участвуют в этом процессе.
Разобщители действуют по нескольким направлениям:
- связывают протоны, препятствуя их возвращению в матрикс
- переносят протоны в матрикс помимо протонных каналов АТФ-азы
Процесс разобщения дыхания и фосфорилирования сопровождается выделением энергии в виде теплоты. Митохондрии бурого жира всегда находятся в режиме разобщения благодаря присутствию особого белка термогенина.
Термогенез необходим для поддержания температуры тканей тела. В животном мире играет решающую роль в пробуждении от зимней спячки.
Физиологическими разобщителями являются жирные кислоты, гормон тироксин, билирубин, разобщающий эффект присущ лекарственным препаратам с пирогенным эффектом действия.
На отдельных этапах дыхательной цепи возможно блокирование переноса электронов
На участке ФМН – FeS ингибитором являются амитал, препарат группы барбитуратов,
ротенон – высокотоксичное вещество, выделенное из некоторых водорослей.
На участке цит. в – цит. с1 действует ингибитор антимицинА, токсичный антибиотик.
Терминальный участок цитохромоксидазу ингибируют ион цианида, угарный газ СО,
сероводород, образуя устойчивые соединения с ионами железа и меди, и тем самым прекращают перенос электронов на кислород. Этим объясняется их высокая токсичность.
При гипоксии начинает действовать укороченный путь переноса электронов, основным субстратом становится сукцинат, который в настоящее время широко используется как лечебное и профилактическое средство в кардиологии, геронтологии, при анемиях у детей.
В случае блокирования цитохромоксидазы, временный эффект оказывают искусственные акцепторы электронов: метиленовый синий (+0.011 в),
аскорбат (+ 0,058 в).
Скорость окисления НАДН в дыхательной цепочке регулирует скорость реакций цикла Кребса, а соотношение АДФ/АТФ- скорость тканевого дыхание. Изменение скорости тканевого дыхания в зависимости от концентрации АДФ носит название дыхательный контроль. Понятно, что повышение содержания АДФ увеличивает скорость тканевого дыхания, а понижение – соответственно снижает.
В медицинской практике используется кислород в в лечебных целях. Примером может служить гипербарическая оксигенация, которую применяют при нарушении кровообращения.. Но ни в коем случае не значит, что поступление кислорода в ткани увеличивает интенсивность синтеза АТФ. Кислород обеспечивает только беспрепятственную возможность образования АТФ путем окислительного фосфорилирования..
Синтез АТФ происходит внутри МХ, а все энергозависимые и энергопотребляющие процессы происходят в иных структурах клетки.
Между митохондрией и цитозолем происходит обмен АДФ и АТФ. В мембране митохондрии есть особый белок АТФ/АДФ-антипортер, который осуществляет перенос этих нуклеотидов через мембрану МХ.
Молекула АДФ поступает в матрикс МХ только при условии выхода АТФ из матрикса.
Матрикс цитозоль
АТФ-----------------------------АТФ
АДФ ----------------------------АДФ
На транспорт расходуется примерно 25% энергии переноса электронов. Транспорт фосфата, необходимого для синтеза АТФ в матриксе МХ, и кальция, также связаны с системой переноса электронов в дыхательной цепочке.
Образование активных форм кислорода
Активные формы кислорода: суперокид-анион, пероксид водорода, гидроксид – радикал.
Основное место образования
- микросомальная цепь переноса электронов ( цит. р-450),
- частично могут возникать в митохондриальной цепи переноса электронов
- в результате ферментативных реакций с участием ксантиноксидазы, алкогольоксидазы
- неферментативных процессов -аутоокисление адреналина, гемоглобина, глутатиона.
Активные формы кислорода обнаружены во всех биологических жидкостях организма: крови, слюне, слезе.
Одноэлектронный перенос сопровождается образованием супероксида - анион-радикала (содержит одиночный неспаренный электрон и заряд минус)
О2 + е = О2-
На второй стадии восстановления образуется анион пероксида и пероксид водорода
О2- + е = О2 2- О2 2- + 2Н+ = Н2О2
Возможно участие воды, среда в процессе реакции становится щелочной.
О2 2- + 2Н 2О = Н2О2 + 2 ОН-
На третьей стадии возникают радикал и анион гидроксида (среда вновь щелочная)
Н2О2 + е = НО. + НО-
На последней стадии восстановление сопровождается образованием иона оксида О 2-
Свободный ион О 2- реагирует с водой, и вновь образуется ион гидроксида..
О 2- + Н 2О = 2 ОН-
Образование воды возможно только в случае восстановления кислорода в системе переносчиков электронов ( мембраны митохондрий и микросом)
О 2- + 2Н+ = Н 2О
Супероксидный анион является высокотоксичным и относительно стабильным радикалом.
Он взаимодействует с молекулами белка, липопротеинами, вызывает разрыв спирали ДНК, окисление тиольных групп, вызывает перекисное окисление липидов, создает структурные нарушения биологических мембран. В физиологических условиях концентрация супероксида чрезвычайно низкая 8. 10 -12. М. Примерно 80% супероксидного аниона превращается в пероксид водорода с участием фермента супероксиддисмутазы (СОД).
2 О2- + 2 Н + = Н 2 О 2 + О2 или
2 О2- + 2 Н 2О = Н 2 О 2 + О2 + 2 ОН-
Активно этот процесс протекает в макрофагах момент фагоцитоза.
Фермент СОД принято называть представителем ферментативной антиоксидантной защиты( АОЗ) в клетке.
Без участия СОД происходит спонтанная дисмутация супероксидного аниона , в результате которой образуется весьма активный и реакционноспособный синглетный кислород
2 О2- + 2 Н + = Н2О 2 + “O2
СОД встречается у всех аэробных организмов. Относится к металлоферментам. Содержит в активном центре ионы меди, марганца, железа, цинка. У человека, независимо от места локализации, в активном центре медь и цинк. Ионы цинка стабилизируют конформационную структуру, а ионы меди находятся в каталитическлм центре.
Цинк также обнаружен в активных центрах карбоангидразы и алкогольдегидрогеназы и необходим для стабилизации структуры белка- гормона инсулина.
Ген Сu-Zn-СОД у человека находится на 21 хромосоме. Высокий уровень активности отмечен в печени, почках, головном мозге, надпочечниках, щитовидной железе. В форменных элементах активность снижается в последовательности:
тромбоциты - эритроциты - лимфоциты - гранулоциты.
Низкая активность СОД характерна для сердца, костного мозга и селезенки.
Перевод супероксидного аниона в пероксид водорода не устраняет полностью токсичного действия.
Пероксид водорода образуется и в других биохимических реакциях:
- окисление аминов ФАД- зависимой моноаминооксидазой (МАО)
- при метаболизме пуриновых соединений ( гипоксантин - ксантин- мочевая кислота) в тканях и , особенно, в процессе трансформации моноцитов в макрофаги. Физиологическая концентрация пероксида водорода 10-9 - 10-7 М.
Пероксид водорода обладает двойственной реакционной способностью окислителя и восстановителя, но в биологических системах, где много восстановителей, пероксид водорода ведет себя как достаточно сильный окислитель. Окисляет тиольные группы белков, ион железа( Fe 2+ ) в гемоглобине, превращая его в метгемоглобин( Fe 3+ ), усиливает пероксидацию липидов и нарушает проницаемость биомембран ,
Пероксид водорода разрушается каталазой, которая относится к гемсодержащим ферментам.
Каталаза, глутатионпероксидаза и глутатионредуктаза относятся к ферментам антиперекисной защиты( АПЗ).
Каталаза является наиболее распространенным ферментом. Содержится в печени, почках, мышцах, головном мозге, костном мозге, селезенке, легких, сердечной мышце, присутствует в жидких средах организма – крови, слюне, моче, ликворе.
Место локализации каталазы – митохондрии и пероксисомы.
Каталаза может не только разлагать пероксид водорода( каталазная функция), но и окислять эндогенные и экзогенные субстраты с участием пероксида водорода ( пероксидазная активность). Пероксидазное действие наблюдается при высокой концентрации субстратов, например , этанола, который окисляется в ацетальдегид..
Каталаза
С 2 Н 5 ОН + Н 2 О 2 --------------------- СН 3 СНО + 2 Н2 О
Глутатионпероксидаза наряду с каталазой проявляет антиперекисное действие.
В активном центре одной их форм глутатионпероксидазы содержится селен, роль переносчика электронов выполняет трипептид глутатион: γ - глутамат- цистеин -
глицин ( G-SH- восстановленная форма, G-S -S-G- окисленная)
глутатионпероксидаза
Н 2 О 2 + 2 G-SH ---------------------------- G-S -S-G + 2 Н2О
Одновременно( сопряженно) протекает реакция восстановления окисленного глутатиона с помощью НДФН- зависимого фермента глутатионредуктазы. Необходимый для этой реакции НАДФН образуется преимущественно в реакциях пентозофосфатного цикла при действии фермента глюкозо-6-фосфатдегидрогеназы.
глутатионредуктаза
НАДФН + Н+ + G-S -S-G ---------------------------НАДФ + 2 G-SH
Помимо ферментативной АО и АП защиты существуют неферментативные биохимические механизмы, обеспечивающие поддержание гомеостаза при действии активных форм кислорода.
Неферментативная антиоксидантная защита.
К представителям неферментативной антиоксидантной защиты следует отнести эндогенные антиоксиданты, представителями которых являются:
- жирорастворимые витамины Е ( α –токоферол) , А ( ß- каротиноиды )
- водорастворимый витамин С ( аскорбиновая кислота)
- низкомолекулярные метаболиты и природные вещества : аминокислоты ( цистеин,
метионин, аргинин), глутатион, холестерин, мочевая кислота, билирубин и ряд других
веществ
- белки плазмы крови( церулоплазмин)
ВНИМАНИЕ! Раздел «Витамины» может Вам показаться трудным. Но рекомендуем эту всю тему прочитать еще раз после изучения всего курса биохимии.
ВИТАМИН Е
Витамин Е - альфа-токоферол - производное токола. Известно 8 родственных соединений, проявляющих витаминную активность. Это прозрачные маслянистые жидкости, светло-желтого цвета, нерастворимые в воде, хорошо - в эфире слабее - в этаноле. По сравнению с другими витаминами у с т о й ч и в: на воздухе - до 170 0 С, в вакууме - до 220-250 0 С не теряет свои биологические свойства. Наибольшей биологическую активностью обладает α – токоферол .Ультра-
фиолетовые лучи разрушают витамин Е, но в кислой и щелочной средах устойчив. В масляных растворах в отсутствии ультрафиолета долго сохраняет свою активность.

РАСПРОСТРАНЕНИЕ В ПРИРОДЕ
Найден в одноклеточных организмах, дрожжах, водорослях,
практически во всех животных тканях.
С о д е р ж а н и е в п р о д у к т а х, мг%
Масло подсолнечное ....................... 60-75
хлопковое .......................... 70-100
соевое ............................. 75-100
кукурузное ......................... 10-23
оливковое .......................... 3-7
Другие распространенные пищевые продукты содержат (мг/кг сырого веса):
мука ............................... 2,6-3,4
неочищенные яблоки ................. 11
очищенные яблоки ................... 6,7
картофель .......................... 1,0
молоко коровье (весна) ............. 4,0 (мкг/кг липидов)
молоко коровье (осень) ............. 30,0
молоко (женское) ................... 40,0
ВНИМАНИЕ! Токоферолы образуются только в зеленых частях рас-
тений, особенно ими богаты прорастающие семена:
животные ткани не с и н т е з и р у ю т витамин Е.
ПОТРЕБНОСТЬ В ВИТАМИНЕ Е
З а в и с и т о т х а р а к т е р а п и т а н и я и увеличивается:
- при потреблении ненасыщенных жиров, поэтому содержание витамина Е в природных маслах находится в прямой зависимости от степени их насыщенности,
- при недостаточности селена и серусодержащих аминокислот в пище,
- при недостаточности витамина А.
П о т р е б н о с т ь в витамине Е до сих пор точно не установлена из-за трудности определения во всех пищевых продуктах. У взрослых - 10-50 мг/сутки.
Имеются критерии Е-витаминной н е д о с т а т о чн о с т и :
- повышенное выделение креатина с мочой
- пониженное выделение креатинина с мочой
- уменьшение отношения креатин/креатинин
ОБМЕН В ОРГАНИЗМЕ
1. Половина поступающего с пищей витамина Е усваивается в кишечнике в присутствии желчных кислот Все формы витамина E связываются энтероцитами и попадают в кровообращение с хиломикронами.
2.Витамин Е достигает печени, где специфический белок избирательно выделяет α-токоферол из всех поступающих токоферолов и включает его в ЛПОНП., а затем ЛПНП. Другие формы выделяются с желчью и мочой в виде продуктов обмена.. Концентрация α-токоферола в ЛПОНП не может быть увеличена более чем в 2-3 раза т.к. процесс абсорбции контролируется.
3 α.-Токоферол инактивируется в печени
Обнаружен во всех тканях организма
Проявления недостаточности
Хорошо изучены на экспериментальных животных.:
- стерильность - атрофия семенников и рассасывание плода,
- мышечная дистрофия, которая сопровождается снижением содержания гликогена, ионов калия, магния, фосфатов и увеличением содержания липидов,
- некротические изменения в печени (жировая инфильтрация),
- энцефаломаляция.
Выделяют несколько причин развития Е-витаминной недостаточности у человека:
- алиментарная, связанная с дефектами питания
- заболевания желудочно-кишечного тракта, которые приводят к нарушению
всасывания,
- повышенные потребности( беременность, профессиональные вредности- химическая интоксикация, электромагнитное и радиоактивное излучение)
- врожденные нарушения.
Врожденные нарушения обмена токоферола связаны с одновременно с нарушением синтеза ЛПНП
Содержание токоферола в плазме снижается , уменьшается гемолитическая стойкость эритроцитов, нарушается липидный состав их мембран.
Витамин Е в метаболических процессах.
Главное назначение витамина Е - антиоксидант:
- предотвращает окисление полиненасыщенных жирных кислот,
- участвует в обмене селена, который входит в состав глутатионпероксидазы, снижающей содержание перекиси водорода в клетке.
витамин Е регулирует:
- уровень перекисного окисления липидов (ПОЛ),
- состояние мембран,
- функционирование цепи тканевого дыхания и окислительное фосфорилирования,
- регулирует процесс транскрипции генов, синтез тропомиозина. Авитаминоз Е сопровождается мышечной слабостью.
- предохраняет витамин А в тканях от окисления.
Отмечено, что усиленное накопление ретинола снижает содержание витамина Е в тканях и сопровождается усиленным его разрушением; в малых дозах токоферол - синергист витамина А, в больших – антагонист:
- снижает токсическое действие больших доз витамина Д, склонного вызывать усиление ПОЛ, гемолиз эритроцитов,
- считается, что токоферол имеет строение, напоминающее убихинон, является его синергистом и может частично выполнять его функции, защищая от окисления и разрушения.
Обладает антисклеротическим действием:
Необходим для поддержания иммунитета (T- и B-клеточные функции).
Участвует в поддержании сперматогенеза и формировании функционально активных сперматозоидов.
Гиповитаминоз Е. Из-за диетических ограничений он наблюдается только у недоношенных новорожденных в виде гемолитической анемии и ретинопатии.
У взрослых гиповитаминоз Е возникает из-за генетического дефицита аполипопротеина B (apo B) или α-токоферол транспортного протеина (α-TTP).
Может наблюдаться скелетная миопатия и пигментный ретинит, развитие гемолитической анемии, креатинурия, отложения сфинголипидов в мышцах.
ВИТАМИН С (АСКОРБИНОВАЯ КИСЛОТА)
Структура. Аскорбиновая кислота — лактон L –гулоновой кислоты, которая образуется из глюкозы( у тех , кто способны синтезировать витамин С ).Человек и некоторые виды приматов, морские свинки потнряли эту способность.
Существует в двух формах: восстановленной (дигидро, АК) и окисленной (дегидро- ДАК), которые обратимо переходят друг в друга в окислительно-восстановительных реакциях.

Аскорбиновая кислота может окисляться кислородом воздуха, пероксидом и другими окислителями. ДАК легко восстанавливается цистеином, глутатионом, сероводородом.
Физико-химические свойства. Белые кристаллы, растворимые в воде. В слабощелочной среде происходят разрушение лактонового кольца и потеря биологической активности. При кулинарной обработке пищи в присутствии окислителей часть витамина С разрушается.
Источники витамина С — свежие фрукты, овощи, зелень.
Продукт |
Содержание витамина, мг/100г |
Продукт |
Содержание витамина, мг/100г |
Плоды шиповника |
2400 |
Яблоки |
30 |
Облепиха |
450 |
Картофель свежий |
25 |
Смородина чёрная |
300 |
Томаты |
20 |
Лимоны |
40 |
Молоко |
2,0 |
Апельсины |
30 |
Мясо |
0,9 |
Суточная потребность человека в витамине С составляет 50—75мг до 100-150
мг.
Биологические функции. АК вместе с ДАК образует в клетках окислительно-восстановительную пару с редокс-потенциалом +0,139 В.
Благодаря этой способности аскорбиновая кислота участвуетв неферментативных и ферментативных реакциях биологического окисления.
Ферментативные реакции, в основном, реакции гидроксилирования.
гидроксилирование пролина и лизина при синтезе коллагена;
гидроксилирование дофамина в норадреналин;
в синтезе стероидных гормонов в коре надпочечников
Реакции восстановления и антиоксидантная защита
восстановление Fe3+ в Fe2+ в кишечнике, что необходимо для всасывания железа;
освобождение железа из ферритина;
превращении фолата в коферментные формы восстановленной тетрагидрофолиевой кислоты
7.Восстанавливает окисленную форму витамина Е, поддерживая в мембране
концентрацию активной формы восстановленного витамина Е.
8..Инактивирует активные формы кислорода О2• , Н2О2, НО• в водной фазе.
Нарушение обмена. Недостаточность аскорбиновой кислоты приводит к развитию цинги (скорбут). Цингой болеют только человек, приматы и морские свинки.
Главные проявления цинги - нарушение образования коллагена в соединительной ткани, что проявляется разрыхлением дёсен, расшатыванием зубов, нарушением целостности капилляров и подкожными кровоизлияниями. Возникают отёки, боль в суставах, анемия. Одной из причин анемии связана с нарушением обмена железа и фолиевой кислоты.
ВИТАМИН В2 (РИБОФЛАВИН).
Структура. В основе лежит изоаллоксазин, соединённый со спиртом рибитолом.

Физико-химические свойства. Кристаллы желтого цвета, слаборастворимые в воде.
Главные источники витамина В2 — печень, почки, яйца, молоко, дрожжи. Витамин содержится также в шпинате, пшенице, ржи. Частично человек получает витамин В2 как продукт жизнедеятельности кишечной микрофлоры.
Суточная потребность в витамине В2 взрослого человека составляет 1,8—2,6 мг.
Активация. В слизистой оболочке кишечника после всасывания витамина происходит образование коферментов ФМН и ФАД по схеме:

Биологические функции. Коферменты ФАД и ФМН входят в состав аэробных и анаэробных дегидрогеназ, принимающих участие в окислительно-восстановительных реакциях (реакции окислительного фосфорилирования, СДГ, оксидазы АК, ксантионоксидаза, альдегидоксидаза и т.д.).
 Нарушение
обмена. Авитаминоз рибофлавина
выражается в остановке роста у
молодых организмов. Часто развиваются
воспалительные
процессы на слизистой оболочке
ротовой полости (глоссит
- воспаление языка),
появляются длительно незаживающие
трещины в углах рта, дерматит
носогубной складки. Типично воспаление
глаз: конъюнктивиты, васкуляризация
роговицы, катаракта. Развиваются
общая мышечная
слабость и слабость сердечной мышцы.
Нарушение
обмена. Авитаминоз рибофлавина
выражается в остановке роста у
молодых организмов. Часто развиваются
воспалительные
процессы на слизистой оболочке
ротовой полости (глоссит
- воспаление языка),
появляются длительно незаживающие
трещины в углах рта, дерматит
носогубной складки. Типично воспаление
глаз: конъюнктивиты, васкуляризация
роговицы, катаракта. Развиваются
общая мышечная
слабость и слабость сердечной мышцы.
ВИТАМИН РР (НИКОТИНОВАЯ КИСЛОТА, НИКОТИНАМИД)

Физико-химические свойства. Плохо растворим в воде, хорошо - в щелочах.
Источники. Витамина РР много в растительных продуктах, в рисовых и пшеничных отрубях, дрожжах, в печени и почках крупного рогатого скота и свиней. Витамин РР может образовываться из триптофана (из 60 молекул триптофана может образоваться 1 молекула НАД), что снижает потребность в витамине РР при увеличении количества триптофана в пище.
Суточная потребность в этом витамине составляет для взрослых 15-25мг, для детей — 15 мг.
Биологические функции. Никотиновая кислота в организме в составе НАД и НАДФ выполняет функции коферментов более 250 анаэробных дегидрогеназ.( анаэробные- означает, что НАДН и НАДФН кислородом непосредственно не окисляются 1)
Нарушение обмена. Авитаминоз витамина РР приводит к заболеванию «пеллагра» (шершавая кожа). Сокращение РР- предотвращающий пеллагру ( pellagra preventing)
Характерны 3 основных признака: дерматит, диарея и деменция («три Д»).
Пеллагра проявляется в виде симметричного дерматита на участках кожи, доступных действию солнечных лучей, расстройств ЖКТ (диарея) и воспалительных поражений слизистых оболочек рта и языка (стоматиты, гингивиты). Расстройства ЦНС проявляются в более поздние сроки в виде головной боли, головокружений, повышенной раздражимости, в тяжелых случаях в виде деменции (потеря памяти, галлюцинации и бред). Непереносимость солнечных лучей является первым действенным признаком дефицита витамина РР в организме.
Для проверки усвоения темы ответьте на тестовые вопросы
Выберите один правильный или наиболее точный ответ.
1. Принцип жизнедеятельности организма связан с использованием энергии:
а. тепловой г. тепловой и химических связей
б. химических связей д. электромагнитной и химических связей
в. электромагнитной
2. Процессы в организме, направленные на обновление структурных элементов, клеток, тканей, называют:
а. метаболизм г. промежуточный обмен
б . катаболизм д. биологическое окисление
в. анаболизм
3. Процессы организма, направленные на образование простых компонентов из сложных молекул, носят название:
а. метаболизм г. промежуточный обмен
б . катаболизм д. биологическое окисление
в. анаболизм
4. Превращение веществ в организме с момента поступления их в клетки до образования конечных продуктов обмена носит название:
а. метаболизм г. промежуточный обмен
б . катаболизм д. биологическое окисление
в. анаболизм
5. Общий метаболит, который образуется из жиров, белков, углеводов:
а. пируват г. АцКоА и оксалоацетат
б. ацетилКоА д. пируват и АцКоа
в.оксалоацетат
6. Какие вещества в организме человека могут быть субстратами только аэробной фазы биологического окисления:
а углеводы г. углеводы и жирные кислоты
б. жирные кислоты д. аминокислоты и жирные кислоты
в. аминокислоты
7. Запишите последовательность реакций цикла Кребса
Используйте все ключевые слова:
1. малат 2. сукцинат 3. сукцинил КоА 4. фумарат 5. оксалоацетат
а 1 – 2- 3 - 4-5 г. 3 – 2 – 4 – 1- 5
б. 5 - 4 -3 - 2 - 1 д. 3 – 2 – 5 – 1- 4
в. 2 – 3 – 4 -1 -5
8. Конечный продукт метаболизма субстратов цикла Кребса:
а. оксалоацетат г. углекислый газ и вода
б. углекислый газ д. оксалоацетат и углекислый газ
в. вода
9. В реакциях цикла Кребса в составе коферментов присутствуют витамины:
а. В-1, В-2, РР , липоевая кислота г. В-2, В- 6, липоевая кислота
б. В-1, РР, липоевая кислота д. В -6, РР, липоевая кислота
в. В-2, РР, липоевая кислота
10. Локализация ферментов ЦТК
а. матрикс митохондрии г. матрикс и внутренняя мембрана
б. цитоплазма д. матрикс и наружная мембрана
в. наружная мембрана
11. Количество макроэргических связей в молекуле АТФ
а . 1 б. 2 в. 3 г. 4 д. 5
12.Процесс тканевого дыхания включает в себя:
а. выделение СО2 г. потребление О2 и выделение Н2О
б. выделение СО2 и Н2О д. потребление О2 и Н2О
в. потребление О2 и выделение СО2
1 3. Токсичность иона цианида связана с его участием в процессе тканевого дыхания:
а. изменяет редокс потенциал цепи г . необратимо ингибирует цитохромы
б. окисляет НАДН д. окисляется кислородом
в. восстанавливает коэнзим Q
14. Локализация ферментов тканевого дыхании в митохондрии:
а. матрикс
б. внешняя мембрана
в. внутренняя мембрана
г. матрикс и внутренняя мембрана
д. внутренняя и внешняя мембрана
15.Синтез АТФ путем окислительного фосфорилирования происходит в клеточной структуре:
а внутренней мембране митохондрии
б. матриксе митохондрии
в. наружной мембране митохондрии
г. цитоплазм е
д. мембране эндоплазматического ретикулума
16. Максимальное количество моль АТФ, которое синтезируется при переносе одного моль электронов в дыхательной цепи:
а. 6 б. 5 в. 4 г. 3 д. 2
17. Процесс разобщения дыхания и фосфорилирования характеризуется изменением процессов в митохондрии:
а прекращением переноса электронов в дыхательной цепи
б. прекращением синтеза АТФ
в. прекращением синтеза АТФ при сохранении процесса переноса электронов
г. прекращением синтеза АТФ и процесса переноса электронов
д. сохранением синтеза АТФ при прекращении переноса электронов
18. Физиологические разобщители
а. глюкоза, гормон тироксин
б. глюкоза, высшие карбоновые кислоты
в. глюкоза, билирубин
г. глюкоза, билирубин, гормон тироксин
д. билирубин, высшие карбоновые кислоты, гормон тироксин
19. Разобщение дыхания и фосфорилирования связано с изменением температуры ткани:
а повышает температуру
б. не влияет на температуру
в. снижает температуру
г. может наблюдаться понижение или повышение
д. может наблюдаться сохранение или понижение
20 . Субстратное фосфорилирование – это биохимический процесс
а. гидролиза АТФ
б. использования АТФ для фосфорилирования другого вещества- субстрата
в. синтеза АТФ за счет макроэргической связи другого субстрата, содержащего макроэргическую связь
г. синтеза АТФ, связанный с переносом электронов
д. синтеза предшественников АТФ.
21. Окислительное фосфорилирование – это биохимический процесс
а. гидролиза АТФ
б. использования АТФ для фосфорилирования другого вещества- субстрата
в. синтеза АТФ за счет макроэргической связи другого вещества - макро-
эргического субстрата
г. синтеза АТФ, связанный с переносом электронов
д. синтеза предшественников АТФ.
22. Основная функция электронтранспортной цепи системы МСО :
а. синтез АТФ г. синтез АТФ и метаболизм субстратов
б. метаболизм субстратов д. синтез АТФ и теплопродукция.
в. теплопродукция
23. Химическую реакцию 2 Н2О2 = О2 + 2 Н2О в тканях и биологических жидкостях (кровь, слюна ) катализирует фермент :
а. каталаза г. цитохром в-5-редуктаза
б. супероксиддисмутаза д. цитохром с-редуктаза
в. пероксидаза
24. В норме на образование активных форм используется доля поступающего в организм кислорода ( в % ):
а. 35 б. 25 в. 20 г. 15 д . 5
25. Кофермент каталазы:
а. НАДН б. ФАДН2 в. НАДФН г. аскорбат д. гем
26. Неферментативная антиоксидантная защита базируется на витаминах:
а. РР, В2 в. РР, В2, аскорбиновая кислота
б. А, Е г. А, Е, аскорбиновая кислота
д. А, Е, РР
27. Белок плазмы крови - антиоксидант:
а. глобулин г. фибриноген
б. церулоплазмин д. глутатион
в. альбумин
28. Ферменты антиоксидантной защиты ( АОЗ ) :
а. каталаза г. глутатионпероксидаза
б. супероксиддисмутаза д. каталаза и супероксиддисмутаза
в. глутатионредуктаза
29. Ферменты антиперекисной защиты ( АПЗ ):
а. каталаза и супероксиддисмутаза
б. глутатионпероксидаза и каталаза
в. супероксиддисмутаза и глутатионпероксидаза
г. супероксиддисмутаза, каталаза, глутатионредуктаза
д. каталаза, глутатионпероксидаза, глутатионредуктаза
30.Недостаток витамина никотиновая кислота сопровождается развитием алиментарного заболевания:
а. пеллагра г. рахит
б. бери-бери д. « куриная слепота »
в. цинга
Попробуйте самостоятельно ответить на вопросы повышенной сложности
1. Гипертиреоз (усиленная продукция щитовидной железой тиреоидных гормонов)
может сопровождаться повышением температуры тела. Какой механизм развития гипертермии характерен для этой ситуации?
2. Гипертиреоз сопровождается повышением аппетита и снижением массы тела. Какой механизм усиления катаболических процессов можно предложить, применив известную Вам информацию из раздела «биологическое окисление».
3. В составе лекарственного препарата содержится лимонная кислота. Укажите значение коэффициента ( Р : О ) для этого метаболита.
4. Природный метаболит - янтарная кислота - является эффективным профилактическим и лечебным препаратом, поддерживающим энергетический обмен при недостаточном поступлении кислорода в организм (сердечно-сосудистая патология, пожилой возраст ).
Объясните роль сукцината, основываясь на знании процессов биологического окисления.
5. Отравление цианистым калием практически всегда сопровождается летальным исходом вследствие нарушения функции дыхательного центра. Объясните механизм действия иона цианида на электронтранспортную систему митохондрий.
6. При высокой концентрации этанола в организме фермент каталаза включается в процесс его метаболизма, выступая в роли пероксидазы, используя перекись водорода. Особенно этот путь характерен для печени и сердца и является одной из причин развития патологических процессов в этих органах.
Б. аскорбиновая кислота + супероксид-анион
7. Аскорбиновая кислота является важнейшим представителем неферментативной защиты в клетке. Как изменяется содержание витамина С в организме :
А. после посещения студии для загара?
Б. у курильщика по сравнению с некурящим?
В. в течение длительного хронического заболевания?
ОТВЕТЫ НА ТЕСТЫ (1 -70)
1 б |
16 г |
2 в |
17 в |
3 б |
18 д |
4 г |
19 а |
5 а |
20 в |
6 а |
21 г |
7 г |
22 б |
8 б |
23 а |
9 а |
24 д |
10 г |
25 д |
11 б |
26 г |
12 г |
27 б |
13 г |
28 б |
14 в |
29 д |
15 а |
30 а |
ЛИТЕРАТУРА ДЛЯ ПОДГОТОВКИ:
