
- •Контрольные работы № 2 и 3
- •«Общая, неорганическая и физическая химия»
- •Содержание
- •Введение
- •Контрольная работа № 2
- •(Неорганическая химия)
- •Задание 1
- •Строение атомов и периодическая система
- •Контрольные задачи
- •Задание 2 Основные классы неорганических соединений.
- •Контрольные задачи
- •Задание 3. Комплексные соединения
- •Контрольные задачи
- •Задание 4. Электролитическая диссоциация pн-растворов
- •Контрольные задачи
- •Задание 5 Ионно-обменные реакции. Произведение растворимости
- •Контрольные задачи
- •Задание 6 Окислительно-восстановительные реакции
- •Контрольные задачи
- •Контрольные задачи
- •Задание 2 Энтропия. Энергия Гиббса
- •КоНтРольные задачи
- •Задание 3 Влияние температуры на химическое равновесие
- •Контрольные задачи
- •Задание 4 Химическая кинетика и равновесие
- •Контрольные задачи.
- •Фазовые равновесия. Законы Коновалова. Азеотропные смеси.
- •Контрольные задачи.
- •Задание 6 Электропроводность электролитов
Задание 2 Основные классы неорганических соединений.
К основным классам неорганических соединений относятся: оксиды, кислоты, основания и соли. Например: CaO – оксид кальция, H2SO4 - серная кислота, Ca(OH)2 – гидроксид кальция, CaSO4 – сульфат кальция.
Оксиды делятся на основные, кислотные и амфотерные. Например: CaO, SO3 и Al2O3. Кислоты диссоциируют с образованием Н+ и кислотного остатка, а основания - с образованием ОН- и катиона металла.
Соли можно рассматривать как продукт взаимодействия кислоты с основанием. При этом могут образовываться средние, кислые или основные соли:
H2SO4 + Ca(OH)2 = CaSO4 + 2H2O,
2H2SO4 + Ca(OH)2 = Ca(HSO4)2 + H2O,
H2SO4 + 2Ca(OH)2 = (CaOH)2SO4 + H2O.
Пример
Ca(HCO3)2 – гидрокарбонат кальция
Кислая соль, образованная угольной кислотой и гидроксидом кальция.
Графическая формула:
Ca
O
O
O
O
O
O
C
C
H
H


Диссоциирует по типу сильного электролита:
![]()
Ион
![]() диссоциирует по типу слабого электролита:
диссоциирует по типу слабого электролита:
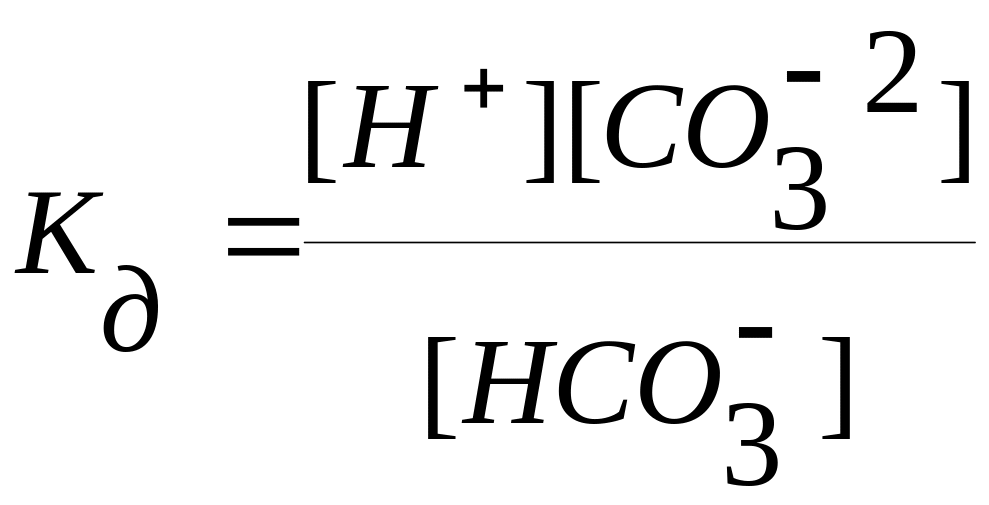
![]()
![]() ,
,
Контрольные задачи
Назовите по систематической номенклатуре и запишите формулы соединений, приведенных в Вашем варианте (табл. 2).
К какому классу неорганических соединений относится каждое из них? Приведите графические формулы данных соединений.
Напишите уравнения электрической диссоциации данных соединений и выражения констант диссоциации для слабых электролитов.
Таблица 2 – Контрольные задачи к заданию № 2.
№ задач |
Формулы и названия неорганических соединений |
21 |
H3PO4, [Al(OH)2 ]2SO4, гидросульфит кальция, ортокремнивая кислота |
22 |
H6TeO6, PbOHNO3, ацетат гидроксоалюминия, гидроортофосфат таллия ( I ) |
23 |
H3BO3, Na2ZnO2, гидроортоарсенат аммония, сероводородная кислота |
24 |
Н2S, Al(OH)3, гидрокарбонат кальция, селенистая кислота |
25 |
KHZnO2, H2SeO4,метаванадат аммония, гидроксид висмута |
26 |
K2GeO3, Na2HPO4,метаарсенит калия, ортосурьмяная кислота |
27 |
Co(OH)2, K2H4TeO6, метаванадиевая кислота, цинкат натрия |
28 |
HBrO3, Zn(H2PO4)2,ортофосфат висмута (III), гидроксид цинка |
29 |
Na3H3TeO6, Ca(OH)2, ортоарсенит калия, селеновая кислота |
30 |
RbOH, Ca(HS)2, гидросульфит калия, ортофосфористая кислота |
31 |
Sr (OH)2, KH2AsO4, нитрат цинка, гидроксид железа (II) |
32 |
Zn(HCO3)2, Be(OH)2,метасурьмяная кислота, гидросульфид кальция |
33 |
Ag2Se, Mg(HSO4)2, дигидроортофосфат натрия, гидроксид марганца (IV) |
34 |
Zn(NO3)2, H3SbO4, гидрокарбонат цезия, гидроксид бария |
35 |
Ba(OH)2, H2Se, гидроксид аммония, гидроортофосфат натрия |
36 |
Ca(HCO3)2, Mn(OH)2, гидроортоарсенит натрия, сернистая кислота |
37 |
Ca3(PO4)2, H2S, гидроортофосфат кальция, гидроксид алюминия |
38 |
Cu(NO3)2, NaHCO3, сульфид алюминия, хлорид дигидроксо цинка |
39 |
Zn(OH)2, Ca(H2PO4)2, перманганат кальция, гидросульфид натрия |
40 |
Mg(OH)2, AlOHSO4,нитрит кальция, сульфат железа (III) |
