- •Розділ ііі Основи теорії сплавів
- •Тема 3.1. Основні поняття із теорії сплавів
- •Тема 3.2. Діаграми стану подвійних сплавів
- •Поняття про діаграми стану сплавів, їх побудова.
- •Діаграми стану для випадку утворення компонентами механічної суміші, твердого розчину необмеженого і обмеженого, хімічної сполуки.
- •Зв’язок між діаграмами стану і властивостями.
- •Діаграма стану сплавів-механічних сумішей (і роду)
- •Правило відрізків (важеля)
- •Діаграма стану для випадку утворення компонентами необмеженого твердого розчину (іі роду)
- •Діаграма стану для випадку утворення компонентами обмеженого твердого розчину (ііі роду)
- •Діаграма стану для випадку утворення компонентами хімічної сполуки (іv роду)
- •Зв’язок між властивостями сплаву і типом діаграми стану
- •Розділ іv. Залізовуглецеві сплави
- •Тема 4.1. Діаграма стану залізо-цементит
- •Діаграма стану Fe-Fe3c
- •Тема 4.2. Вуглецеві сталі
- •Тема 4.3. Чавуни
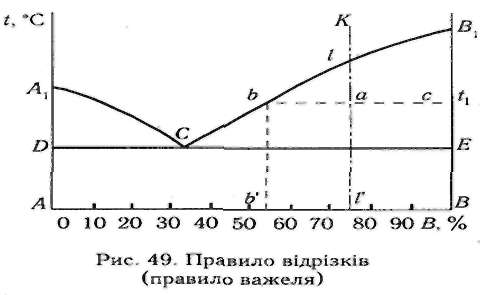
Правило відрізків (важеля)
Це правило дозволяє визначити співвідношення твердої і рідкої фаз, а також концентрацію рідкої фази в будь-який момент кристалізації сплаву.
Щоб визначити кількість твердої і рідкої фази сплаву К в точці а, треба через точку а провести горизонтальну лінію до перетину з лініями діаграми, що обмежують дану область (отримаємо відрізок bc) (див. рис.3.6). Кількість твердої фази
Кількість
рідкої фази
|
|
Рисунок 3.6. Правило відрізків (важеля). |
Тобто, Qтв – відношення довжини відрізка, що прилягає до рідкої частини сплаву, до довжини всього відрізка;
Qр – відношення довжини відрізка, що прилягає до твердої частини сплаву, до довжини всього відрізка.
Концентрація рідкої фази в будь-якій точці сплаву визначається проекцією даної точки на лінію ліквідус. Так, рідка фаза сплаву К в точці а буде містити b1 % компоненту В (точка b – проекція точки а на лінію ліквідус, точка b1 – проекція точки b на вісь концентрацій). При охолодженні сплаву К концентрація компоненту В зменшується по лінії В1С, а при температурі евтектичного перетворення досягає концентрації В в точці С (евтектична концентрація).
Діаграма стану для випадку утворення компонентами необмеженого твердого розчину (іі роду)
AmB – лінія ліквідус; AnB – лінія солідус (рис.3.7).
Точка А – початок і кінець кристалізації компоненту А; точка В – початок і кінець кристалізації компоненту В.
Лінії ліквідус і солідус показують, що початок і кінець кристалізації відбуваються при різних температурах для різних сплавів системи.
Розглянемо процес кристалізації сплаву К.
Вище точки 1 сплав знаходиться в рідкому стані.
В точці 1 починається кристалізація сплаву – з рідкого розчину виділяються кристали твердого розчину α компоненту В в компоненті А.
В інтервалі 1-2 сплав знаходиться у двохфазному стані: рідина + кристали α-твердого розчину. С=К+1–Ф=2+1–2=1, - тобто концентрація компонентів у фазах змінюється з температурою.
Точка 2 – кінець кристалізації.
Нижче точки 2 сплав повністю закристалізувався і складається з кристалів α-твердого розчину, тобто є однофазним.

Рисунок 3.7. Діаграма стану ІІ роду, крива охолодження і схеми структур.
Кількість
твердої фази в точці а -
![]() ;
рідкої фази -
;
рідкої фази -
![]() ;
склад рідини відповідає концентрації
в точці b,
склад α-твердого розчину – концентрації
в точці с.
;
склад рідини відповідає концентрації
в точці b,
склад α-твердого розчину – концентрації
в точці с.
Діаграма стану для випадку утворення компонентами обмеженого твердого розчину (ііі роду)
КСD – лінія ліквідус; КEСF – лінія солідус (рис.3.8).
Лінія ES – лінія зміни розчинності компонента В в компоненті А; із збільшенням температури розчинність В в А зростає від мінімальної в точці S до максимальної в точці E (при евтектичній температурі).
ECF – лінія евтектичного перетворення
Р → Евт.( α + В)
Е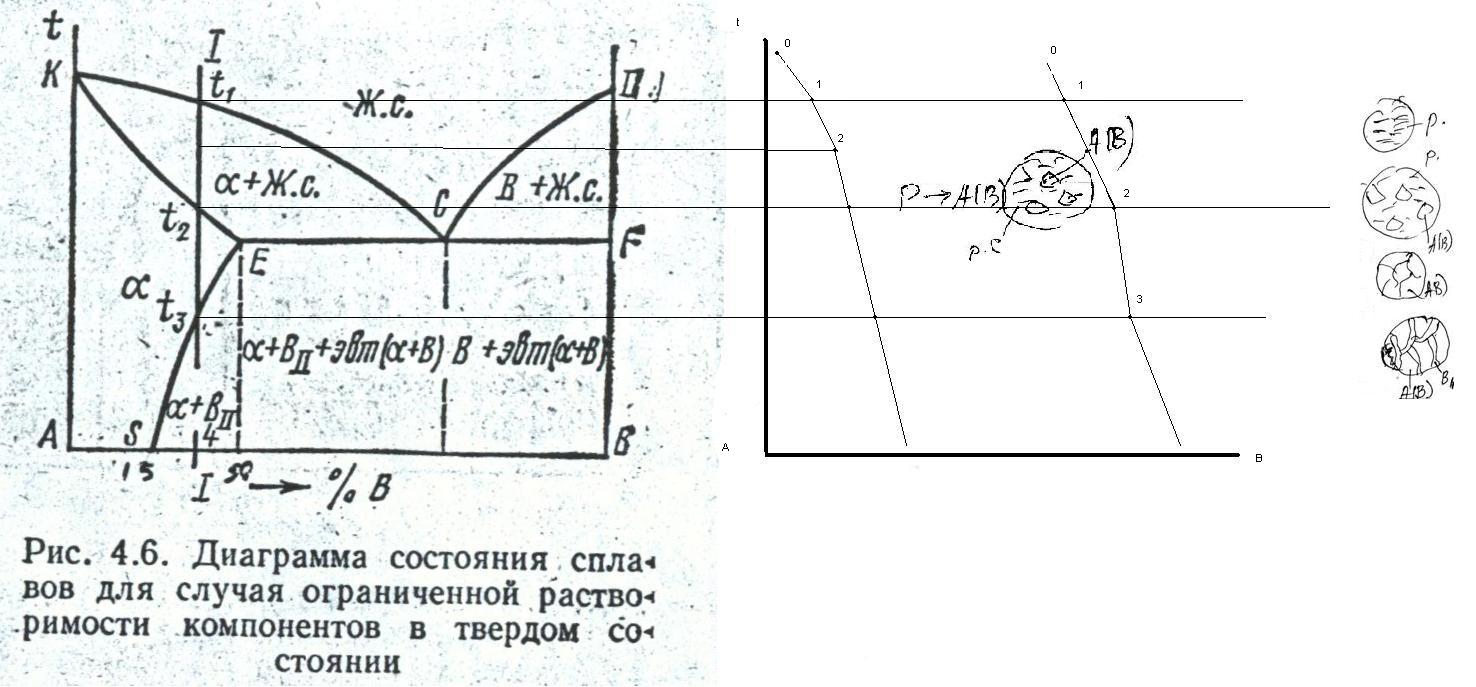 втектика
складається з α-твердого розчину і
компоненту В.
втектика
складається з α-твердого розчину і
компоненту В.
Рисунок 3.8. Діаграма стану ІІІ роду і криві охолодження.
При охолодженні нижче лінії евтектики з α-твердого розчину випадають кристали компонента В – ВІІ (вторинні кристали) через зменшення розчинності.
Розглянемо перетворення в сплаві І при охолодженні:
вище точки 1 – в рідкому стані;
1-2 – з рідини виділяються кристали α-твердого розчину;
2-3 - α-твердий розчин, що повністю за кристалізувався;
нижче точки 3 – виділення з α-твердого розчину вторинних кристалів компоненту В по границях зерен.
Кристалізація сплавів, що знаходяться правіше точки Е, відбувається аналогічно випадку утворення механічної суміші (розглянуто раніше).
|
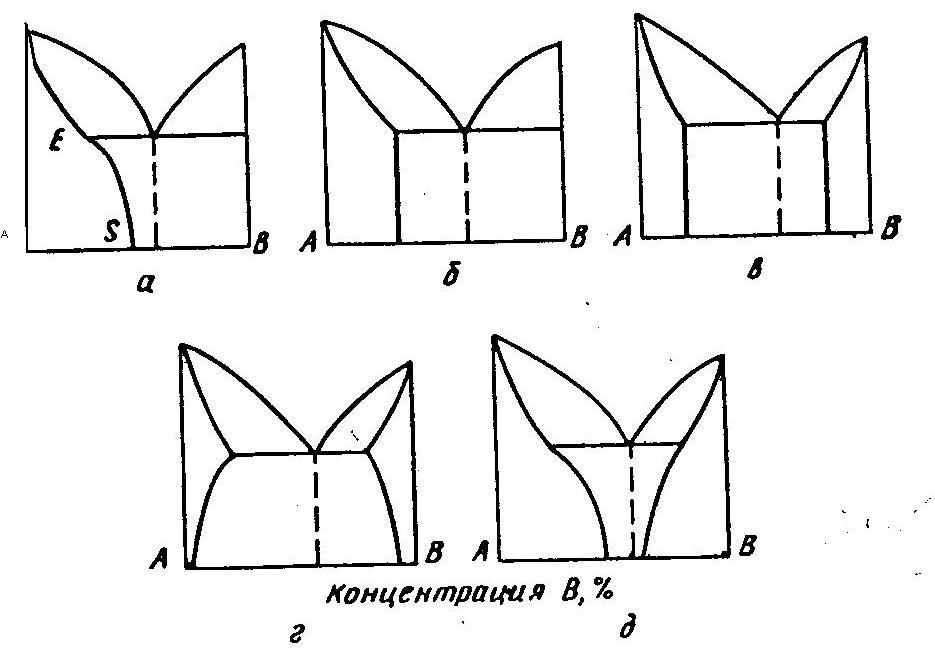
а) одностороння, зменшується з підвищенням температури; б) одностороння, стала; в) двостороння, стала; г) двостороння, збільшується з підвищенням температури; д) двостороння, зменшується з підвищенням температури. |
Рисунок 3.9. Різні варіанти обмеженої розчинності: |
|