
- •060101 65 – Лечебное дело, 060103 65 – Педиатрия, 060105 65 – Стоматология, 060104 65 – Медико-профилактическое дело
- •Тема 1. Поверхностные явления 12
- •Предисловие
- •Введение
- •Тема 1. Поверхностные явления
- •1. Свободная поверхностная энергия, поверхностное натяжение
- •2. Смачивание, адгезия, когезия
- •3. Сорбция и ее виды
- •Абсорбция
- •Адсорбция на подвижной поверхности раздела фаз
- •Адсорбция пав в системе воздух-вода
- •Адсорбция на неподвижной поверхности раздела фаз
- •Молекулярная (неэлектролитов) адсорбция из растворов.
- •Адсорбция ионов из растворов
- •Ионообменная адсорбция
- •Основные физико-химические характеристики ионитов
- •4. Хроматография
- •5. Биологические поверхностно-активные вещества
- •6. Медико-биологическое значение адсорбции
- •Типы сорбентов, использующихся для удаления различных веществ
- •Основные области применения энтеросорбентов
- •Тема 2. Дисперсные системы
- •1. Классификация дисперсных систем
- •Свободно- и связнодисперсные системы
- •Лиофобные и лиофильные дисперсные системы
- •Классификация дс по агрегатному состоянию дисперсной фазы и дисперсионной среды
- •2. Методы получения и очистки дисперсных систем
- •Методы очистки дисперсных систем
- •3. Лиофобные коллоидные растворы
- •Строение мицелл в лиофобных коллоидных растворах
- •Устойчивость лиофобных коллоидных растворов
- •Кинетика коагуляции
- •Механизм коагуляции
- •Пептизация или физико-химическое диспергирование
- •Коллоидная защита и флокуляция
- •4. Лиофильные коллоидные растворы
- •Истинный раствор ((;(( коллоидный раствор.
- •Зависимость области применения пав от значения глб
- •Свойства лиофильных коллоидных растворов пав и вмс
- •Ослабление высаливающего действия
- •Солюбилизация
- •5. Микрогетерогенные дисперсные системы
- •Аэрозоли и их свойства
- •Порошки и их свойства
- •Суспензии и их свойства
- •Эмульсии и их свойства
- •Пены и их свойства
- •Тема 3. Свойства вмс и их растворов
- •Классификация вмс
- •Полимерные полиэлектролиты и их свойства
- •Свойства растворов вмс, общие с истинными растворами:
- •Кислотно-основные свойства белков
- •Значения pI белков живого организма
- •Окислительно-восстановительные свойства белков
- •Комплексообразующие свойства белков
- •Поверхностные свойства белков
- •3. Набухание и растворение вмс
- •4. Вязкость растворов вмс
- •5. Осмотические свойства растворов вмс
- •6. Мембранное равновесие Доннана
- •7. Устойчивость и разрушение растворов вмс
- •8. Застудневание (желатинирование). Возникновение связнодисперсных систем и их свойства
- •Обучающие тесты
- •Обучающие задачи
- •Учебно-исследовательские лабораторные работы
- •Тема I. Поверхностные явления
- •Тема: Адсорбция уксусной кислоты на активированном угле. Качественные опыты по адсорбции и хроматографии
- •Тема: Определение обменной емкости ионита
- •Тема: Изотерма поверхностного натяжения и адсорбции изоамилового спирта на твердом адсорбенте
- •Учебно-исследовательская лабораторная работа № 4 Тема: Изучение адсорбции пав на твердом адсорбенте из водных растворов
- •Тема II. Дисперсные системы
- •Тема: Получение и свойства лиофобных коллоидных растворов
- •Конденсационный метод получения золей (химическая конденсация)
- •II. Дисперсионный метод получения золей.
- •Тема: Устойчивость и коагуляция лиофобных коллоидных растворов. Коллоидная защита
- •Тема: Получение и свойства эмульсий
- •Тема III. Растворы вмс
- •Учебно-исследовательская лабораторная работа №8
- •Тема: Вискозиметрическое определение молекулярной
- •Массы полимера
- •Тема: Набухание вмс
- •Тестовые задания, задачи, упражнения для самостоятельного решения
- •Тема 1. Поверхностные явления
- •Тема II. Дисперсные системы
- •Тема III. Растворы вмс
- •Тестовый контроль по теме: «Поверхностные явления».
- •Тестовый контроль по теме: «Лиофобные коллоидные растворы»
- •Тестовый контроль по теме: «Свойства вмс и их растворов».
- •Темы реферативных докладов для студентов лечебного, педиатрического, стоматологического и медико-профилактического факультетов
- •Список использованной литературы
- •Приложение
- •1. Основные единицы измерения физических величин
- •2. Основные физические постоянные
- •3. Метрическая система мер
- •4. Множители и приставки для образования десятичных кратных и дольных единиц и их обозначения
- •5. Плотность пав в жидком состоянии
- •6. Зависимость поверхностного натяжения воды от температуры
- •7. Поверхностное натяжение жидкостей при 293 k
- •Зависимость адсорбции газов на древесном угле от
- •9. Золотые числа
- •10. Критические концентрации мицеллообразования для некоторых мыл
- •11. Значения констант в уравнении Марка-Хаувинка и омм полимеров
Адсорбция пав в системе воздух-вода
Вода является полярной фазой, воздух – неполярной, т.к. состоит из неполярных молекул азота и кислорода. В соответствии с правилом Ребиндера молекула ПАВ ориентируется на границе раздела фаз таким образом, что полярная группа направлена в воду, а гидрофобная часть - к неполярной части (воздух), выравнивая, таким образом, полярность контактирующих фаз. При этом на границе раздела фаз образуется мономолекулярный слой ПАВ.
У дифильных молекул с короткой углеводородной цепью преобладают гидрофильные свойства, поэтому такие молекулы хорошо растворимы в воде. С удлинением углеводородной цепи усиливаются гидрофобные свойства молекул, и понижается их растворимость в воде, поэтому они в большей степени вытесняются на поверхность, вызывая снижение поверхностного натяжения.
Влияние природы ПАВ на их поверхностную активность описывается правилом Траубе-Дюкло (рис. 4):
Поверхностная активность ПАВ в разбавленных водных растворах при одинаковой молярной концентрации увеличивается в 3-3,5 раза при удлинении гидрофобной части на одну метиленовую группу (–СН2 –).
И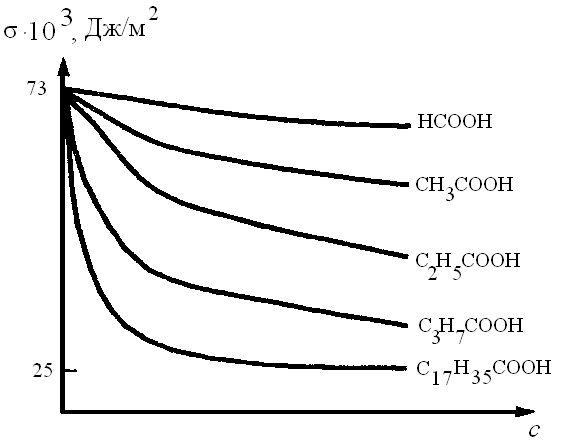 з
графика видно: чем длиннее углеводородная
цепь, тем больше снижается поверхностное
натяжение водного раствора.
з
графика видно: чем длиннее углеводородная
цепь, тем больше снижается поверхностное
натяжение водного раствора.
Рис. 4. Зависимость поверхностного натяжения от природы ПАВ
Правило Траубе-Дюкло соблюдается для водных растворов некоторых ПАВ при небольшой длине УВ-радикала и комнатной температуре.
В зависимости от концентрации ПАВ в растворе строение поверхностного слоя будет различным. При небольших концентрациях молекул в поверхностном слое углеводородные цепи лежат на поверхности, а полярная группа погружена в воду. По мере увеличения концентрация ПАВ углеводородные цепи поднимаются и при концентрации, которая соответствует мономолекулярному слою, полностью заполняющему поверхность, они размещаются перпендикулярно поверхности. При дальнейшем увеличении концентраций ПАВ в растворе строение адсорбционного слоя, а также поверхностное натяжение не изменяются.
Для характеристики поверхностной активности молекул ПАВ можно использовать их гидрофильно-липофильный баланс (ГЛБ). ГЛБ заключается в том, что в молекуле любого поверхностно-активного вещества имеется определенное соотношение между активностями гидрофильных и гидрофобных групп. От соотношения гидрофильных и гидрофобных свойств зависит пригодность ПАВ для той или иной цели. Так, для пеногасителей нужны ПАВ, в молекулах которых гидрофобные свойства значительно превосходят гидрофильные. Для получения эмульсий масло в воде необходимы ПАВ, в молекулах которых гидрофильные свойства уже становятся заметными, но гидрофобные свойства еще сильно преобладают. Для получения эмульсий воды в масле нужны ПАВ, в молекулах которых гидрофобные свойства уже близки к гидрофильным свойствам. При использовании ПАВ в качестве моющих средств применяют вещества, в молекуле которых гидрофобные свойства выражены незначительно меньше, чем гидрофильные свойства.
Ж идкости,
резко отличающиеся по полярности,
например, вода и масло, при смешивании
всегда расслаиваются. Появится граница
раздела между ними. Если в этой системе
растворить ПАВ, то они будут адсорбироваться
на границе раздела фаз, снижая межфазное
поверхностное натяжение. Молекулы ПАВ
своей полярной гидрофильной частью
будут ориентированы к воде (полярной
жидкости), а гидрофобной - к маслу
(неполярной жидкости). Положение молекул
ПАВ на границе будет зависеть от
соотношения активностей полярного и
неполярного фрагментов, т.е. от величины
ГЛБ.
идкости,
резко отличающиеся по полярности,
например, вода и масло, при смешивании
всегда расслаиваются. Появится граница
раздела между ними. Если в этой системе
растворить ПАВ, то они будут адсорбироваться
на границе раздела фаз, снижая межфазное
поверхностное натяжение. Молекулы ПАВ
своей полярной гидрофильной частью
будут ориентированы к воде (полярной
жидкости), а гидрофобной - к маслу
(неполярной жидкости). Положение молекул
ПАВ на границе будет зависеть от
соотношения активностей полярного и
неполярного фрагментов, т.е. от величины
ГЛБ.
