
- •Оглавление
- •Глава 5. Собственный материал и исследования 128
- •Глава 6. Клиническая картина видов хронической артериальной ишемии конечностей 142
- •Глава 7. Лечение хроническИх артериальных ишемий конечностей 159
- •Глава 1.Используемые сокращения
- •Хаик– хроническая артериальная ишемия конечностей
- •Введение
- •Глава 2. Современные представления о хронических артериальных ишемиях конечностей (обзор литературы)
- •2.1.Хронические артериальные ишемии конечностей: вертеброгенные, ангиоспастические и при облитерирующих заболеваниях артерий
- •2.2.Классификации артериальных ишемий конечностей
- •2.2.1.При функциональных заболеваниях артерий
- •2.2.2.При органических заболеваниях артерий
- •2.3.Лечение хронических артериальных ишемий конечностей
- •Консервативное лечение хронической артериальной ишемии конечностей Медикаментозное лечение
- •Физиотерапевтические методы лечения
- •Оксигенобаротерапия
- •Нетрадиционные методы лечения
- •Оперативное лечение хронической артериальной ишемии конечностей
- •Обсуждение оперативных методов лечения
- •Глава 3. Собственная классификация хронических артериальных ишемий конечностей
- •Классификация хронических артериальных ишемий конечностей
- •Глава 4. Диагностика артериальных ишемий конечностей
- •4.1.Методы клинической диагностики
- •4.2. Методы функциональной диагностики
- •4.2.1.Реовазография
- •4.2.2.Термография
- •4.2.3.Рентгенография
- •4.2.4.Рентгеноконтрастная артериография
- •4.2.5.Внутриартериальная радиоизотопная ангиосцинтиграфия
- •Техника исследования
- •Меры предосторожности
- •Оценка сцинтиллятионной картины сегментов конечности в разных проекциях
- •4.2.6.Ультразвуковая допплерография
- •Качественный анализ допплеровских кривых усредненной по объему скорости кровотока
- •4.2.7.Лазерная флоуметрия (допплерография)
- •4.2.8.Транскутанное определение напряжения кислорода
- •Глава 5. Собственный материал и исследования
- •5.1.Количество больных и их распределение по группам
- •5.2.Виды и количество диагностических исследований
- •Глава 6. Клиническая картина видов хронической артериальной ишемии конечностей
- •6.1.Клиника ангиоспастической хронической артериальной ишемии конечностей
- •6.2.Клиническая картина хронической артериальной ишемии конечностей при облитерирующих заболеваниях
- •6.3.Дифференциальная диагностика форм хронической артериальной ишемии конечностей
- •Глава 7. Лечение хроническИх артериальных ишемий конечностей
- •7.1.Общие принципы и тактика лечения
- •7.2.Биохирургические методы лечения
- •7.2.1.Биохирургическая сегментарная реваскуляризация конечностей
- •7.2.2.Подвздошная биохирургическая реваскуляризация
- •Техника подвздошной биохирургической реваскуляризации
- •7.2.3.Тазовая биохирургическая реваскуляризация
- •Техника тазовой биохирургической реваскуляризации
- •7.2.4.Направленная биохирургическая реваскуляризация
- •7.3.Мануальные методы лечения
- •7.4.Лазерные методы лечения
- •Техника выполнения лазерных процедур Реваскуляризация паравертебральных симпатических ганглиев
- •Лазеропунктурная реваскуляризация конечностей
- •Сканирующее облучение
- •Облучение крови
- •7.5.Хирургические методы лечения
- •7.5.1.Восстановительные операции на магистральных артериях
- •7.5.2.Операции Илизарова-Зусмановича
- •7.5.3.Ампутации
- •7.6.Исходы лечения больных с хаик
- •Заключение
- •Практические рекомендации
- •Список литературы
Глава 2. Современные представления о хронических артериальных ишемиях конечностей (обзор литературы)
Ангиология давно приковывала к себе внимание врачей разных специальностей. Это внимание с течением времени возрастает. Причин две: прогрессирующая распространенность среди населения земного шара болезней системы периферического кровообращения и неудовлетворенность эффективностью методов и средств лечения (Вишневский А.А., Краковский Н.И., Золотаревский В.Я., 1972).
2.1.Хронические артериальные ишемии конечностей: вертеброгенные, ангиоспастические и при облитерирующих заболеваниях артерий
Артериальные ишемии конечностей находятся в числе главнейших проблем нашего столетия. В изучение этого заболевания внесла большой вклад плеяда выдающихся отечественных и зарубежных ученых: Brown-Sequard, Cannon, В.И.Шевкуненко, Б.А.Долго-Сабуров, Л.А.Орбели, В.А.Оппель, А.Д.Сперанский, Alexander, Lerich, Fontaine, А.В.Вишневский, А.А.Вишневский и др. Опубликовано большое число монографий, которые стали руководством для практической работы ангиологов и ангиохирургов. Однако все еще не разрешены узловые вопросы этиологии и патогенеза, не разработаны способы и методы эффективного этиопатогенетического лечения, а отсюда вытекает неудовлетворенность его результатами.
В настоящее время известно, что хронические артериальные ишемии конечностей возникают в результате функциональных и органических заболеваний периферических артерий (Бондарчук А.В., 1969). Группа функциональных заболеваний включает в себя общие и местные вазопаралитические и вазоспастические заболевания. Выделена особая группа ангионеврозов в связи с общим и местным поражением сосудистых центров, сосудистой иннервации. Повышенная реакция сосудов чаще проявляется в виде спазма и редко - расширения. Это объясняется конституциональной или наследственной предрасположенностью к необычно повышенной реакции на обычные внешние, чаще климатические, раздражения (А.В.Бондарчук, 1969).
В "Основах физиологической хирургии" Рене Лериша (1955) есть глава "Вегетативная жизнь артерий". Вот некоторые из основных ее положений.
"Артерия реагирует на раздражение сегментарным спазмом, и он может быть длительным. К сосудам конечностей через более или менее равные промежутки подходят симпатические веточки от близлежащих смешанных нервных стволов. Однако кроме сегментарной иннервации, исходящей из паравертебральной симпатической цепочки, на денервированной конечности сохраняется автономная сосудистая реакция на местное раздражение". Опытами, проведёнными проф. Леришем с 1935 по 1946 годы, было доказано существование сегментов артерии и их независимость относительно друг друга. Эти расположенные в линию сегменты являются функционально независимыми друг от друга, образуют ряд маленьких периферических сердечек, следующих деятельности сердца (де Моран Ж.С., 1997). Доказано наличие ганглионарных нервных клеток, принадлежащих симпатической нервной системе, находящихся в периартериальном сосудисто-нервном сплетении (Долго-Сабуров Б.А., 1936; Серанова А.И., 1952; Myers H.A. et al., 1975 ) , к которым подходят симпатические волокна из соматических нервных стволов. Следует заметить, что под контролем сегментарной симпатической иннервации находятся как мышечные сосуды, так и vasa vasorum et vasa nеrvorum. В соматические стволы через определенные промежутки (от 2 до 7 см в зависимости от толщины ствола) проникают артерии, подпитывающие центральную артерию нервного ствола (Огнев Б.В., 1950).
И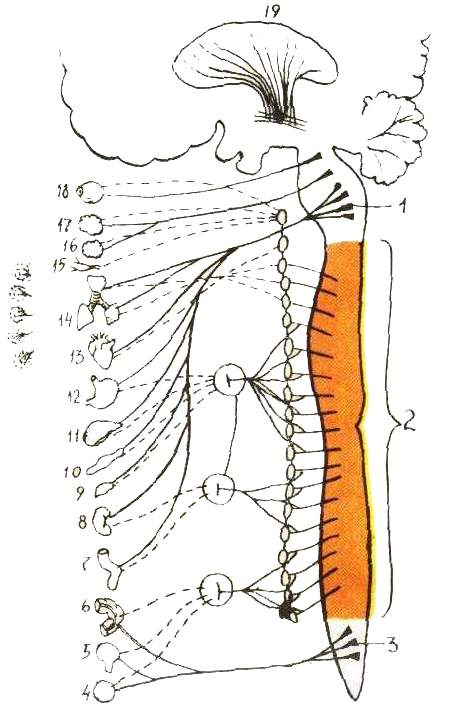 мея
в настоящее время такие данные по
анатомо-физиологическим взаимоотношениям
симпатических нервных структур с
сосудистыми, необходимо сделать последний
шаг в изучении вопроса о поведении
капиллярных микрососудов, питающих
стенку артерий и нервные стволы. Этот
вопрос совершенно не изучен (Чернух
А.М., Александров П.Н., Алексеев О.В.,
1984).
мея
в настоящее время такие данные по
анатомо-физиологическим взаимоотношениям
симпатических нервных структур с
сосудистыми, необходимо сделать последний
шаг в изучении вопроса о поведении
капиллярных микрососудов, питающих
стенку артерий и нервные стволы. Этот
вопрос совершенно не изучен (Чернух
А.М., Александров П.Н., Алексеев О.В.,
1984).
Общая схема вегетативной нервной системы:
1 – центры парасимпатической системы в головном мозгу (краниальный отдел); 2 – центры симпатической нервной системы; 3 – центры парасимпатической системы в нижнем конце спинного мозга (крестцовый отдел); 4 – половые органы; 5 – мочевой пузырь; 6 – толстая кишка; 7 – тонкая кишка; 8 – почка; 9 – надпочечник; 10 – поджелудочная железа; 11 – печень; 12 – желудок; 13 – сердце; 14 – легкое; 15 – сосуды головы; 16, 17 – слюнные железы; 18 – глаз; 19 – полосатое тело
Базовый тонус мышечных артерий определяется симпатической нервной системой (рис.1). Центральная ее часть представлена клетками задних рогов спинного мозга шейно-грудного и верхнепоясничного и крестцового утолщений. Спинномозговые симпатические центры через передние корешки спинного мозга связаны аксонами (белые соединительные волокна) с паравертебральными симпатическими ганглиями, расположенными по обе стороны позвоночника, образуя "симпатическую цепочку", от которых отходят аксоны на периферию в составе соматических нервов. В этой цепочке имеются 20-22 узла: 3 шейных (нижний шейный, объединяясь с верхнегрудным, образует звёздчатый узел), 10-12 грудных, 3-4 брюшных и 4 тазовых. Преганглионарные волокна, подходящие к ганглиям, частично прерываются в нейронах узлов, частично идут к превертебральным ганглиям. Волокна одного нейрона могут подходить к нескольким узлам симпатической цепочки (до 8). Анатомическое строение аксональных связей спинномозговых центров с паравертебральными ганглиями и межганглионарных обеспечивает страховку функции любого симпатического узла двумя соседними узлами. Об этом факте нужно помнить, когда снижение функциональной активности одного симпатического узла каким-либо патологическим процессом в одноименном позвоночно-двигательном сегменте (ПДС) страхуется более высокой активностью соседних узлов. Постганглионарные волокна от верхнего шейного узла по ходу сонной артерии идут к мозгу и лицу, от звёздчатого узла - в сплетении позвоночной артерии к сосудам мозга, от грудных, брюшных и тазовых узлов - к превертебральным узлам и сплетениям (Вейн А.М., 1991). Периферическая симпатическая нервная система представлена периартериальными симпатическими сплетениями с ганглионарными нервными клетками (Долго-Сабуров Б.А., 1936). Только симпатическую иннервацию имеют мышечные сосуды, мочеточники, надпочечники, потовые железы и гладкая мускулатура волосяных мешочков. Степень выраженности основного сосудистого тонуса находится в зависимости от состояния центральных отделов симпатической нервной системы и местных влияний на клетки периартериального симпатического сплетения. Сосудосуживающее действие симпатических волокон обнаружил ещё в 1842 году Вальтер. Симпатические центры спинного мозга определяют уровень возбуждения паравертебральных симпатических ганглиев (Григорьева Т.А., 1952; Шевелева В.С., 1977), которые, посылая 1-2 импульса в секунду по аксонам на периферию, обеспечивают базовый тонус артерий мышечного типа на 25% их возможности. Однако в этом участвует и периферическая нервная симпатическая система, ибо центральная денервация не приводит к полной дилятации этих сосудов, хотя кровоток и увеличивается в 1,5-2 раза. Раздражение же центральной симпатической нервной системы может увеличить сопротивление кровотоку в резистивных сосудах до 80% и на 35% снизить объемный кровоток. Тонус сосудов может быть слабо выраженным, повышенным и очень высоким. Последний именуется спазмом артерий. Он может быть по продолжительности, по нашим данным, от 2-3 сердечных сокращений до 5 минут. Степень спазма определяет в какой-то мере продолжительность его существования. Он может быть окклюзирующим, но тогда непродолжительным.
Функциональное состояние мышечных артерий зависит от питания их стенок через vasa vasorum. И хотя этот вопрос до сих пор является не изученным, определенные суждения о механизме осуществления этого питания можно выявить.
Прохождение крови по vasa vasorum в media артерии при открытом сфинктере в артериальной петле капилляра, контролируемом симпатическими нервами, осуществляется, вероятно, по механизму "мышечного насоса": расслабление артерии дает возможность притока крови по vasa vasorum в media (Шабанов А.Н., Котельников В.П., 1983). Сокращение мышечного сосуда приводит к выдавливанию крови из капилляров и посткапилляров мышечной стенки сосуда (Залманов А.С., 1991).
Логично предположить, что, чем больше расслабляется артерия, тем свободнее приток крови в мышечную стенку артерии. Повышение базового тонуса артерии препятствует этому притоку крови. Спазм артерии, кроме того, ликвидирует волну обратного тока крови в просвете сосуда и тем сокращает вторую фазу мышечного насоса за время одного сердечного цикла, на долю которого можетприходится до 25% объёмного кровотока. Наступает гипоксия мышечной стенки сосуда, интимы с эндотелием с последующими дегенеративно-деструктивными изменениями. Степень и продолжительность гипоксического состояния мышечной стенки артерии определяют выраженность дистрофических изменений.
Таким образом, спазмы артериокапиллярной системы вызывают дистрофические изменения в стенках сосудов (Бондарчук А.В., 1969). Ещё В.А.Оппель (1911) утверждал, что развившийся спазм мельчайших артерий приводит к расстройству питания артериальных стенок (артериол) с последующим их тромбозом. Таковы анатомо-функциональные взаимоотношения симпатической нервной системы и сосудистой.
Артериальная ишемия конечности возникает либо остро, либо развивается медленно и по клиническому течению может быть компенсированной, либо декомпенсированной. В последние годы получило распространение понятие критической артериальной ишемии конечности. Эта характеристика степени артериальной ишемии, пограничной с декомпенсированной, скорее отражает потребность в применении срочных лечебных мер для сохранения целостности конечности, которую трудно сохранить в декомпенсированной стадии артериальной ишемии.
Основной причиной артериальной ишемии конечности является снижение суммарного объемного артериального кровотока через магистральные, шунтирующие и коллатеральные артерии в сегменты конечности, недостаточного наполнения капиллярной сети. Снижение объемного артериального кровотока через поперечное сечение сегмента конечности возникает в случаях спазма артерий, облитерирующего заболевания их, внешнего или внутреннего сдавления артерий, травмы с нарушением целостности стенок, тромбоза.
Травмы артерий и сдавление их не является предметом исследования в данной работе.
Спазмы артерий сегмента конечности имеют причины местные и центральные.
Местные причины, вызывающие сегментарный спазм артерий, - это электрическая, химическая, термическая или механическая травма, сопровождающаяся ушибом или механическим повреждением артерии, переломом костей, разрывом или отрывом связок, сухожилий, мышц, их сдавлением, возникновением ран (Обыдёнов С.А., Фраучи И.В., 2000), неправильно сросшиеся переломы, разрыв связок и сухожильных растяжений, посттравматические деформации сегментов конечностей с нарушением статических и динамических нагрузок, изменяющих индивидуальный стереотип.
Спазмы артерий конечностей центрального происхождения возникают при функциональном и органическом заболевании позвоночника, которые могут сочетаться.
Функциональные заболевания проявляются функциональным блоком ПДС - это обратимое ограничение подвижности в ПДС (рис.2).
Д
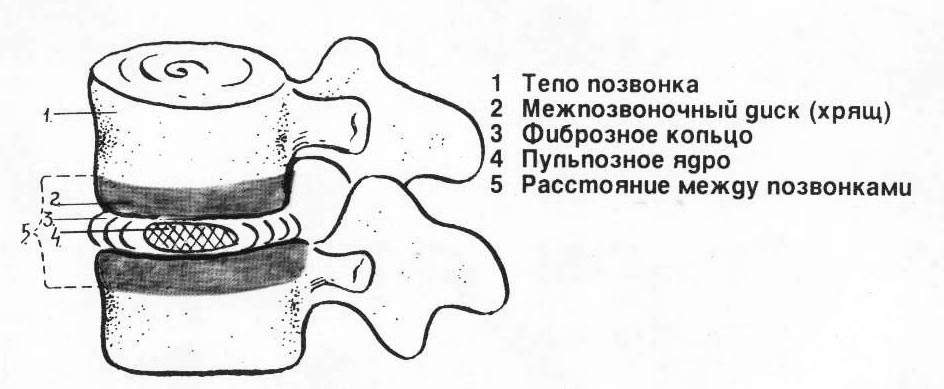 вигательный
сегмент позвоночного столба (ПДС)
вигательный
сегмент позвоночного столба (ПДС)
Причинами функционального блока могут быть острый или хронический нервно-мышечный стресс (Ханна Т., 1995), неадекватная двигательному стереотипу статическая нагрузка, сильная однократная или слабая длительная, неадекватная динамическая нагрузка, пассивное перерастяжение, длительная обездвиженность, смещение или ущемление менискоидов дугоотросчатых суставов, подвывих их (Emminger E., 1967).
Внешние факторы, действующие на человека, вызывают реакцию адаптации (стресс). Стресс бывает положительным и отрицательным. Положительный вызывает реакцию "готовности к действиям" (рефлекс "зеленого цвета"). Мускулатура задней поверхности тела сокращается, а антагонисты передней поверхности тела расслабляются. Возникает характерная осанка. Тревога и беспокойство создают отрицательный стресс, который вызывает реакцию "ухода" (рефлекс "красного цвета"), в основе которого - уход от опасности. Сокращаются передние мышцы туловища, задняя мускулатура расслабляется. Возникает другая характерная осанка. При возникновении у человека положительных и отрицательных стрессов происходит суммирование двух рефлексов. Один из них может преобладать, что приводит к возникновению определенных вариантов осанки, свидетельствующих о различной силе мышечно-компрессионных воздействий на позвоночный столб спереди и сзади в различных его отделах. Это проявляется сглаживанием физиологи-
ческих лордозов
и кифозов, возникновением сегментарных
лордозов и кифозов, а также сколиозов,
С- или S-о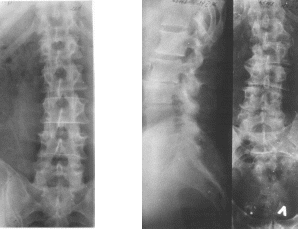 бразных
(рис.3).
бразных
(рис.3).
а) б)
а) Рентгенограмма С-образного искривления позвоночника. б) Рентгенограмма S-образного искривления позвоночника
У человека два вида мышц: произвольно сокращающиеся (не осаночные) и непроизвольно сокращающиеся (осаночные). Они различаются и качественно, и по назначению. Произвольно сокращающиеся мышцы приводятся в действие нашими волевыми усилиями и быстро утомляются. Непроизвольно сокращающиеся мышцы включаются в работу без наших волевых усилий и могут находиться в рабочем состоянии длительное время (Crase R., 1996). Человек, способный в полной мере управлять своими мышцами, может привести их к нулевому тонусу. У человека, потерявшего способность управлять мышцами, тонус их повышен до 20 - 40%. Мышцы с высоким тонусом, т. е. в состоянии хронического напряжения, всегда болезненны, твердые, в них всегда ощущается усталость. В таких мышцах постоянно расходуется гликоген и накапливается молочная кислота. Повышение содержания молочной кислоты на 10% вызывает чувство усталости, на 40% - постоянную болезненность в мышцах (Ханна Т., 1995). Возникает хроническая боль в тонически сокращенных мышцах, миофиксация ПДС с блокированием его. Выраженные постоянные сокращения мышц являются причиной их гипертрофии на первом этапе существования хронического нервно-мышечного стресса. При этом образуется локальная гипертермия. Длительное сокращение мышц нарушает микроциркуляцию в них, постепенно формируется хроническая мышечная ишемия, которая вызывает деструктивно-дегенеративные изменения мышечных волокон и нервно-мышечных веретен, отвечающих за удлинение мышц, их частичное перерождение в соединительную ткань. Образуются рубцовые тяжи и болезненные узлы, уменьшающие потенциальные сократимость и растяжимость мышц. Локальная гипертермия сменяется гипотермией, что имеет определенное диагностическое значение (Хабиров Р.А., Салихов И.Г., 1995). Региональное нарушение тонусо-силовых взаимоотношений мышц позвоночника, региональный дисбаланс мышц, функциональный блок ПДС создают неоптимальный двигательный стереотип различной степени выраженности. Возникают ненормальные нагрузки на различные анатомо-функциональные элементы позвоночника, сопровождающиеся болью, образуется функциональный блок ПДС.
Органические заболевания позвоночника: остеохондроз, спондилез, спондилолистез, спондилоартроз, протрузия, грыжа дисков - сопровождаются возникновением очагов патологического болевого раздражения рецепторов синувертебрального нерва, нерва Люшка, состоящего из симпатических и соматических волокон. Болевое раздражение нерва Люшка вызывает спазм резистивных сосудов ПДС и артериальную ишемию соответствующего ПДС узла симпатического ствола. Надпороговое раздражение нерва сопровождается локальным болевым синдромом. При его длительном существовании в результате приспособительно-компенсаторных способностей нервной системы болевой порог повышается. Болевой синдром проходит ( Tepe Y.J..,1956; Schon D.,1963) но сохраняется спазм резистивных сосудов, артериол ПДС и соответствующих симпатических узлов. Последние вызывают на периферии в соответствующих им зонах по дерматому сегментарный спазм артерий согласно иннервации дерматомов по схеме Koegan (рис.4).
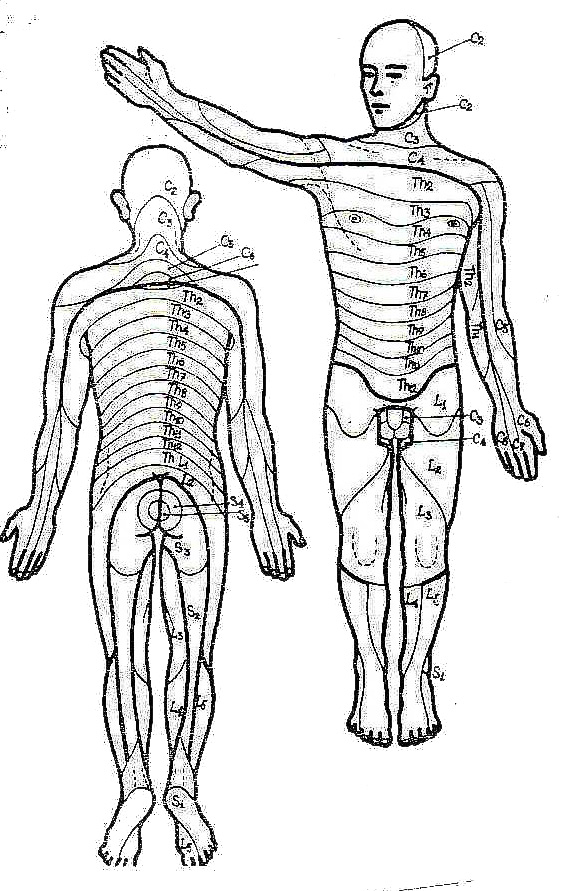
Схема сегментарной иннервации тела (дерматомы) по Кигану
Местно этот спазм создаёт условия для дегенеративно-деструктивных изменений в мышцах, связках, суставах, в межпозвонковых дисках, а затем и в костной ткани. Дифференцированные ткани постепенно замещаются соединительной тканью. Развивается то или иное органическое заболевание позвоночника (остеохондроз, деформирующий спондилоартроз, спондилёз и др.). Известно, что при синдроме Рейно почти всегда выявляется шейный остеохондроз. Морфологи выявили существование артериальной ишемии паравертебральных симпатических ганглиев при органических заболеваниях позвоночника, чаще всего остеохондрозе.
А.Н.Шабанов, В.П.Котельников (1983) при изучении удаленных ганглиев симпатического ствола во время операции по поводу артериальных ишемий конечностей при облитерирующем эндартериите нашли изменения в каждом узле в виде разрастания соединительной ткани и склеротических изменений сосудов и в клетках самого узла, выражавшихся в деструктивных и атрофических процессах в некоторых нервных клетках и волокнах. Они утверждают, что изменения в симпатических узлах зависят от первичных изменений в сосудах ганглиев. Это характерно для состояния хронической ишемии, гипоксии, нарушения питания. Такие изменения в ганглиях характерны для облитерирующего атеросклероза, болезни Рейно, трофических язв конечностей.
Вертебрологи и невропатологи, изучающие остеохондроз, установили существование вегето-сосудистого синдрома, корешково-сосудистого синдрома, сопровождающихся спазмом периферических артерий (Антонов И.П., 1984, 1985; Жулев М., Лобзин В.С., Бадзгарадзе Ю.Д., 1992).
Блокирование функций позвоночно-двигательных сегментов возникает при остром и хроническом нервно-мышечном стрессе, когда различные отрицательные психические воздействия, сильные однократные или слабые и длительные, вызывают через центральную нервную систему повышение тонуса мышц до 40% от исходного. При таком тонусе теряется волевая способность управления мышцами. Скованность мышц с нарушением осанки, ограничение движений нарушают нервно-мышечный стереотип движений, создают несбалансированные асимметричные нагрузки на различные отделы позвоночника, блокируя его функции, что может вызвать ущемление менискоидов, смещение позвонков. Это обратимые изменения. Однако длительные асимметричные нагрузки на позвоночник приводят к дегенеративным, патологоанатомическим изменениям в межпозвонковых дисках и связочно-суставном аппарате (Веселовский В.П., 1984, 1991). Дегенеративно-дистрофические изменения позвоночника занимают ведущее место в происхождении вертеброгенных синдромов (Calabro J.I. et al., 1980). Возникают постоянные патологические очаги боли, восприятие которой со временем меняется в связи с адаптацией нервной системы, снижающей надпороговую боль до уровня подпороговой по восприятию (Антонов И.П., Шанько Г.Г., 1981). Исследованиями А.Ю.Ратнера (1990) доказано, что патология шейного отдела позвоночника повинна в развитии сосудистых симптомов как у взрослых, так и у детей. Однако очевидная взаимосвязь между патологическими изменениями позвоночника и сосудистой патологией в ангионеврологической литературе просто игнорируется (Лобзин С.В., 2001).
Итак, функциональные и органические заболевания позвоночника приводят к ангиоспастическим артериальным ишемиям соответствующих конечностей. Реализация происходит через ишемию паравертебральных симпатических ганглиев, гипертонусом соответствующих ганглиям по дерматому сегментов артерий конечностей [очень редко вазодилятацией, - у 2% больных, по Я.Ю.Попелянскому (1983)] и артериальной ишемией сегментов конечностей. Форма и вид гипертонуса периферических артерий зависит от функционального состояния ганглиев.
Клинический опыт по изучению хронической артериальной ишемии конечностей показывает, что начало развития хронической артериальной ишемии начинается с функциональных нарушений артериального кровоснабжения, которые затем превращаются в морфологически обозначенные заболевания артерий. Спазм артерий, с которого начинаются облитерирующие заболевания, особенно облитерирующий эндартериит, при дальнейшем развитии наслаивается на органические изменения магистральных и формирующих коллатерали артерий (Оппель В.А., 1911).
Для объяснения патогенеза облитерирующего эндартериита существуют несколько теорий: кортикоорганная (Вишневский А.В. с соавт.), воспалительная (Фридлендер, 1876; Введенский А.А., 1892), эндокринная (Оппель В.А., 1928, Лериш Р., 1961; Чепелев А.Д., 1951; Гутцайт-Лосева Н.И. с соавт., 1952), нейрогуморальная (Котельников В.П., 1961; Шабанов А.Н., 1970; Шабанов А.Н., Комов Д.В., 1971; Гомзяков О.А., с соавт., 1973). Не останавливаясь на описании каждой из перечисленных теорий, следует отметить, что наиболее близка к истине нейрогуморальная теория. Она основательно объясняет патофизиологию развития облитерирующего эндартериита, однако в этой теории нет объяснения пусковых механизмов для развития патофизиологического процесса. Наряду с этим, исследованиями Д.В.Комова (1971), установлено, что в I стадии облитерирующего эндартериита и болезни Рейно имеется преходящий сосудистый спазм и выраженные морфологические изменения мелких сосудов кожи и мышц носят характер начального склероза. Однако вывод из этих данных сделан (Шабанов А.Н., Котельников В.П., 1983) странный: морфологические изменения мелких сосудов являются причиной спазма сосудов. Хотя более логичным и естественным был бы вывод, к которому пришли В.А.Оппель и Р.Лериш и которого придерживаются многие отечественные авторы, - длительный спазм сосудов и сопровождающие их vasa vasorum ведут к хронической ишемии сосудистой стенки, что приводит к развитию морфологических изменений, гиперплазии интимы, субэндотелиальной ткани, фиброзу адвентиции, склерозу мышечной оболочки (Вишневский А.А., Краковский Н.И., Золотаревский В.Я., 1972; Ситенко В.М., 1973; Кузин М.И., 1986; Залманов А.С., 1991). Установлено, что наибольшие изменения при гипертонусе сосудов, доходящем до спазма, возникают в артериолах. Мышечный слой их утолщается в области ветвления их на прекапилляры, диаметр капилляров уменьшается до 4-6 мкм (в норме диаметр сосудов микроциркуляторного русла от 2 до 200 мкм: капилляры - 2-20 мкм, прекапилляры - 10-15 мкм, метаартериолы с одним мышечным слоем - 15-25 мкм, артериолы с несколькими мышечными слоями - 30-100 мкм). Редукция капиллярных петель приводит к деструкции их. В местах распада сосудов образуются сливные геморрагии. В венозном звене посткапилляры и венулы расширены до 50 мкм, извиты, местами имеется венозный застой. Стенки вен деформируются, клапаны атоничны. При более тяжелой III ст. ишемии спазм гладкомышечных клеток в стенках артериол закрывает их просвет, кровоток проходит по артериовенозным анастомозам. Происходит распад артериол и венул. Образуются обширные геморрагии. Расширяются лимфатические сосуды. Нарушается кровоснабжение вен, они теряют свой тонус. Наступает дилятация сосудов венозного звена (рис.5) с застоем крови и повышением венозного давления (Allen E.F. et al.,
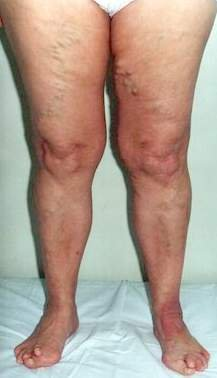
Больная С.В.М., 55 лет. Хроническая артериальная ишемия нижних конечностей, вертеброгенный статический ангиоспазм артерий в сосудистых сегментах L2 по дерматому (по Кигану), расширение подкожных вен в этих сегментах, гемангиома тела L2
1962; Неркунас П.И., 1966; Димитров Н.Т., Чайковский А.Б., 1984). Уменьшается артериовенозная разница напряжения кислорода, а ткани страдают от гипоксии (Котельников В.П., 1970). Развиваются соответствующие дистрофические изменения тканей, в первую очередь капилляров. Наступает дегенерация большой их части и исчезновение. Резко уменьшается объемное капиллярное русло. При этом магистральный кровоток не уменьшается. В сыворотке крови больных эндартериитом появляются антисосудистые и антиэритроцитарные антитела. Уровень титра их находится в прямой зависимости от стадии патологического процесса (Шарлуян П.М., Поляк А.И., Дюжиков А.А., 1976). Со временем склеротические изменения в артериолах распространяются проксимально до магистральных артерий. При этом наступает не только диффузное сужение магистральной артерии, но часто - сегментарная окклюзия магистрали. Тогда начинает уменьшаться магистральный кровоток. Итак, при облитерирующем эндартериите склероз начинается с артериол с исчезновением большой части капиллярного русла и распространяется затем на магистральные артерии.
До сих пор развитие атеросклероза связывали с количеством холестерина в крови согласно инфильтрационно-комбинационной теории атеросклероза (Аничков Н.Н., 1965). Однако клиницистам известно, что у многих больных тяжелым атеросклерозом нет гиперхолестеринемии. Встречаются люди с гиперхолестеринемией, но не страдающие атеросклерозом. В чем же причина таких неувязок?
Липиды, состоящие из холестерина, фосфолипидов, триглицеридов, в соединении с транспортными белками образуют липопротеиды. Они по плотности классифицируются на липопротеиды высокой плотности (ЛВП или α-липопротеиды), липопротеиды низкой плотности (ЛНП или δ-липо- протеиды), липопротеиды очень низкой плотности (ЛОНП или пре-δ-липо- протеиды) и хиломикроны. Поврежденный эндотелий сосудов восстанав- ливается с использованием холестерина и фосфолипидов, которые внедря- ются в интиму артерии в местах повреждения эндотелия из кровяного русла. Установлена высокая зависимость развития атеросклероза от содержания в плазме крови ЛНП и ЛОНП, называемых атерогенными (Климов А.Н., Нагорнев В.А., 1984). Они соединяются с рецепторами поверхностных мембран клеток и путем эндоцитоза проникают в эндотелий (Brown M.S. et Goldstein, 1974). Концентрация этих рецепторов эндотелия vasa vasorum плотнее, чем у эндотелия самого сосуда. В нормальных условиях потребность в строительном холестерине удовлетворяется за счет ЛВП. Но в условиях недостаточного обеспечения кровью стенки артерий по vasa vasоrum (гипертонус, спазм, сопровождающийся стазом, повышенной проницаемостью) возникает тканевая гипоксия (Буркова Н.Ф., 1984), провоцируется захват ЛНП и ЛОНП поврежденным эндотелием и практически неповрежденным эндотелием со стороны кровотока (Бисярин В.П. с соавт., 1986). Количество холестерина в крови стабильно. Меняется количество транспортных белков. Кроме того, в крови человека образуются аутоиммунные комплексы в результате превращения липопротеидов в аутоантигены (авт. свид. № 249 - 1981 г.). Изменение количества липидных фракций, наличие атерогенно модифицированных липопротеидов и нарушение доставки липидов нормальным путем - наиболее вероятные причины развития атеросклероза артерий (Климов А.Н., Нагорнев В.А., 1989; Жолондз М.Я., 1996).
Атеросклероз артерий является одной из наиболее частых причин артериальной ишемии конечностей. Морфологически он проявляется образованием, главным образом в интиме, плоских желтоватых (липоидных) бляшек, выступающих в просвет артерии. В толще бляшек находятся кашицеобразные липоидные массы. Размеры бляшек варьируют от долей миллиметра до нескольких сантиметров в диаметре, и они могут выступать в просвет сосуда до почти полного его закрытия. Некоторые из них в центре могут изъязвляться, на изъязвлении формируется тромб, который частично или полностью перекрывает просвет артерии. Создаются условия для уменьшения объемного кровотока через артерию. Атеросклеротические бляшки образуются обычно в магистральных артериях, артериях первого, второго и третьего порядка (Вишневский А.А., Краковский Н.И., Золотаревский В.Я., 1972). Наступает сначала уменьшение магистрального кровотока, отчего возникает гипоксия тканей и, в первую очередь, капилляров, их деструктивные изменения и исчезновение большой их части. Так развивается артериальная ишемия конечностей при атеросклерозе артерий, и начинается она с магистральных артерий.
Остается без ответа вопрос. Почему облитерирующий эндартериит развивается преимущественно у молодых людей, а облитерирующий атеросклероз - у пожилых? В научной литературе ответа на этот вопрос найти не удалось. Однако при изучении опубликованных данных вытекает логическое положение: при развитии облитерирующего эндартериита в I его стадии всегда имеется преходящий (перемежающийся) ангиоспазм (Шабанов А.Н., Котельников В.П., 1983). Кроме того, при облитерирующем эндартериите развивается сенсибилизация к собственным сосудистым антигенам, возникает аутоиммунная агрессия к собственным сосудам (Шарлуян с соавт., 1976; Петровский Б.В., 1980; Чопяк В.В., 1987). Развитие облитерирующего атеросклероза артерий конечностей начинается с ангиоспастической фазы (Бондарчук А.В., 1969). Видимо, характер ангиоспазма определяет вид развивающегося облитерирующего заболевания артерий, а аллергический аутоиммунный процесс определяет развитие эндартериита.
Сахарный диабет сопровождается развитием диабетической микроангиопатии, которая в соответствии с клиническим проявлением может иметь преимущественное поражение сосудов сердца, мозга, периферических артерий, чаще всего нижних конечностей. Механизмы развития микроангиопатии у диабетиков не выяснены. Однако выявлены некоторые факты, имеющие отношение к патогенезу микроангиопатии. Гипергликемия вызывает неферментативное гликозилирование белков с образованием промежуточного соединения, называемого продуктом Амадори. Последний медленно преобразуется в необратимые сложные соединения, обнаруживаемые в соединительной ткани сосудов, фосфолипидном компоненте ЛПНП, в составе утолщенных базальных мембран. Образуются свободные радикалы с мощной окислительной активностью. Повышается проницаемость, снижается эластичность сосудов. Изменяются функция энзимов и обмен липопротеидов. Гликозилированные ЛПНП легко окисляются и имеют большое сродство к макрофагам. Образуются "пенистые клетки", являющиеся основным элементом атерогенеза. Повышается активность тромбоцитов, возникает гиперфибринемия, увеличиваются факторы V, VII, VIII, снижается фибринолитическая активность крови. Нарушается баланс между вазодилятаторами и вазоконстрикторами. Возникают микротромбы, нарушая микроциркуляцию, вызывая окклюзии артерий. Клинически это проявляется перемежающейся хромотой и ишемической стопой. При резком нарушении кровотока возникает гангрена стопы и голени, при меньшем нарушении кровотока - язва, деструкция костей, мышц (Ромашевский Б.В., 1999).
Итак, на основании изучения научной литературы выяснили, что артериальные ишемии конечностей бывают ангиоспастические и при облитерирующих заболеваниях артерий.
Ангиоспастические ишемии конечностей могут быть центрального и периферического (местного) генеза. Центрального генеза ангиоспастические ишемии конечностей возникают при функциональных и органических заболеваниях позвоночника. Местного генеза ангиоспастические хронические артериальные ишемии бывают при местных патологических процессах, состояниях и травмах.
Артериальные ишемии конечностей при облитерирующих заболеваниях артерий - это ишемии при облитерирующем эндартериите, при облитерирующем атеросклерозе, при диабетической ангиопатии. Артериальные ишемии при других заболеваниях артерий не рассматриваются, поскольку они встречаются редко.
В литературе не удалось найти данных о степени выраженности ангиоспазма и облитерирующего заболевания артерий при ХАИК, их взаимоотношении и соотношении, способах их диагностирования. Знание этих данных патогенеза необходимо дляразработки принципоы лечения.
