
- •Глава 1. Характеристика района
- •1.1 Физико-географический очерк
- •1.2. Геологическое строение и гидрогеологические условия
- •1.3. Почвенный покров
- •1.4 Растительный и животный мир
- •1.5 Экологическая ситуация
- •Глава 2. Методики полевых исследований, отбора и обработки проб
- •2.1. Выбор сред опробования и его обоснование
- •2.2 Методика отбора и обработки почв
- •2.3. Опробование вод и донных отложений водоемов
- •Глава 3. Методы лабораторных исследований
- •3.1. Потенциометрия
- •Перманганатный метод
- •3.3 Титриметрическое определение хлора
- •3.4. Определение тяжелых металлов в пробах воды методом ивам
- •3.5 Карбонатная система
- •Расчет концентраций карбонат- и бикарбонат-ионов по измеренным величинам щелочности и рН Определение общей щелочности
- •Расчет концентраций карбонат- и бикарбонат-ионов по измеренным величинам щелочности и рН
- •2. Оценка степени насыщения вод по карбонату кальция
- •Определение концентрации кальция
- •Глава 4. Результаты, их обработка и обсуждение
- •4.1 Состояние почв в зоне влияния мкад
- •4.2 Состояние водных объектов
- •Заключение
- •Список литературы
3.5 Карбонатная система
Неорганические соединения углерода
находятся в природных водах в виде
угольной кислоты и ее производных. В
отличие от сильных соляной и серной
кислот, которые полностью диссоциируют
в растворе, угольная кислота является
слабой. Поэтому она диссоциирует не
полностью, и в растворе одновременно
присутствуют ионы
![]() ,
,
![]() и
и
![]()
Чтобы определить концентрации ионов
и
![]() в растворе, проводят измерения величин
рН и общей щелочности (Alk),
которая представляет собой сумму анионов
слабых кислот – угольной H2CO3,
фосфорной H3PO4,
кремниевой H2SiO3,
сероводородной H2S,
борной H3BO3,
уксусной CH3COOH
и др. По сравнению с угольной кислотой,
вклад анионов других слабых кислот
пренебрежимо мал, и отличия общей
щелочности от карбонатной, как правило,
незначительны. Поэтому с достаточным
приближением можно принять
в растворе, проводят измерения величин
рН и общей щелочности (Alk),
которая представляет собой сумму анионов
слабых кислот – угольной H2CO3,
фосфорной H3PO4,
кремниевой H2SiO3,
сероводородной H2S,
борной H3BO3,
уксусной CH3COOH
и др. По сравнению с угольной кислотой,
вклад анионов других слабых кислот
пренебрежимо мал, и отличия общей
щелочности от карбонатной, как правило,
незначительны. Поэтому с достаточным
приближением можно принять
![]() (1)
(1)
Расчет концентраций карбонат- и бикарбонат-ионов по измеренным величинам щелочности и рН Определение общей щелочности
Принцип метода. Определение щелочности проводится объемным ацидиметрическим методом, основанном на взаимодействии бикарбонат- и карбонат-ионов с сильной соляной кислотой. При титровании диссоциированные формы угольной кислоты ( и ) переходят в недиссоциированную форму , которая распадается на CO2 и H2O с выделением CO2 в атмосферу.
При рН 8.1 в растворе присутствуют в достаточном количестве ионы . Их концентрацию можно определить титрованием с индикатором фенолфталеином (по переходу окраски из красной в бесцветную) перед определением .
В диапазоне рН от 4.5 до 8.0 (при рН < 4.5 все формы переходят в ) проводят только определение ионов со смешанным индикатором (метилрот + метиленовый голубой), поскольку количество ионов в этом случае пренебрежимо мало.
Ход определения. К 50 мл исследуемого раствора добавляют 3–4 капли смешанного индикатора и титруют 0.05 N HCl до слабо розовой окраски. Выделяющийся при этом СО2 удаляется продуванием воздухом, пропускаемым через аскаритовую трубку.
Вычисление результатов анализа:
![]() (2)
(2)
где
![]() – количество HCl,
израсходованной на титрование пробы,
мл;
– количество HCl,
израсходованной на титрование пробы,
мл;
![]() – нормальность раствора HCl
(0.05 N);
– нормальность раствора HCl
(0.05 N);
![]() – объем пробы, мл.
– объем пробы, мл.
Расчет концентраций карбонат- и бикарбонат-ионов по измеренным величинам щелочности и рН
Основные теоретические положения. Слабая угольная кислота диссоциирует в растворе по двум ступеням:
![]() ,
(3)
,
(3)
![]() (4)
(4)
Константы равновесия реакций (2) и (3) представляют собой первую и вторую константы диссоциации угольной кислоты:
 ,
(5)
,
(5)
 (6)
(6)
где
![]() и
и
![]() – соответственно термодинамическая и
концентрационная константы равновесия;
а, [ ] и *
– активности, концентрации и общие
коэффициенты активности ионов.
– соответственно термодинамическая и
концентрационная константы равновесия;
а, [ ] и *
– активности, концентрации и общие
коэффициенты активности ионов.
В атмосферном воздухе содержится
углекислый газ, парциальное давление
(![]() )
которого равно 3.8
10–4 атм. При равновесии воды с
атмосферой концентрация недиссоциированной
угольной кислоты (
)
которого равно 3.8
10–4 атм. При равновесии воды с
атмосферой концентрация недиссоциированной
угольной кислоты (![]() )
связана с
через константу Генри (
)
связана с
через константу Генри (![]() ):
):
 .
(7)
.
(7)
Перемножив
![]()
![]() и
,
получим связь
с активностью ионов
и
,
получим связь
с активностью ионов
![]() при условии равновесия воды с
атмосферой:
при условии равновесия воды с
атмосферой:
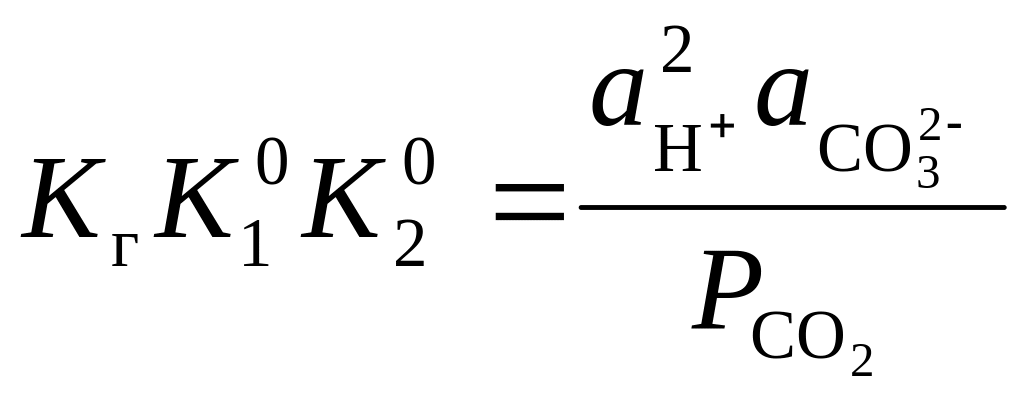 .
(8)
.
(8)
Однако поверхностные воды далеко не всегда равновесны с углекислой атмосферы. Главная причина неравновесности – продукционно-деструкционные процессы, которые приводят либо к подщелачиванию, либо к подкислению среды, постоянно изменяя соотношение между компонентами карбонатной системы.
Расчет концентрационной константы
равновесия второй ступени диссоциации
угольной кислоты (![]() ).
В качестве основного параметра в расчетах
будем использовать константу
).
В качестве основного параметра в расчетах
будем использовать константу
 (9)
(9)
Значение
![]() зависит от температуры раствора и
вычисляется с помощью эмпирического
уравнения связи [Робинсон, Стокс, 1963]:
зависит от температуры раствора и
вычисляется с помощью эмпирического
уравнения связи [Робинсон, Стокс, 1963]:
![]() (10)
(10)
где T
– температура в K
(T, K
= 273.16 + T, С).
При температуре 25 С
получим, что
![]() ,
откуда
,
откуда
![]()
![]() .
.
По определению общий коэффициент
активности ионов i
(![]() )
равен произведению коэффициента
активности свободных ионов (
)
равен произведению коэффициента
активности свободных ионов (![]() )
и их доли от общего содержания компонента
i в растворе (
)
и их доли от общего содержания компонента
i в растворе (![]() )
[Робинсон, Стокс, 1963]:
)
[Робинсон, Стокс, 1963]:
![]() (11)
(11)
Коэффициенты активности свободных ионов в природных водах различной минерализации удовлетворительно описываются в рамках теории Дебая-Хюккеля третьего приближения, в частности, с помощью полуэмпирического уравнения Девиса:
![]() (12)
(12)
где
![]() – заряд иона i;
A
– постоянная величина, равная 0.5115 при
25 С;
I
– ионная сила раствора, которую для вод
исследуемого района можно принять
равной 0.005.
– заряд иона i;
A
– постоянная величина, равная 0.5115 при
25 С;
I
– ионная сила раствора, которую для вод
исследуемого района можно принять
равной 0.005.
В соответствии с результатами исследований,
проведенных на Можайском водохранилище
[Савенко, 2000], примем, что ионные пары
с катионами основного солевого состава
вносят пренебрежимо малый вклад в общую
концентрацию растворенных бикарбонатов
(< 1%) и
![]() =
0.93.
=
0.93.
Вкладом ионных пар
![]() и
и
![]() также можно пренебречь, однако с Ca2+
и Mg2+ связана примерно
половина ионов
также можно пренебречь, однако с Ca2+
и Mg2+ связана примерно
половина ионов
![]() .
Поэтому для расчета общего коэффициента
активности карбонат-ионов будем
использовать эмпирическое уравнение
связи, полученное с учетом температурных
зависимостей констант устойчивости
ионных пар
.
Поэтому для расчета общего коэффициента
активности карбонат-ионов будем
использовать эмпирическое уравнение
связи, полученное с учетом температурных
зависимостей констант устойчивости
ионных пар
![]() и
и
![]() ,
приведенных в работе [Робинсон, Стокс,
1963]:
,
приведенных в работе [Робинсон, Стокс,
1963]:
![]() =
0.40. (13)
=
0.40. (13)
Теперь, после того как мы рассчитали
величины
![]()
![]() и
и
![]() ,
получим искомое значение концентрационной
константы равновесия
,
получим искомое значение концентрационной
константы равновесия
![]() :
:
 = 1.08
10–10.
(14)
= 1.08
10–10.
(14)
Расчет концентраций карбонат- и бикарбонат-ионов. Из уравнения (6) следует, что
 (15)
(15)
Подставив
выражение для
![]() в уравнение
в уравнение
![]() (16)
(16)
получим:
 (17)
(17)
Отсюда по измеренным величинам щелочности
и рН (![]() )
и расчетному значению
)
и расчетному значению
![]() мы можем определить концентрации ионов
и
мы можем определить концентрации ионов
и
![]() :
:
 (18)
(18)
![]() (19)
(19)
Расчет
концентрации ионов
![]() можно проверить по уравнению (15).
можно проверить по уравнению (15).
Результаты определений величин щелочности и рН в пробах и расчетные значения концентраций ионов и приведены в табл. 3.5.1 и 3.5.2
Таблица 3.5.1 Определение величины щелочности и концентрации ионов кальция объемным ацидиметрическим и трилонометрическим методами.
|
||||||||||||||||||||||||||||
ф – фильтрованная
нас – насыщенная СaCO3
Таблица 3.5.2 Расчет концентраций карбонат- и бикарбонат-ионов по измеренным величинам щелочности и pH
№ пробы |
Alk, мг-экв/л |
рН |
ан |
COз, мM |
HCOз, мM |
1ф |
2,20 |
7,86 |
1,38E-08 |
0,01695 |
2,166 |
1 ф-нас |
2,10 |
7,97 |
1,07E-08 |
0,02075 |
2,059 |
32 ф |
2,00 |
7,82 |
1,51E-08 |
0,01407 |
1,972 |
32 ф-нас |
1,90 |
8,06 |
8,71E-09 |
0,02299 |
1,854 |
ф – фильтрованная
нас – насыщенная СaCO3
