
Лекция №1
ТЕМА: «ВВЕДЕНИЕ В ОРГАНИЧЕСКУЮ ХИМИЮ».
Органическая химия – это наука, изучающая состав, строение, свойства органических веществ, а также их взаимное превращение друг в друга.
Органические вещества – это соединения углерода.
Исторический очерк развития органической химии как науки.
С древних времен люди знали масла, жиры, уксус, сахар и т.д. Это были смеси, чистые органические вещества стали получать позже.
В VIII веке, в 1773 году, уже была выделена кристаллическая мочевина.
В 1828 году немецкий химик Велер синтезировал органическое вещество мочевину из неорганического вещества цианата амония. С этого момента начинается бурное развитие органического синтеза.
Периоды развития органической химии.
Ятрохимия –(от греч. «ятрос» - врач). Основателем этого периода считается Парацельс. Его Герцен назвал «Первым профессором от сотворения мира». Это период длился VI – VII века.
Эмпирический (VII – VIII века) – охватывает промежуток от первоначального знакомства с органическими веществами до возникновения органической химии как науки.
Аналитический (кон. VIII сер. XIX века) – связан с появлением методов установления состава органических веществ.
Структурный (втор. пол.XIX – нач. XX века) – связан с открытием теории строения органических веществ А.М. Бутлерова.
Современный.
Теория строения органических
веществ А.М. Бутлерова.
Эта теория была разработана А.М. Бутлеровым в 1861 году.
Атомы и молекулы соединены друг с другом химическими связями в соответствии с их валентностью.
Атомы в молекулах органических веществ соединены между собой в определенной последовательности, что обуславливает химическое строение молекулы.
Свойства соединений зависят не только от числа и природы входящих в их состав атомов, но и от их химического строения.
В молекулах существует взаимное влияние атомов как связанных, так и непосредственно друг с другом не связанных.
Химическое строение вещества можно определить в результате изучения его химических превращений и наоборот: по строению вещества можно охарактеризовать его свойства.
Открытие этой теории послужило толчком к бурному развитию органической химии.
Классификация органических соединений.
При классификации органических соединений используют два критерия:
I. Строение углеродного скелета.
По строению углеродного скелета органические вещества делятся на:
Ациклические (алифатические) – вещества не циклического строения.
Карбоциклические (от греч. «карбонеум» - углерод) – вещества, в которых углеродная цепь замкнута в цикл, состоящий только из атомов углерода.
Гетероциклические (от греч. «гетерос» - другой, разный) – соединения, в которых углеродная цепь замкнута в цикл, состоящий не только из атомов углерода, а из атомов кислорода, азота, серы и т.д.
-

S
О
Фуран Тиофен
По наличию молекул функциональных групп
органические вещества делят на классы.
Функциональная группа – атом или группа атомов не углеводородного характера, которые определяют принадлежность соединений к определенному классу.
Функциональная группа |
Название класса |
Общая формула класса |
-F, –Cl, –Br, –I галогены |
галогенопроизводные |
R - |
- OH (гидроксильная) |
спирты, фенолы |
R – OH |
- OR (алкоксильная) |
простые эфиры |
R – OR |
- SH (тиольная) |
тиолы (меркаптаны) |
R – SH |
NH
|
амины |
R – NH2 R – NH – R1 R – N – R1
R2 |
- NO2 |
нитросоединения |
R – NO2
|
К а) O
H
б) С (кетонная) ║ О |
альдегиды
кетоны |
O
R – C H
R1 — C — R2 ║ O |
– C (карбоксильная) ОH |
карбоновые кислоты |
R – COOH |
O ║ — S — OH ║ O (сульфогруппа) |
сульфокислоты |
R – SO3H |
Причины выделения органической химии в отдельную науку:
Многочисленность органических веществ (более 6 миллионов);
Большое практическое значение органических соединений;
Большое своеобразие:
а) почти все горят
б) при незначительных воздействиях изменяются, разлагаются.
в) в молекулах органических соединений углерод может соединяться практически с любым элементом периодической системы.
г) в молекулах органических соединений часто содержатся по несколько
однородных атомов, чаще всего атомов углерода.
д) большинство органических соединений не диссоциируют на ионы.
е) реакции идут медленно, не доходят до конца, дают большие выходы.
ж) для органических веществ характерна изомерия.
Изомеры – это вещества, обладающие различными свойствами, но имеющие при этом один и тот же состав и одинаковую молекулярную массу.
Электронная структура атома углерода в органических соединениях.
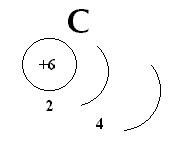
Нормальное состояние
-
2S2
2P2
1S2
Возбужденное состояние атома углерода
-
2S1
2P3
1S2

 NH2,
NH2, N
N
 арбоксильные
группы:
арбоксильные
группы:
 –
C
(альдегидная)
–
C
(альдегидная)
 О
О