- •Кинематика поступательного и вращательного движения.
- •Динамика поступательного движения.
- •Динамика вращательного движения.
- •Работа. Энергия.
- •Законы сохранения в механике.
- •Ответ: 3
- •Ответ: 4
- •Ответ: 1
- •Ответ: 1
- •Ответ: 1
- •Ответ:1
- •Ответ: 1
- •Ответ: 4
- •Ответ: 1
- •Ответ: 1
- •Ответ: 1
- •Ответ: 1
- •Ответы: 1, 2
- •Ответы: 1, 2
- •Ответ: 1
- •Ответ: 1
- •Правильный ответ 2.
- •Ответ: 3
- •Ответ: 1
- •Ответ: 1
- •Ответ: 1
- •Ответ: 1
- •Ответ: 1
- •Ответ: 3
- •Ответы: 1, 2
- •Ответы: 1, 2
- •Ответ: 1
- •Ответы: 2, 4, 6
- •Волны. Уравнение волны.
- •Ответ: 1
- •Ответ: 1
- •Энергии волны. Перенос энергии волной.
- •Интерференция и дифракция света.
- •Ответ: 3
- •Ответ: 1
- •Ответ: 1
- •Ответ: 1
- •Ответ: 1
- •Тепловое излучение. Фотоэффект.
- •Дуализм свойств микрочастиц. Соотношения неопределенностей Гейзенберга.
- •Правильный ответ 1.
- •Спектр атома водорода. Правило отбора.
- •Правильный ответ 1.
- •Правильный ответ 1.
Правильный ответ 1.
Ф6.1.2-1
Установить соответствие квантовых чисел, определяющих волновую функцию электрона в атоме водорода, их физическому смыслу 1. n А. определяет ориентации электронного облака в пространстве 2. l Б. определяет форму электронного облака 3. m В. Определяет размеры электронного облака Г. Собственный механический момент |
1: 1-В, 2-Б, 3-А* 2: 1-Г, 2-Б, 3-А 3: 1-В, 2-А, 3-Г 4: 1-А, 2-Б, 3-В |
Главное квантовое число (n) – целое число, обозначающее номер энергетического уровня. Характеризует энергию электронов, занимающих данный энергетический уровень. С возрастающим главным квантовым числом возрастают радиус орбиты и энергия электрона.
Орбитальное квантовое число (l) – определяет форму электронного облака и определяет энергетический подуровень данного энергетического уровня. Орбитальное квантовое число связано с главным квантовым числом соотношением: .
Магнитное квантовое число (m) – характеризует ориентацию в пространстве орбитального момента количества движения электрона или пространственное расположение электронной орбитали. Магнитное квантовое число принимает целые значения . Каждое из возможных значений магнитного квантового числа определяет проекцию вектора орбитального момента на данное направление (обычно ось Z). Проекция орбитального момента импульса на ось Z равна .
Спин – собственный момент импульса (или магнитный момент) элементарных частиц, имеющий квантовую природу и не связанный с перемещением частицы как целого. Спином называют также собственный момент импульса атомного ядра или атома.
Ответ: 1
Ф6.1.2-2

Правильный ответ 1.
Ф6.1.2-3
|
1* |
проекцию орбитального момента импульса электрона на заданное направление |
2 |
орбитальный механический момент электрона в атоме |
|
3 |
собственный механический момент электрона в атоме |
|
4 |
энергию стационарного состояния электрона в атоме |
Ф6.1.3-1
В атоме водорода уровню энергии номера n отвечает (без учёта спина) … |
1: 2n2 различных квантовых состояний 2: (n - 1)2 различных квантовых состояний 3: n 2 различных квантовых состояний* 4: n - 1 различных квантовых состояний 5. n + 1 различных квантовых состояний |
Для каждого n существует n орбитальных квантовых чисел, и соответственно электронных облаков. Для каждого l-облака существует 2l+1 пространственных расположение электронных орбиталей. Т.о. для каждого n существует .
Ответ: 3
Ф6.1.4-1
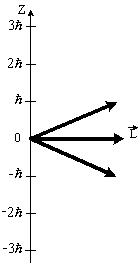
На рисунке приведена одна из возможных ориентаций момента импульса электрона в p-состоянии. Какие еще значения может принимать проекция момента импульса на направление Z внешнего магнитного поля?
|
1: 0* 2:
3:
4:
|
p-состоянию соответствует орбитальное квантовое число l=1.
Существует пространственное квантование: вектор момента импульса электрона может иметь лишь такие ориентации в пространстве, при которых проекция вектора на направление внешнего магнитного поля принимает квантовые значения; кратные : , где m – магнитное квантовое число, принимающее значения: , где – орбитальное квантовое число.
Значит, p-уровню соответствуют следующие значения проекции : , а на рисунке представлен только значение . Поэтому ещё могут быть проекции .
Ответ: 1, 2
Ф6.1.4-2
На рисунке приведена одна из возможных ориентаций момента импульса электрона в p-состоянии. Какие еще значения может принимать проекция момента импульса на направление Z внешнего магнитного поля?
|
1: 2:0* 3: 4: |
p-состоянию соответствует орбитальное квантовое число l=1.
Существует пространственное квантование: вектор момента импульса электрона может иметь лишь такие ориентации в пространстве, при которых проекция вектора на направление внешнего магнитного поля принимает квантовые значения; кратные : , где m – магнитное квантовое число, принимающее значения: , где – орбитальное квантовое число.
Значит, p-уровню соответствуют следующие значения проекции : , а на рисунке представлен только значение . Поэтому ещё могут быть проекции .
Ответ: 1, 2
Ф6.1.4-3
На рисунке приведены некоторые из возможных ориентаций момента импульса для электронов в d-состоянии. Какие еще значения может принимать проекция момента импульса на направление Z внешнего магнитного поля?
|
1: * 2: * 3:
4:
|
d-состоянию соответствует орбитальное квантовое число l=2.
Существует пространственное квантование: вектор момента импульса электрона может иметь лишь такие ориентации в пространстве, при которых проекция вектора на направление внешнего магнитного поля принимает квантовые значения; кратные : , где m – магнитное квантовое число, принимающее значения: , где – орбитальное квантовое число.
Значит, p-уровню соответствуют следующие значения проекции : , а на рисунке представленs только значения . Поэтому ещё могут быть проекции .
Ответ: 1, 2
Ф6.1.4-4
На рисунке приведены некоторые из возможных ориентаций момента импульса для электронов в d-состоянии. Какие еще значения может принимать проекция момента импульса на направление Z внешнего магнитного поля?
|
1: * 2: * 3: 4: |
d-состоянию соответствует орбитальное квантовое число l=2.
Существует пространственное квантование: вектор момента импульса электрона может иметь лишь такие ориентации в пространстве, при которых проекция вектора на направление внешнего магнитного поля принимает квантовые значения; кратные : , где m – магнитное квантовое число, принимающее значения: , где – орбитальное квантовое число.
Значит, p-уровню соответствуют следующие значения проекции : , а на рисунке представленs только значения . Поэтому ещё могут быть проекции .
Ответ: 1, 2
Ф6.1.5-1
Закон сохранения момента импульса накладывает ограничения на возможные переходы электрона в атоме с одного уровня на другой (правило отбора). В энергетическом спектре атома водорода (рис.) запрещённым переходом является …
|
1: 3p – 2s 2: 3s – 2s* 3: 4f – 3d 4: 4s – 3p |
Правило отбора гласит, что возможны только такие переходы, при которых орбитальное квантовое число l меняется на единицу: Δl = ±1. Это правило является следствием закона сохранения момента количества движения. Изменение главного квантового числа n может быть любое. Возможные переходы показаны на схеме уровней.
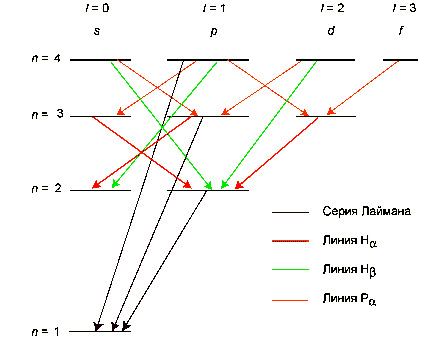
Ответ: 3s-2s
Ответ: 2
Ф6.1.5-2
При переходах электрона в атоме с одного уровня на другой закон сохранения момента импульса накладывает определенные ограничения (правило отбора). Если система энергетических уровней атома водорода имеет вид, представленный на рисунке, то запрещенными переходами являются…
|
1: 2s – 1s* 2: 4f – 2p* 3: 3d – 2p 4: 2p – 1s |
Правило отбора гласит, что возможны только такие переходы, при которых орбитальное квантовое число l меняется на единицу: Δl = ±1. Это правило есть следствие закона сохранения момента количества движения. Изменение главного квантового числа n может быть любое.
Ответ: 4f-2p, 2s-1s
Ответ: 1, 2
Ф6.1.5-3
При переходах электрона в атоме с одного уровня на другой закон сохранения момента импульса накладывает определенные ограничения (правило отбора). Если система энергетических уровней атома водорода имеет вид, представленный на рисунке, то запрещенными переходами являются…
|
1: 2s – 1s* 2: 4s – 3d* 3: 4s – 3p 4: 2p – 1s |
Правило отбора гласит, что возможны только такие переходы, при которых орбитальное квантовое число l меняется на единицу: Δl = ±1. Это правило есть следствие закона сохранения момента количества движения. Изменение главного квантового числа n может быть любое.
Ответ: 4s-3d, 2s-1s
Ф6.1.5-4
При переходах электрона в атоме с одного уровня на другой закон сохранения момента импульса накладывает определенные ограничения (правило отбора). Если система энергетических уровней атома водорода имеет вид, представленный на рисунке, то запрещенными переходами являются…
|
1: 4s – 3s* 2: 4f – 2p* 3: 3s – 2p 4: 4p – 3d |
Правило отбора гласит, что возможны только такие переходы, при которых орбитальное квантовое число l меняется на единицу: Δl = ±1. Это правило есть следствие закона сохранения момента количества движения. Изменение главного квантового числа n может быть любое.
Ответ: 4s-3s, 4f-2p
Ответ: 1, 2
Ф6.1.5-5
При переходах электрона в атоме с одного уровня на другой закон сохранения момента импульса накладывает определенные ограничения (правило отбора). Если система энергетических уровней атома водорода имеет вид, представленный на рисунке, то запрещенными переходами являются…
|
1: 3s – 2s* 2: 4f – 2p* 3: 4s – 3p 4: 3s – 2p |
Правило отбора гласит, что возможны только такие переходы, при которых орбитальное квантовое число l меняется на единицу: Δl = ±1. Это правило есть следствие закона сохранения момента количества движения. Изменение главного квантового числа n может быть любое.
Ответ: 4f-2p, 3s-2s
Ф6.1.5-6
При переходах электрона в атоме с одного уровня на другой закон сохранения момента импульса накладывает определенные ограничения (правило отбора). Если система энергетических уровней атома водорода имеет вид, представленный на рисунке, то запрещенными переходами являются…
|
1: 4p – 3p* 2: 4d – 2s* 3: 4s – 3p 4: 3d – 2p |
Правило отбора гласит, что возможны только такие переходы, при которых орбитальное квантовое число l меняется на единицу: Δl = ±1. Это правило есть следствие закона сохранения момента количества движения. Изменение главного квантового числа n может быть любое.
Ответ: 4p-3p, 4d-2s
Ответ: 1, 2
Ф6.1.5-7
|
1* |
4f-2p |
2 |
2p-1s |
|
3 |
3s-2p |
|
4 |
4p-3d |
Ф6.1.5-8
|
1* |
4d-2s |
2 |
2p-1s |
|
3 |
4s-3p |
|
4 |
3d-2p |
Ф6.1.5-9
|
1* |
5s→3d |
2 |
5d→3p |
|
3 |
4p→3s |
|
4 |
4d→3p |
Ф6.1.5-10
|
1* |
5 |
2 |
4 |
|
3 |
3 |
|
4 |
2 |
|
5 |
1 |