
(для внутрикафедрального пользования)
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РЕСПУБЛИКИ БЕЛАРУСЬ
УО «ГОМЕЛЬСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ»
Кафедра патологической
физиологии
Утверждено на заседании кафедры
протокол № 7 от 31.08.2011
Зав. кафедрой патофизиологии, к.м.н.
доцент_____________Т.С. Угольник
Патология системы пищеварения
Учебно-методическая разработка для студентов
медико-диагностического факультета
Гомель 2011 патология системы пищеварения
1. Актуальность темы: Функционирование пищеварительной системы обеспечивает поступление в организм пищи и воды, которые необходимы для снабжения его энергетическими и пластическими материалами. Если поступающая в организм пища не усваивается, развивается недостаточность пищеварения. Между различными отделами пищеварительной системы существует тесная взаимосвязь, которая в условиях патологии проявляется компенсаторными возможностями этой системы. Вместе с тем нарушение функций одного звена пищеварительной системы влечет за собой нарушение функций других. Последствиями недостаточности пищеварения являются нарушение обмена веществ, истощение, интоксикация, снижение реактивности. У детей нарушаются рост и развитие.
2. Цель занятия: изучить этиологию и патогенез расстройств пищеварительной системы.
3. Задачи занятия:
Знать основные причины и механизмы развития типовых форм расстройств пищеварительной системы.
Усвоить причины и механизмы язвообразования.
Уметь интерпретировать количественные и качественные нарушения секреторной функции желудка.
Знать и объяснить роль гастроинтестинальных гормонов в развитии патологии пищеварительного тракта.
Уметь по данным анамнеза, характерным симптомам и результатам лабораторных исследований распознать развитие у больного заболевание желудочно-кишечного тракта (на примере ситуационных задач).
Знать основные механизмы нарушений полостного и пристеночного пищеварения.
Уметь объяснить формирование компенсаторно-восстановительных процессов в системе пищеварения.
4. Основные учебные вопросы (план):
Общая этиология и патогенез расстройств пищеварительной системы.
Типовые расстройства аппетита. Нарушение слюноотделения: гипо- и гиперсаливация, его характеристика.
Типовые расстройства: вкуса, жевания, глотания, функций пищевода.
Причины и механизмы развития типовых нарушений резервуарной, секреторной и моторной функции желудка, их взаимосвязь.
Эндокринная функция желудка при патологии.
Язва желудка: причины, механизмы развития, осложнения. Дуоденальная язва.
Расстройства функций тонкого и толстого кишечника. Нарушение секреторной функции.
Расстройства полостного и пристеночного пищеварения.
Нарушение моторики кишечника: поносы, запоры, кишечная непроходимость.
Нарушение барьерной функции кишечника; кишечная аутоинтоксикация: колисепсис, дисбактериозы. Энтериты, колиты.
Нарушения секреторной функции поджелудочной железы: острые и хронические панкреатиты. Патогенез панкреатического коллапса.
Методы диагностики типовых форм нарушений желудочно-кишечного тракта.
5. Вспомогательные материалы по теме:
Недостаточность пищеварения - состояние желудочно-кишечного тракта (ЖКТ), при котором не происходит достаточного усвоения поступающей в организм пищи.
Желудочно-кишечная патология весьма многообразна, так как наряду с кожей и органами дыхания чаще других подвергается действию чрезвычайных раздражителей.
Причины, вызывающие патологию ЖКТ, подразделяют на повреждающие органы пищеварения непосредственно и опосредованно.

Рис. 1. Основные причины нарушения пищеварения в желудке и кишечнике: факторы, непосредственно повреждающие органы пищеварения.
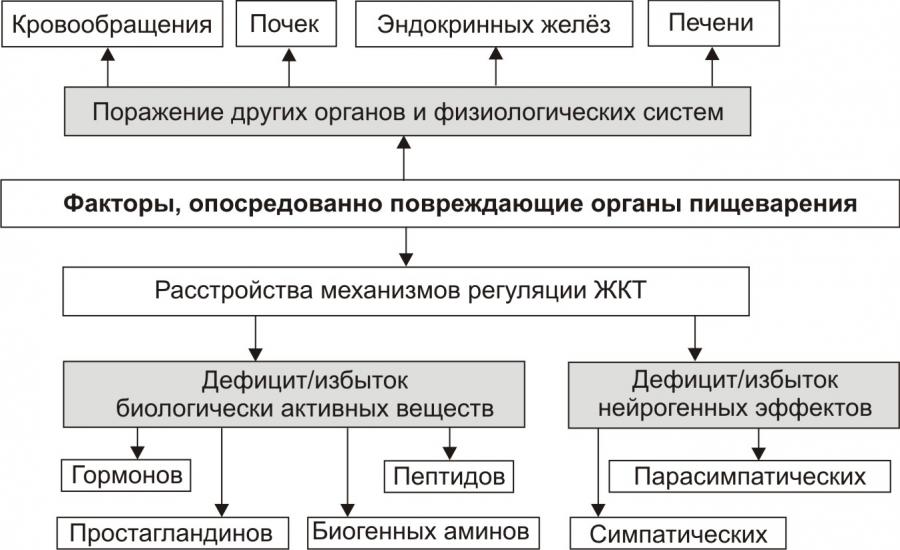
Рис. 2. Основные причины нарушения пищеварения в желудке и кишечнике: факторы, опосредованно повреждающие органы пищеварения.
Типовые формы патологии желудочно-кишечного тракта
Основные расстройства и наиболее клинически значимые типовые формы патологии ЖКТ приведены на рис. 3.
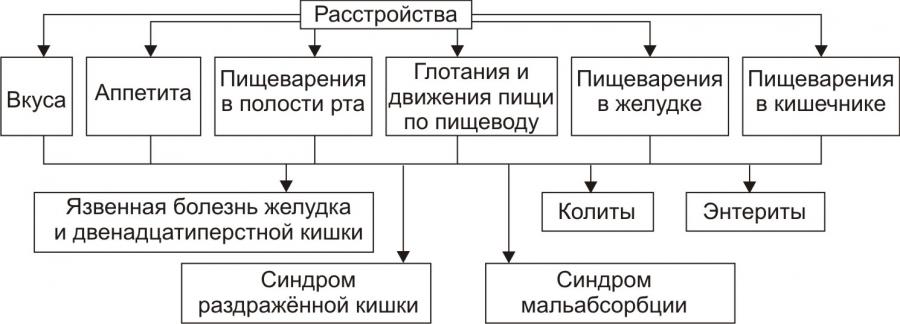
Рис. 3 Типовые формы патологии системы пищеварения.
Нарушения пищеварения в желудке
В основе нарушений пищеварения в желудке находятся парциальные, а чаще сочетанные расстройства секреторной, моторной, всасывательной, барьерной и защитной функций желудка.
В желудочной секреции различают две фазы: сложнорефлекторную и нейрохимическую. В каждую из этих фаз выделяется примерно одинаковое количество желудочного сока, и моторика желудка является равномерной (рис. 24.1, А). В условиях патологии различают пять типов желудочной секреции и моторики:
Возбудимый тип (рис. 24.1, Б). Он характеризуется быстрым и интенсивным нарастанием секреции в первую фазу, ее длительным продолжением и относительно медленным спадом во вторую фазу.
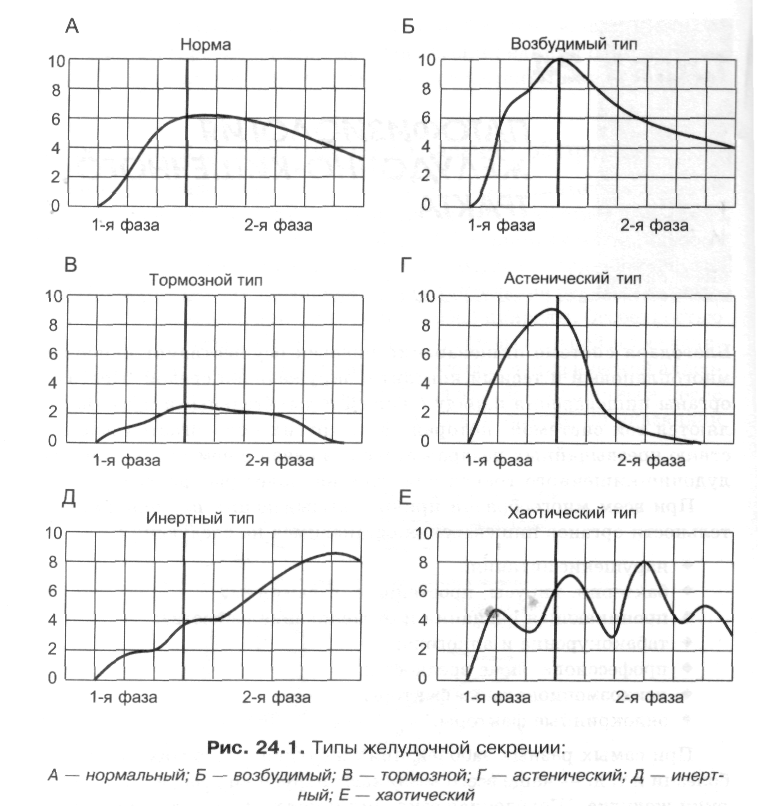
Однако соотношение интенсивности секреции между фазами остается нормальным. Моторика желудка характеризуется гиперкинезом.
Тормозной тип (рис. 24.1, В). Секреция и моторика желудка снижены в обе фазы.
Астенический тип (рис. 24.1, Г). В первую фазу происходит быстрое нарастание секреции и наблюдается бурная моторика, но этот процесс длится недолго. Во вторую фазу наблюдается быстрый спад секреции и гипокинезия желудка.
Инертный тип (рис. 24.1, Д). В первую фазу секреция нарастает медленно, но затем долго держится на высоком уровне и медленно угасает. Аналогично ведет себя и моторика.
Хаотический тип (рис. 24.1, Е). Он характеризуется отсутствием каких-либо закономерностей динамики секреции и моторики желудка.
Расстройства секреторной функции
Характеристика расстройств секреторной функции желудка приведена на рис. 4.

Рис. 4. Типовые расстройства секреторной функции желудка.
К расстройствам желудочной секреции относятся гиперсекреция, гипосекреция и ахилия.
1. Гиперсекреция — увеличение количества желудочного сока, повышение его кислотности и переваривающей способности
Причины: увеличение массы секреторных клеток желудка (детерминируется генетически), активация влияний блуждающего нерва (напр., при невротических состояниях или конституциональной ваготонии), повышение синтеза и/или эффектов гастрина, гипертрофия и/или гиперплазия энтерохромаффинных (энтероэндокринных) клеток (например, при гипертрофическом гастрите), перерастяжение антрального отдела желудка, действие некоторых ЛС (например, ацетилсалициловой кислоты или кортикостероидов).
Последствия: замедление эвакуации пищевой массы из желудка, эрозии и изъязвления слизистой оболочки желудка, сопровождающийся изжогой гастро-эзофагальный рефлюкс, нарушения пищеварения в кишечнике.
2. Гипосекреция — уменьшение объёма желудочного сока, снижение его кислотности и расщепляющей эффективности.
Причины: уменьшение массы секреторных клеток (напр., при гипо- и атрофической форме хронического гастрита или распадающейся опухоли желудка), снижение эффектов блуждающего нерва (напр., при неврозах или конституциональной симпатикотонии), снижение образования гастрина, дефицит в организме белков и витаминов, действие ЛС, снижающих или устраняющих эффекты блуждающего нерва (например, блокаторов холинорецепторов или активаторов холинэстераз).
3. Ахилия — состояние, характеризующееся практически полным отсутствием желудочной секреции. Причина ахилии — значительное снижение или прекращение секреторной функции желудка.
Таблица 1. Базальная и максимальная секреция желудка
Состояние секреции |
Секреция |
|||||
базальная |
максимальная |
|||||
Кол-во секрета мл/ч |
HCl |
Кол-во секрета мл/ч |
HCl |
|||
ммоль/ч |
ммоль/ч |
ммоль/ч |
ммоль/ч |
|||
Норма |
60±25 |
3±2,5 |
45±15 |
200±55 |
20±4 |
100±15 |
Гиперсекреция (язва двенадцатиперстной кишки) |
100 |
6 |
60 |
250 |
27,5 |
110 |
Гипосекреция (рак желудка) |
40 |
0,5 |
12,5 |
80 |
4 |
50 |
Нарушения моторики желудка
Нарушения моторной функции желудка и последствия расстройств желудочной моторики представлены на рис. 5.

Рис. 5. Типовые расстройства моторной функции желудка и её последствия.
• Последствия.
В результате нарушений моторики желудка возможно развитие синдрома раннего насыщения, изжоги, тошноты, рвоты и демпинг-синдрома.
Синдром раннего (быстрого) насыщения. Является результатом снижения тонуса и моторики антрального отдела желудка. Приём небольшого количества пищи вызывает чувство тяжести и переполнения желудка. Это создаёт субъективные ощущения насыщения.
Изжога — ощущение жжения в области нижней части пищевода (результат снижения тонуса кардиального сфинктера желудка, нижнего сфинктера пищевода и заброса в него кислого желудочного содержимого).
Тошнота. При подпороговом возбуждении рвотного центра развивается тошнота — неприятное, безболезненное субъективное ощущение, предшествующее рвоте.
Рвота — непроизвольный рефлекторный акт, характеризующийся выбросом содержимого желудка (иногда и кишечника) наружу через пищевод, глотку и полость рта.
Механизмы развития: усиленная антиперистальтика стенки желудка, сокращение мышц диафрагмы и брюшной стенки, расслабление мышц кардиального отдела желудка и пищевода, возбуждение рвотного центра продолговатого мозга.
Значение рвоты. Рвота имеет защитное и патогенное значение.
Защитное (при рвоте из желудка устраняются токсичные вещества или инородные тела).
Патогенное (потеря организмом жидкости, ионов, продуктов питания, особенно при длительной и/или повторной рвоте).
Демпинг-синдром — патологическое состояние, развивающееся в результате быстрой эвакуации желудочного содержимого в тонкий кишечник. Развивается, как правило, после удаления части желудка.
Нарушение барьерной и защитной функции желудка
Слизисто-бикарбонатный барьер защищает слизистую оболочку от действия кислоты, пепсина и других потенциальных повреждающих агентов.
• Компоненты барьера.
Слизе-бикарбонатный барьер: слизь постоянно секретируется на поверхность эпителия,
бикарбонат (ионы HCO3–) секретируется поверхностными слизистыми клетками, имеет нейтрализующее действие.
pH. Слой слизи имеет градиент pH. На поверхности слоя слизи pH равен 2, а в примембранной части более 7.
Н+. Проницаемость плазмолеммы слизистых клеток желудка для Н+ различна. Она незначительна в мембране, обращённой в просвет органа (апикальной), и достаточно высока в базальной части. При механическом повреждении слизистой оболочки, при воздействии на неё продуктов окисления, алкоголя, слабых кислот или жёлчи концентрация H+ в клетках возрастает, что приводит к их гибели и разрушению барьера.
Плотные контакты. Формируются между поверхностными клетками эпителия. При нарушении их целостности нарушается функция барьера.
• Регуляция. Секрецию бикарбоната и слизи усиливают глюкагон, ПгЕ, гастрин, эпидермальный фактор роста (EGF). Для предупреждения повреждения и восстановления барьера применяют антисекреторные агенты (напр., блокаторы гистаминовых рецепторов), Пг, гастрин, аналоги сахаров (напр., сукральфат).
• Разрушение барьера.
При неблагоприятных условиях барьер разрушается в течение нескольких минут, происходят гибель клеток эпителия, отёк и кровоизлияния в собственном слое слизистой оболочки. Существуют факторы, неблагоприятные для поддержания барьера, например нестероидные противовоспалительные препараты (аспирин, индометацин), этанол, соли жёлчных кислот.
Helicobacter pylori — грамотрицательная бактерия, выживающая в кислой среде желудка. H. pylori поражает поверхностный эпителий желудка и разрушает барьер, способствуя развитию гастрита и язвенного дефекта стенки желудка. Этот микроорганизм выделяют у 70% больных язвенной болезнью желудка и 90% больных язвой двенадцатиперстной кишки или антральным гастритом.
Снижение кислотности в желудке создаёт благоприятные условия для жизнедеятельности и размножения многих микробов, например, холерного вибриона, шигелл, амёб. Так, пациенты с желудочной ахилией чаще заболевают инфБ (передающимися орально-фекальным путём), подвергаются интоксикациям, имеют более высокий риск развития новообразований желудка.
Расстройства пищеварения в кишечнике
Расстройства пищеварения в кишечнике обусловлены нарушением основных его функций: переваривающей, всасывательной, моторной и барьерно-защитной.
Нарушения переваривающей функции кишечника
• Нарушения экзокринной функции поджелудочной железы приводят к панкреатической ахилии.
Причины.
Уменьшение массы поджелудочной железы (напр., при некрозе, резекции её части, поражении опухолью, склерозе).
Нарушение оттока секрета железы по её протокам в двенадцатиперстную кишку в результате обтурации протоков (камнем, опухолью и др.) или сдавления протоков (например, новообразованием или рубцом).
Дискинезия протоков железы (вследствие снижения тонуса или, напротив — спазма ГМК протоков).
Нарушение деятельности железы в результате нервных и гуморальных регуляторных расстройств.
• Расстройства выделения жёлчи в тонкий кишечник.
• Нарушения секреции бокаловидными клетками и бруннеровыми железами.
Причины: атрофия или гипотрофия слизистой оболочки кишечника (напр., при хроническом энтерите), резекция части тонкого кишечника, язвенно-эрозивные и некротические изменения в слизистой оболочке кишечника (например, при острых энтеритах, интоксикациях, ишемии стенки кишки).
Нарушения переваривающей функции кишечника приводят к расстройствам полостного и пристеночного (мембранного) пищеварения (в том числе к развитию синдрома мальабсорбции). Эти же расстройства сказываются и на состоянии организма в целом в силу дефицита субстратного и энергетического обеспечения организма и развития кишечной аутоинфекции и интоксикации.
Расстройства всасывательной функции кишечника
Основные причины:
Недостаточное полостное и мембранное пищеварение.
Ускорение эвакуации кишечного содержимого (например, при поносах).
Атрофия ворсинок слизистой оболочки кишечника.
Избыточное содержание экссудата на поверхности слизистой оболочки (например, при острых кишечных инфекциях, при хронических энтеритах).
Резекция большого фрагмента тонкого кишечника (например, при его опухолевом поражении и/или некрозе).
Расстройства крово- и лимфообращения в стенке кишечника.
Синдром мальабсорбции (нарушенного всасывания) — комплекс расстройств, развивающихся в результате нарушений процессов переваривания пищи и всасывания её компонентов.
Формы синдрома мальабсорбции (по происхождению):
Первичная
генетически детерминированные или врожденные ферментопатии тонкой кишки
патология абсорбирующего эпителия тонкой кишки (целиакия, тропическая спру)
Вторичная
поражения отдельных структур или всей стенки тонкой кишки, возникающие как следствие других заболеваний
Нарушение моторной функции кишечника
Формы нарушения моторики кишечника разнообразны. Крайними вариантами нарушений являются диарея и запор (рис.7).

Рис. 7. Типовые формы нарушения моторной функции кишечника и их разновидности.
• Диарея.
Понос (диарея, от гр. diarrheo — истекаю) — учащенный (более 2–3 раз в сутки) стул жидкой или кашицеобразной консистенции, сочетающийся с усилением моторики кишечника.
Основные виды и механизмы возникновения.
Экссудативный: результат избыточного образования воспалительного экссудата слизистой оболочкой кишечника (напр., при инфекционных и неинфекционных энтеритах и колитах).
Секреторный: следствие чрезмерной секреции жидкости в просвет кишечника (напр., при холере, вирусных энтероколитах).
Гиперосмоляльный: результат значительной гиперосмоляльности кишечного содержимого (напр., при нарушении всасывания компонентов кишечного химуса при мальабсорбции или передозировке солевых слабительных).
Гиперкинетический: следствие гиперсекреции и повышенной перистальтики кишечника (напр., при энтероколитах, синдроме раздражённой кишки.
Последствия: гипогидратация организма, вплоть до эксикоза (крайняя степень гипогидратации организма); гиповолемия и нередко — артериальная гипотензия, нарушения электролитного баланса и КЩР (различного характера и выраженности в зависимости от основного заболевания).
• Обстипация.
Запор (обстипация) — длительная задержка стула или затруднение опорожнения кишечника (до 3 сут и более). Наблюдается у 25–30% людей в возрасте после 70 лет.
Основные виды и механизмы возникновения.
Алиментарный (малообъёмный). Является результатом малого объёма кишечного содержимого (напр., при хроническом недоедании, малом потреблении жидкости, недостатке овощей и фруктов в пище, употреблении легкоусвояемой пищи). Малый объём кишечного содержимого и экскрементов недостаточен для активации рефлекторного процесса дефекации.
Нейрогенный (спастический и атонический запоры).
а) Спастический запор. Чрезмерное повышение вагальных нейрогенных влияний на стенку кишечника может привести к спазму её мускулатуры. Это замедляет эвакуацию пищи и опорожнение кишечника.
б) Атонический запор. Снижение нейроэффекторных воздействий на мускулатуру кишечника вызывает его гипотонию и задержку стула.
Ректальный. Является следствием патологических процессов в прямой кишке (например, трещины или парапроктита), сопровождающихся болью. Это подавляет рефлекс дефекации.
Механический. Результат механической задержки эвакуации кишечного содержимого (например, опухолью, рубцом).
Кишечная непроходимость – нарушение проходимости кишечника вследствие механического препятствия или нарушение его функций. Кишечная непроходимость может быть врожденной и приобретенной.
По патогенезу:
Механическая
Динамическая
Тромбоэмболическая
Механическая непроходимость обусловлена механическим закрытием просвета кишки опухолью, каловыми камнями, гельминтами, инородными телами или сдавление кишок извне опухолью, рубцом.
Виды:
Обтурационная механическая непроходимость (просвет кишки закрыт, но кровообращение в кишечной стенке первоначально не нарушено)
Странгуляционная механическая непроходимость (сдавливается кишечная стенка и резко страдает ее кровоснабжение)
Динамическая непроходимость возникает при спазме или параличе кишечной мускулатуры.
Тромбоэмболическая (гемостатическая) непроходимость кишечника возникает в результате нарушения кровообращения в кишечной стенке при тромбозе или параличе сосудов.
В участке непроходимости развиваются застойная гиперемия, паралич сосудов, отек, воспаление и некроз. Под влиянием болевых импульсов и сосудистых расстройств резко снижается всасывание в кишечнике, однако секреция кишечного сока продолжается. Содержимое кишечника растягивает его отделы, расположенные выше места непроходимости, раздражает рецепторы и вызывает упорную рвоту. В результате развивается обезвоживание организма, наступает сгущение крови. В крови падает содержание хлоридов, которые вместе с водой переходят в брюшную полость, увеличивается содержание аммиака, мочевины, индикана и других продуктов гниения, усиленно образующихся в кишечнике и всасывающихся в кровь Развивается тяжелая кишечная аутоинтоксикация.
Нарушение внешней секреции поджелудочной железы
Основными причинами нарушений внешней секреции поджелудочной железы являются:
1) недостаточная продукция секретина при ахлоргидрии;
2) неврогенное торможение функции поджелудочной железы (вагусная дистрофия, отравление атропином);
3) развитие в железе аллергических и утоаллергических реакций;
4) разрушение железы опухолью;
5) закупорка или сдавление протока железы;
6) дуодениты — воспалительные процессы двенадцатиперстной кишки, сопровождающиеся уменьшением образования секретина; вследствие этого снижается секреция панкреатического сока;
7) травмы брюшной полости;
8) экзогенные интоксикации;
9) острые и хронические панкреатиты.
Наиболее принята ферментативная теория патогенеза острого панкреатита. Согласно этой теории повреждение железы происходит вследствие активации в ней ферментов поджелудочного сока: липазы, трипсина, хемотрипсина, эластазы и др. Ферменты активируются, например, при забросе в железу желчи, что возможно при наличии общей ампулы желчного и панкреатического протоков и блокады устья фатерова соска. Фосфолипаза желчи активирует трипсиноген.
Другой причиной панкреатита может послужить дуоденально-панкреотический рефлюкс, развитию которого способствуют зияние фатерова соска и повышение давления в двенадцатиперстной кишке, например при ее воспалении, нарушениях диеты (переедании). При этом попадающая в железу энтеропептидаза активирует трипсиноген. Образовавшийся трипсин оказывает аутокаталитическое действие — активирует трипсиноген и другие протеолитические ферменты. Так, если в эксперименте ввести в проток поджелудочной железы небольшое количество трипсина, то происходит бурный некроз ее ткани, так образуются активные протеолитические ферменты. В условиях патологии трипсиноген может активироваться в поджелудочной железе под влиянием кофермента цитокиназы, выделяющейся из поврежденных клеток паренхимы, важную роль играет активность ингибитора трипсина, который в норме содержится в поджелудочной железе и препятствует превращению трипсиногена в трипсин. При дефиците этого фактора облегчается переход трипсиногена в трипсин в поджелудочной железе.
Трипсин активирует панкреатический калликреин, который вызывает образование каллидина и брадикинина. Эти медиаторы увеличивают проницаемость сосудов, способствуют развитию отека, раздражают рецепторы и вызывают боль. Из клеток железы освобождаются гистамин и серотонин, которые также усиливают процессы повреждения. Из разрушенных клеток железы выходит липаза, вызывающая гидролиз жиров и фосфолипидов; развивается стеатонекроз (жировой некроз) поджелудочной железы и окружающих тканей (сальник). При попадании липазы в кровь возможны стеатонекрозы отдаленных органов. Процесс может осложниться перитонитом и абсцессами брюшной полости.
Панкреатические ферменты и образовавшиеся в железе медиаторы (брадикинин и др.) могут попасть в кровоток и вызвать резкое падение артериального давления – панкреатический коллапс, иногда со смертельным исходом. При расстройствах функции поджелудочной железы в ней уменьшается и даже полностью прекращается образование пищеварительных ферментов – панкреатическая ахилия.
В связи с этим разрушается дуоденальное пищеварение. Особенно резко страдают переваривание и всасывание жира. До 60—80 % его не усваивается и выводится с калом (стеаторея). В несколько меньшей степени нарушено переваривание белка, до 30—40 % которого не усваивается. О недостаточном переваривании белка свидетельствует появление большого количества мышечных волокон в каловых массах после приема мясной пищи. Переваривание углеводов также нарушено. Расстройства пищеварения усугубляются упорной рвотой вследствие рефлекторной стимуляции центра рвоты с поврежденной поджелудочной железы. Развивается тяжелая недостаточность пищеварения.
Энтеропатии (энтериты)
Хронический энтерит — заболевание, характеризующееся нарушениями кишечного пищеварения и всасывания — обусловлен воспалительными и дистрофическими изменениями слизистой оболочки тонкой кишки.
Виды
Хронический энтерит дифференцируют в зависимости от этиологии заболевания, а также с учётом морфологических изменений, функциональной характеристики и клинических данных.
• По этиологии: инфекционный (при дизентерии, сальмонеллёзе, иерсиниозе, вирусных инфекциях и др.), паразитарный (например, при глистных инвазиях, лямблиозе); алиментарный (например, при несбалансированном питании и др.), физического и химического генеза (например, при воздействии алкоголя или ионизирующего облучения и др.).
• По анатомо-морфологическим особенностям: поверхностный энтерит с дистрофией энтероцитов, хронический энтерит без атрофии, хронический энтерит с парциальной атрофией ворсин, еюнит, илеит, энтерит.
• По функциональной характеристике: Энтерит, характеризующийся нарушением мембранного пищеварения (дисахаридазная недостаточность), нарушением всасывания (электролитов, железа, воды, витаминов, белков, жиров, углеводов), расстройствами моторной функции (гипер- и гипокинетические типы).
• По проявлениям: различают энтериты в зависимости от степени тяжести синдрома нарушенного всасывания; характера течения (часто рецидивирующее); фазы болезни (обострение, ремиссия); наличия осложнений (солярит, неспецифический мезаденит)
патогенез
Основные звенья патогенеза заболевания связаны с нарушением барьерной функции стенки кишки. Это приводит к снижению активности ферментов клеточных мембран, нарушению функций транспортных каналов, через которые всасываются продукты гидролиза, ионы и вода. Определённое значение в патогенезе хронического энтерита имеют также нарушения функций других органов пищеварения (нарушение ферментной активности пищеварительных желёз), дисбактериоз кишечника, расстройства обмена веществ, изменения иммунитета, которые вторично могут поддерживать кишечные дисфункции, создавая порочный круг.
Расстройства барьерной системы определяют клиническую картину заболевания: синдром нарушенного всасывания, рецидивирующую диарею. Развитие диареи связано с кишечной гиперсекрецией, повышенной осмолярностью содержимого тонкой кишки, ускорением кишечного транзита и дисбактериозом кишечника.
Проявления
Проявления заболевания можно разделить на две группы: внекишечные и кишечные.
• Внекишечные проявления. Связаны с синдромом нарушенного всасывания. К ним относят уменьшение массы тела (нередко до 20 кг и более), снижение трудоспособности, раздражительность, бессонница. У больных развиваются трофические изменения кожи и её придатков: сухость, истончение, шелушение кожи, выпадение волос, ломкость и утолщение ногтей. При выраженной гипопротеинемии развивается пастозность кожных покровов или отёки. У больных появляются боли в мышцах, мышечная слабость, ослабление сухожильных рефлексов, парезы, тахикардия, по данным ЭКГ снижение сегмента ST, уплощение и двухфазность зубца T, экстрасистолия, обусловленные гипокалиемией. У 2/3 больных наблюдают гипокальциемию и связанные с ней парестезии, судороги мелких мышц, симптомы Хвостека (сокращение мышц лица при поколачивании ниже скуловой дуги), Труссо (судорога кисти, рука «акушера» при наложении жгута на плечо). Дефицит витаминов, возникающий при синдроме нарушенного всасывания, может сопровождаться различной симптоматикой: развитием гемералопии (недостаточность витамина A), хейлита (недостаточность витамина B2), глоссита (недостаточность витамина B12), подкожных кровоизлияний (недостаточность витамина K), оссалгии и миопатии (недостаточность витамина D), невропатии (недостаточность витаминов B1, B2, E).
• Кишечные проявления. Если в процесс вовлекается только начальный отдел тощей кишки, заболевание протекает с минимальными кишечными симптомами. При вовлечении подвздошной кишки может нарушаться абсорбция жёлчных кислот, осуществляемая в норме в дистальном отделе кишечника. Это приводит к их избыточному поступлению в толстую кишку и вызывает диарею, так как жёлчные кислоты стимулируют секрецию воды, ионов натрия и хлора в просвет кишечника и активизируют его моторную функцию. Больных беспокоит боль в правой подвздошной области. Нарушается функция илеоцекального клапана, что ведёт к забросу в подвздошную кишку содержимого толстой кишки и обсеменению первой микробной флорой. При длительном рефлюкс–илеите может нарушаться абсорбция витамина B12 с последующим развитием B12-дефицитной анемии.
• Боли, локализующиеся в средней части живота, вокруг пупка. Они возникают через 3–4 ч после еды. По характеру они могут быть различными: схваткообразными, тупыми, распирающими. При пальпации ощущается болезненность в проекции тощей кишки — слева выше пупка, шум плеска в петлях кишечника, особенно часто в слепой кишке (симптом Образцова).
• Стул жидкий, учащённый до 5–6 раз в сутки, жёлтого цвета, обильный (полифекалия). Стеаторея: каловые массы блестящие, плохо смываются с унитаза. Больных беспокоит метеоризм, вздутие, урчание в животе.
Колиты
К колитам отнесены хронический колит, синдром раздражённой кишки и неспецифический язвенный колит.
Хронический колит — заболевание, характеризующееся воспалительно-дистрофическими изменениями слизистой оболочки толстой кишки и нарушением её функций. Заболевание достаточно широко распространено, так как около половины больных, обращающихся за медицинской помощью по поводу различных заболеваний органов пищеварения, страдают хроническим колитом. У женщин заболевание чаще возникает в возрасте 20–60 лет, у мужчин — 40–60 лет.
Синдром раздражённой кишки — устойчивая совокупность функциональных расстройств, проявляющаяся болью и/или дискомфортом в животе, которые проходят после дефекации, сопровождаются изменением частоты и консистенции стула.
Неспецифический язвенный колит (НЯК) — хроническое воспалительное заболевание толстой кишки, характеризующееся язвенно-деструктивными изменениями её слизистой оболочки. Распространённость — 50–230 случаев на 100 000 населения. Заболевание возникает во всех возрастных группах, но основной пик приходится на 20–40 лет. Мужчины и женщины болеют с одинаковой частотой.
Нарушения выработки гормонов пищеварительной системы
АПУД-система (диффузная нейроэндокринная система) – система, представлена эндокринными клетками, способными поглощать предшественников биогенных аминов и декарбоксилировать их, превращая в биогенные амины, а также, синтезировать различные пептидные гормоны.
Таблица 2. Основные эффекты гастроинтестинальных пептидов в пищеварительном тракте
Название |
Основная локализация |
Механизм действия |
Роль в патологии |
Гастрин |
Антральный отдел желудка |
Стимуляция секреции кислоты в желудке и ферментов в поджелудочной железе, сокращение НПС, освобождение кальцитонина |
Повышен уровень при ахлоргидрии, пернициозной анемии, ваготомии; опосредует синдром Золлингера-Эллисона |
Холецистокинин |
Тонкая кишка |
Стимуляция сокращения желчного пузыря и секреции ферментов поджелудочной железой, трофическое действие на поджелудочную железу, торможение аппетита |
Повышен уровень при недостаточности поджелудочной железы, снижен при целиакии |
Секретин |
Тонкая кишка |
Стимуляция секреции гидрокарбоната поджелудочной железой, торможение секреции кислоты в желудке, расслабление НПС |
Снижен уровень при целиакии |
Гастроингибирующий пептид (ГИП) |
Тонкая кишка |
Торможение секреции кислоты и моторики желудка, стимуляция секреции инсулина |
Снижен уровень при целиакии, предполагают участие в патогенезе ожирения |
Вазоактивный интестинальный пептид (ВИП) |
Тонкая кишка |
Снижает тонус сосудов, активирует панкреатическую и кишечную секрецию |
Опосредует синдром Вернера-Морисона |
Энтероглюкагон |
Тонкая и толстая кишка |
Трофическое влияние на слизистую оболочку кишечника |
Повышен уровень при удалении или повреждении слизистой оболочки |
Мотилин |
Тонкая кишка |
Стимуляция моторики желудка, кишечника |
Повышен уровень при диарее
|
Нейротензин |
Тонкая кишка |
Стимуляция секреции в тонкой кишке, гипотензия, угнетение секреции кислоты в желудке и инсулина |
Повышен уровень при мальабсорбции |
Соматостатин |
Гипоталамус, поджелудочная железа, желудок |
Торможение желудочной и панкреатической секреции, выработки СТГ, гастрина, ГИП, инсулина, глюкагона |
Опосредует синдром соматостатиномы (диспепсия + сахарный диабет + холелитиаз) |
Панкреатический полипептид |
Поджелудочная железа |
Торможение секреции ферментов поджелудочной железой и сокращение желчного пузыря, моторики желудка и кишечника |
Снижен уровень при недостаточности поджелудочной железы, повышен при диарее |
Опиоидные пептиды (эндорфины) |
Мозг, кишечник, желудок |
Торможение желудочной секреции, активация моторики кишечника, расслабление НПС, стимуляция аппетита |
Снижен уровень при ожирении, повышен при голодании, предполагают участие в патогенезе «синдрома раздраженной кишки» |
Методы диагностики типовых форм нарушений желудочно-кишечного тракта
Эзофагогастродуоденоскопия
Эзофагогастродуоденоскопия (ЭГДС) позволяет осмотреть слизистую оболочку пищевода, желудка и проксимального отдела двенадцатиперстной кишки с помощью гибкого фиброволоконного или видеоэндоскопа. Она показана при желудочно-кишечных кровотечениях, кровавой рвоте, дегтеобразном стуле, болях за грудиной или в эпигастрии, рефлюкс-эзофагите, дисфагии, анемии, стриктурах пищевода и выходного отдела желудка, язвенной болезни желудка и двенадцатиперстной кишки; ее выполняют также для удаления инородных тел пищевода и желудка и при послеоперационных рецидивах заболеваний этих органов. ЭГДС нередко устраняет необходимость в диагностической торако- или лапаротомии и позволяет выявить небольшие или поверхностные очаги поражения, которые невозможно обнаружить при рентгенологическом исследовании. Кроме того, ЭГДС благодаря возможности выполнения щипковой и щеточной биопсии позволяет уточнить характер поражения, выявленного при рентгенологическом исследовании. С помощью ЭГДС можно также удалить инородные тела, как мелкие и мягкой консистенции путем отсасывания, так и крупные и твердые с помощью коагуляционной петли и щипцов. Цель
Диагностика воспалительных заболеваний, злокачественных и доброкачественных опухолей, язвенной болезни, синдрома Мэллори-Вейса.
Оценка состояния желудка и двенадцатиперстной кишки после операции.
Срочная диагностика язвенной болезни и повреждений пищевода (например, при химическом ожоге).
Колоноскопия
При колоноскопии с помощью фиброволоконного эндоскопа осматривают слизистую оболочку толстой кишки. Колоноскопия показана пациентам, страдающим запорами и диареей, ректальными кровотечениями, а также болями в нижних отделах живота, когда с помощью ректороманоскопии и ирригоскопии установить причину заболевания не удается. Цель
Диагностика воспалительного или язвенного поражения толстой кишки.
Установление источника кровотечения из нижних отделов ЖКТ.
Диагностика стриктур толстой кишки, обусловленных злокачественной или доброкачественной опухолью.
Послеоперационный контроль за состоянием толстой кишки (выявление рецидива полипа или злокачественной опухоли).
Виртуальная колоноскопия
Виртуальная колоноскопия сочетает в себе КТ и рентгенографию и осуществляется с помощью сложных компьютеров, позволяющих получить трехмерное изображение толстой кишки пациента. Интерпретация этих изображений и воссоздание на их основе картины внутренней поверхности кишки требуют специально обученного врача. Хотя по своей информативности виртуальная колоноскопия несколько уступает колоноскопии, она менее инвазивна и позволяет выявить даже небольшие полипы.
Ректороманоскопия
Ректороманоскопия включает в себя осмотр слизистой оболочки сигмовидной и прямой кишок с помощью ректороманоскопа и ректоскопа и пальцевое исследование анального канала. Она показана пациентам с нарушением стула, болью в нижних отделах живота и в промежности, выпадением прямой кишки при дефекации, анальным зудом и примесью слизи, крови и гноя в кале. Образцы для исследования можно получить с помощью биопсионных щипцов, смывов, щетки и стерильного тампона. К осложнениям ректороманоскопии относятся кровотечение и, реже, перфорация. Цель - диагностика воспалительного процесса, кишечной инфекции, неспецифического язвенного колита, а также выявление геморроя, гипертрофического анального сосочка, полипов, трещины и свищей прямой кишки и анального канала.
Эндоскопическое УЗИ
Эндоскопическое УЗИ является комбинированным методом, который включает в себя эндоскопическое и ультразвуковое исследование ЖКТ. Ультразвуковой датчик, вмонтиро-ванный в дистальный конец эндоскопа, позволяет получить ультразвуковое изображение высокого разрешения. Цель
Осмотр пищевода, желудка, двенадцатиперстной кишки, поджелудочной железы, печеночно-поджелудочной ампулы, желчных протоков и прямой кишки, оценка их состояния и уточнение стадии заболевания.
Диагностика подслизистой опухоли.
Уточнение локализации опухолей с эндокринной активностью.
Методы обнаружения Хеликобактер пилори
Инфицирование человека Helicobacter Pylori с высокой вероятностью приводит к заболеваниям гастритом, язвой двенадцатиперстной кишки и желудка, раком желудка. Современная медицина обладает средствами эрадикации Helicobacter Pylori. Однако, необходимо выяснить имеется ли инфицированность у человека, а также проконтролировать результаты лечения.
Обычно для обнаружения Н. рylori используется один из следующих методов: гистологический, цитологический, серологический тест, быстрый уреазный тест, полимеразно-цепная реакция, фазово-контрастная микроскопия, тест на бактериокультуру и дыхательный тест.
|
Прямые |
Косвенные |
Инвазивные |
Тест на бактериокультуру Полимеразно-цепная реакция
|
Быстрый уреазный тест Гистология Цитология Фазово-контрастная микроскопия |
Неинвазивные |
|
Изотопный дыхательный тест Серологический тест
|
При применении инвазивных методов диагностики проводится биопсия для получения образцов тканей желудка, которые в дальнейшем и исследуются. Как правило, взятие биопсийных образцов совмещается с проведением гастроскопии.
Наиболее распространенным методом диагностики бактерий является гистологическое исследование. Данный метод весьма точен и долгое время являлся "золотым стандартом", однако, если бактерии распределены неравномерно (например, в 1-5 % случаев они присутствуют в теле желудка и отсутствуют в антральной его части или наоборот), то можно получить ложноотрицательный результат. Чувствительность и специфичность цитологического метода исследования не превышают 60-75 %.
Полимеразно-цепная реакция (ПЦР) - метод дающий практически 100%-ную точность, однако он требует очень аккуратного обращения с исследуемыми образцами.
Тест на бактериокультуру, гистология, ПЦР - все эти методы требуют высокой квалификации персонала, проводящего исследования.
Относительно точным неинвазивным методом является серологический тест на определение антител к Helicobacter pylori, но для контроля за проводимой терапией он не подходит, поскольку антитела в крови сохраняются в течение длительного времени (от 4 до 24 месяцев) после проведенного лечения, когда самих бактерий в желудке уже нет.
Дыхательный изотопный тест является наиболее подходящим для мониторинга проводимого лечения, кроме того, он с успехом может использоваться и в диагностических целях, поскольку его высокая чувствительность (98 %) и специфичность (100 %) позволяют определить присутствие Н. pylori уже на ранних стадиях заболевания.
6. Контрольные вопросы по теме:
Назовите основные причины нарушения пищеварения. Какова роль ионизирующей радиации и психоэмоциональных факторов в развитии патологии желудочно-кишечного тракта?
Какова роль в развитии патологии желудочно-кишечного тракта?
Какие существуют формы расстройства аппетита?
Рвотный акт: это патологическая или защитная реакция?
Какую роль играет рефлюкс-эзофагит в возникновении изжоги?
Какие существуют патологические типы желудочной секреции?
Роль Helicobacter pylori в гастродуоденальной патологии.
Какую роль играют нейрогенные факторы в развитии язвы желудка?
В чем заключается защитная роль слизистой оболочки желудка?
Что такое защитные и агрессивные факторы язвообразования?
Каковы этапы патогенеза дуоденальной язвы и язвы желудка?
Какие патологические нарушения возникают после резекции желудка?
Значение повреждения энтероцитов, панкреатической ахилии, ахолии.
Дайте определение понятию панкреатический коллапс?
Назовите виды и стадии кишечной непроходимости.
Назовите механизмы колисепсиса?
Назовите методы диагностики панкреатита?
Охарактеризуйте методы диагностики язвы желудка?
7. Материалы для самоподготовки и УИРС:
Нейрогуморальная регуляция пищеварения.
Роль Helicobacter pylori в гастродуоденальной патологии.
Пострезекционные синдромы и их патофизиологическое обоснование.
Этиология и патогенез кишечной непроходимости.
Острые и хронические панкреатиты.
Нарушение секреторной функции желудка.
8. Укажите все правильные ответы:
1. Укажите последствия плохого пережевывания пищи:
а) уменьшение рефлекторного отделения желудочного сока;
б) усиление секреции желудочного сока;
в) уменьшение рефлекторного отделения панкреатического сока;
г) увеличение секреции панкреатического сока;
д) возможное механическое повреждение слизистой пищевода, желудка;
е) замедление пищеварения в желудке.
Ответ: а), в), д).
2. Укажите факторы, участвующие в патогенезе изжоги:
а) зияние кардии;
б) гастроэзофагальный рефлюкс;
в) спазм и антиперистальтика пищевода;
г) понижение кислотности желудочного сока;
д) увеличение содержания в желудке органических кислот;
е) понижение чувствительности рецепторов пищевода.
Ответ: а), б), в), д).
3. К каким изменениям в желудке приводит чрезмерное повышение тонуса парасимпатических нервов:
а) увеличение образования слизи;
б) уменьшение образования слизи;
в) увеличение секреции желудочного сока;
г) уменьшение выделения гистамина;
д) увеличение выделения гистамина;
е) гиперсекреция соляной кислоты.
Ответ: б), в), д), е).
Примеры решения ситуационных задач
Задача 1.
Крысам массой 160-180 г. вводили внутримышечно ежедневно по 0,5-1,0 мг гидрокортизона на 100 г массы животного. После 10-15 инъекций у всех животных появлялись эрозии или язвы в секреторном отделе желудка.
Объяснить механизмы развития "гидрокортизоновой" язвы желудка у подопытных животных.
Ответ.
Глюкокортикоиды усиливают секрецию желудочного сока, стимулируя продукцию пепсина и соляной кислоты главным и обкладочными клетками и тем самым повышая его переваривающую способность. Одновременно глюкокортикоиды подавляют процессы пролиферации и регенерации слизистой желудка, уменьшают продукцию слизи. Таким образом, в основе стероидных язв лежит повышение активности кислотно-пептического фактора на фоне недостаточности местных механизмов защиты слизистой от повреждения.
Задача 2.
Больной М., 52 лет, поступил в клинику на обследование. Примерно 3 мес. назад ухудшился аппетит, появилось отвращение к мясу, стал худеть.
В анамнезе в течение 12 лет не резко выраженные боли в эпигастральной области, изжога.
При фракционном зондировании выявлено: порция натощак - 5 мл желудочного содержимого, свободная соляная кислота - 0, общая кислотность - 35 т.ед. Базальная секреция: часовое напряжение - 25 мл, свободная соляная кислота - 0, общая кислотность - 12-18 т.ед. В ответ на гистаминовую стимуляцию: часовое напряжение секреции - 20 мл, свободная соляная кислота - следы, общая кислотность - 15-21 т.ед.
1. Каков характер нарушения секреторной функции желудка?
2. Как объяснить высокие цифры общей кислотности при отсутствии свободной соляной кислоты в порции, полученной натощак?
Ответ:
1. Выраженная секреторная недостаточность. Анацидное состояние.
2. Разрыв между общей кислотностью и свободной соляной кислотой может быть обусловлен накоплением в желудке большого количества органических кислот, в частности молочной. Одной из причин накопления молочной кислоты может быть активация процессов гниения и брожения в условиях ахлоргидрии. Другой причиной накопления молочной кислоты может быть наличие опухоли в желудке, клетки которой продуцируют ее в большом количестве.
