
- •1. Атом
- •2. Атомная масса
- •3. Нуклид
- •4. Модель атома по бору и резерфорду
- •5. Принцип неопределенности Гейзенберга
- •6. Уравнение де Бройля
- •7. Уравнение Шредингера
- •8. Волновая функция
- •9. Квантовые числа
- •10. Порядок заполнения орбитали
- •11. Принцип (запрет) Паули
- •12. Правило Хунда
- •13. Периодичность изменения свойств элементов:
- •14. Виды химической связи
- •15. Основные характеристики химической связи: энергия и длина связи
- •16. Ионная связь, ковалентная связь и их особенности
- •17. Полярность связи
- •18. Метод валентных связей
- •19. Донорно-акцепторный механизм образования связи
- •20. Σ,π,δ связи
- •21. Кратные связи. Делокализация связи
- •22. Гибридизация атомных орбиталей. Теория полной гибридизации Гиллеспи
- •23. Пространственная конфигурация молекул
- •24. Полярность молекул
- •25. Метод молкао (молекулярная орбиталь есть линейная комбинация атомных орбиталей)
- •26. Порядок и энергия связь в методе мо лкао
- •27. Водородная связь
21. Кратные связи. Делокализация связи
____________
22. Гибридизация атомных орбиталей. Теория полной гибридизации Гиллеспи
ГИБРИДИЗАЦИЯ АТОМНЫХ ОРБИТАЛЕЙ,
квантовохим. способ описания
перестройки орбиталей атома в молекуле по
сравнению со своб. атомом.
Являясь формальным мат.
приемом, гибридизация атомных орбиталей позволяет
отразить нарушение
сферич. симметрии распределенияэлектронной
плотности атома при
образовании хим. связи.
Сущность гибридизации атомных орбиталей состоит
в том, что электрон молекулывблизи
выделенного атомного
ядра характеризуется
не отдельной атомной орбиталью (АО),
а линейной комбинацией атомных орбита-лей
с разл. значениями азимутального и
магнитного квантовых чисел. Такая
линейная комбинация наз. гибридной
(гибридизированной) орбиталью (ГО).
Как правило, гибридизация затрагивает
лишь высшие и близкие по энергии занятые
АО своб. атома.
Напр., для атомов элементов
второго периода периодич. системы
типичная форма ГО![]() -линейная
комбинация 2s-орбитали
-линейная
комбинация 2s-орбитали![]() и
2р-орбиталей
и
2р-орбиталей![]()
![]() ,
,![]()
![]() ,
,![]() с
численными коэффициентами
с
численными коэффициентами![]() и
и
ГО
обладают более низкой симметрией,
чем составляющие их АО. Так,
распределение электронной
плотности,
отвечающее указанной ГО![]() ,
смещено от атомного
ядра в
направлении вектора п
с координатами
,
смещено от атомного
ядра в
направлении вектора п
с координатами![]() ; вектор п
является осью симметрии ГО
(рис. 1). При изменении ориентации в
пространстве осей координат коэффициенты
линейной комбинации могут изменяться,
однако остается постоянным отношение
сумм квадратов коэффициентов для данного
значения азимутального квантового
числа. Это отношение определяет тип ГО.
Напр., орбиталь
; вектор п
является осью симметрии ГО
(рис. 1). При изменении ориентации в
пространстве осей координат коэффициенты
линейной комбинации могут изменяться,
однако остается постоянным отношение
сумм квадратов коэффициентов для данного
значения азимутального квантового
числа. Это отношение определяет тип ГО.
Напр., орбиталь![]() относится
к типу sapb,
где а и b- числа, подобранные так, чтобы
относится
к типу sapb,
где а и b- числа, подобранные так, чтобы![]() .
Обычно принимают а — 1, b = 1, 2 или 3.
.
Обычно принимают а — 1, b = 1, 2 или 3.
Как правило, гибридные орбитали данного атома в молекуле относятся к одному типу, к-рый называют типом гибридизации атома. Так, атом N вмолекуле аммиака имеет гибридизацию типа sp3, атом С в молекуле этилена - sp2-гибридизацию, атом С в молекуле ацетилена - sp-гибридизацию. Это дает основание отождествлять тип гибридизации атома в молекуле с символом его некоей гипотетич. электронной конфигурации.
Обычно
система ГО строится таким образом, чтобы
для разных орбиталей одного атома интегралы
перекрывания были равны нулю
(см.Молекулярные
интегралы).
Кроме того, каждая орбиталь в молекуле либо
остается негибридизированной АО, либо
выбирается гибридизированной по
определенному типу. Этим требованиям
удовлетворяют неск. наборов орбиталей.
Напр., атом О
в молекуле Н2О
можно считать как sp2-,
так и 5р3-гибридизированным.
Оси симметрии всех орбиталей обычно
образуют симметричную фигуру (см. рис.
2). Операции симметрии этой
фигуры переводят ГО одного атома друг
в друга. Такие ГО наз. эквивалентными.
Напр., линейная комбинация четырех
валентных АО атома С
приводит к четырем 5р3-гибридным орбиталям,
оси симметрии к-рых
по отношению друг к другу расположены
под углом 109,5°, т.е. направлены по углам
тетраэдра (рис. 2, в).
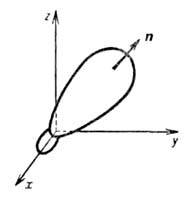
Рис.
1. Гибридная орбиталь,
образованная из 2s- и 2р-атомных орбиталей;
х, у, z- координатные оси, п-ось симметрии.
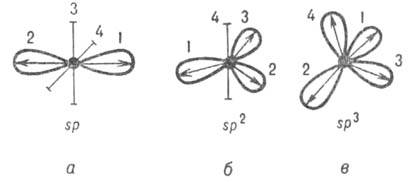
Рис. 2. Система гибридных орбиталей 5р"-типа (1, 2, 3, 4); о, б, в соответствуют п = 1, 2, 3. Оси симметрии негибридизированных атомных орбиталейизображены отрезками. Стрелками указано направление смещения электронной плотности.
Представление о гибридизации атомных орбиталей используется для изучения закономерностей изменения электронной плотности молекулывблизи к.-л. атомного ядра в зависимости от его окружения, т.е. позволяет установить связь между электронным строением молекулы и ее структурой. При этом возможны разл. подходы к анализу этой связи. Если известно геом. расположение атомных ядер, расчет волновой ф-циимолекулы можно свести к изучению парных взаимод. соседних атомов (см. Валентных связей метод, Молекулярных орбиталей методы). Для такого расчета выбирают одну из возможных систем ГО и располагают ее в пространстве так, чтобы обеспечить макс. перекрывание отдельных пар ГО разных атомов. Другой подход применяется в неэмпирических методах квантовой химии, в к-рых все взаимод. атомов в молекуле учитываются одновременно и волновая ф-ция молекулы не зависит от того, атомные или гибридизированные орбитали используются для расчета. В этом случае ГО строят после определения волновой ф-ции молекулы таким образом, чтобы в отдельных областях пространства распределение электронной плотности можно было описать одной ГО. В обоих подходах тип гибридизации атомных орбиталей обусловлен геом. конфигурацией молекулы и для большинства равновесных конфигураций оба подхода приводят к близким формам ГО.
В теоретич. химии для систематизации эксперимент. данных о равновесных конфигурациях молекул часто применяют феноменологич. подход, в рамках к-рого атомы данного элемента склонны к гибридизации определенного типа, а тип гибридизации определяет взаимное расположение ядер ближайшего окружения. Отклонение конфигурации молекулы от симметричной связывают с взаимод. хим. связей (напр., с отталкиванием парэлектронов, образующих связь). В такой форме представления о гибридизации атомных орбиталей используются в стереохимии.
Понятие о гибридизации атомных орбиталей введено в химию Л. Полингом в 1931.
