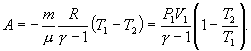- •8 Вопрос:
- •12 Вопрос: Изопроцессы
- •13 Вопрос:
- •Вывод основного уравнения мкт
- •Уравнение среднеквадратичной скорости молекулы
- •15 Вопрос: Закон Максвелла о распределении молекул идеального газа по скоростям и энергиям теплового движения
- •16 Вопрос: Число степеней свободы молекулы и закон равномерного распределения энергии по степеням свободы молекул
- •17 Вопрос: Внутренняя энергия
- •Идеальные газы
- •19 Вопрос:
- •Раздел 2. Электричество. Постоянный ток. Магнетизм.
- •24 Вопрос: Работа по перемещению заряда в электрическом поле. Потенциал
- •26 Вопрос:
- •28 Вопрос: 1.8. Электрический ток. Закон Ома
- •30 Вопрос: Закон Ома для неоднородного участка цепи
- •32 Вопрос: Закон Био - Савара - Лапласа и его применение к расчету магнитного поля
- •34 Вопрос:
- •35 Вопрос: Сила Лоренца
- •36 Вопрос: Закон полного тока
- •Ток смещения
- •37 Вопрос: Основные формулы
- •38 Вопрос: Явление электромагнитной индукции.
- •Закон Фарадея
- •40 Вопрос: Уравнения Максвелла для электромагнитного поля
- •Раздел 3. Оптика и атомная физика
- •45 Вопрос: Дифракция Света
- •47 Вопрос: фракция Фраунгофера на одной щели
- •48 Вопрос: Дифракция Фраунгофера на дифракционной решетке. Условия минимумов и максимумов.
- •Энергетическая светимость тела
- •52 Вопрос: 1.2. Законы Кирхгофа
- •53 Вопрос: Формулы Рэлея - Джинса и Планка
- •54 Вопрос: Модели атома Томсона и Резерфорда
- •55 Вопрос: Формула Бальмера
- •История создания формулы Бальмера и ее значение
- •57 Вопрос: Квантовые числа и их физический смысл
- •58 Вопрос: Состав атомного ядра
- •1919 Г. Э. Резерфорд. Ядерная реакция. 14n(α,p)17o
- •1919 Г. Э. Резерфорд. Ядерная реакция. 14n(α,p)17o
- •1932 Г. Дж. Чедвик. Открытие нейтрона
- •Нейтроны
- •Размер ядра
- •Размер ядра и закон сил
- •Характеристики свободных нейтрона и протона
- •59 Вопрос: Закон радиоактивного распада
19 Вопрос:
Применение первого начала термодинамики к изопроцессам |
Среди
равновесных процессов, которые
происходят с термодинамическими
системами, отдельно рассматриваются
изопроцессы, при которых один из
основных параметров состояния остается
постоянным.
Изохорный
процесс
(V=const). Диаграмма этого процесса
(изохора)
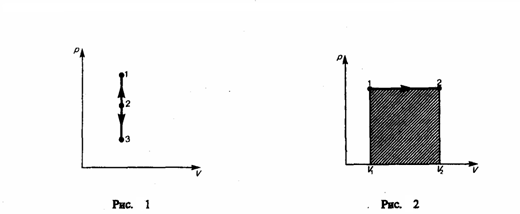
в координатах р, V изображается прямой,
параллельной оси ординат (рис. 1), где
процесс 1—2 есть изохорное нагревание,
а 1—3 — изохорное охлаждение. При
изохорном процессе газ не совершает
работы над внешними телами, т. е.
Рис.1
В
изобарном процессе при сообщении газу
массой m количества теплоты
|
20
вопрос: Адиабатический процесс - это
такое изменение состояний газа, при
котором он не отдает и не поглощает
извне теплоты. Следовательно, адиабатический
процесс характеризуется отсутствием
теплообмена газа с окружающей средой.
Адиабатическими можно считать быстро
протекающие процессы. Так как передачи
теплоты при адиабатическом процессе
не происходит, то
![]() и
уравнение I начала термодинамики
принимает вид
и
уравнение I начала термодинамики
принимает вид
|
(9.20) |
или
![]()
т.е. внешняя работа газа может производиться вследствие изменения его внутренней энергии. Адиабатное расширение газа (dV>0) сопровождается положительной внешней работой, но при этом внутренняя энергия уменьшается и газ охлаждается (dT<0).
Сжатие газа (dV0, т.е. адиабатное сжатие газа сопровождается его нагреванием.
Найдем связь между параметрами состояния идеального газа (например, Р и V) в адиабатическом процессе. Для этого перепишем (9.20) в форме
![]()
а
величину
![]() найдем
из уравнения Менделеева - Клапейрона
найдем
из уравнения Менделеева - Клапейрона
![]() Таким
образом,
Таким
образом,
![]() или,
учитывая, что для идеального газа
или,
учитывая, что для идеального газа
![]()
![]() Разделим
обе части этого уравнения на
Разделим
обе части этого уравнения на
![]()
![]()
где
![]() безразмерная
величина, называемая постоянной адиабаты.
Пренебрегая зависимостью
безразмерная
величина, называемая постоянной адиабаты.
Пренебрегая зависимостью
![]() от
температуры, можно считать, что для
данного газа
от
температуры, можно считать, что для
данного газа
![]() .
Интегрируя последнее уравнение
.
Интегрируя последнее уравнение
![]() получим
получим
![]() т.е.
т.е.
|
(9.21) |
Это выражение называют уравнением Пуассона. Соотношение между давлением и температурой, а также между объемом и температурой идеального газа в адиабатическом процессе имеют вид
![]()
Эти
соотношения легко получить из (9.21),
пользуясь уравнением Менделеева -
Клапейрона. Линию, изображающую
адиабатический процесс в диаграмме
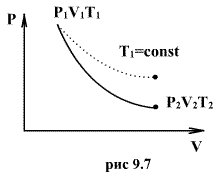
состояния, называют адиабатой. На рис.
9.7 сплошной линией показан вид адиабаты
в (P-V) диаграмме. Для сравнения в том же
рисунке пунктирной линией изображена
изотерма, соответствующая температуре
газа в начальном состоянии 1. Так как
для любого идеального газа показатель
адиабаты
![]() ,
то в (P-V) диаграмме адиабата всегда идет
круче, чем изотерма. Объясняется это
тем, что при адиабатическом сжатии
увеличение давления обусловлено не
только уменьшением объема газа, как при
изотермическом сжатии, то также еще и
увеличения температуры. При адиабатическом
расширении температура газа уменьшается,
поэтому давление газа падает быстрее,
чем при изотермическом расширении.
,
то в (P-V) диаграмме адиабата всегда идет
круче, чем изотерма. Объясняется это
тем, что при адиабатическом сжатии
увеличение давления обусловлено не
только уменьшением объема газа, как при
изотермическом сжатии, то также еще и
увеличения температуры. При адиабатическом
расширении температура газа уменьшается,
поэтому давление газа падает быстрее,
чем при изотермическом расширении.
Работу, совершаемую газом в адиабатическом процессе, найдем интегрируя выражение
![]() Полная
работа
Полная
работа
![]()
Из
уравнения Майера (9.18) и выражения
![]() для
показателя адиабаты γ следует, что
для
показателя адиабаты γ следует, что
![]()
Поэтому
|
(9.22) |
В
соответствии с соотношением
![]()
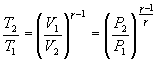
Следовательно, выражение (9.22) для работы можно представить в виде
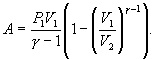 или
или