- •8 Вопрос:
- •12 Вопрос: Изопроцессы
- •13 Вопрос:
- •Вывод основного уравнения мкт
- •Уравнение среднеквадратичной скорости молекулы
- •15 Вопрос: Закон Максвелла о распределении молекул идеального газа по скоростям и энергиям теплового движения
- •16 Вопрос: Число степеней свободы молекулы и закон равномерного распределения энергии по степеням свободы молекул
- •17 Вопрос: Внутренняя энергия
- •Идеальные газы
- •19 Вопрос:
- •Раздел 2. Электричество. Постоянный ток. Магнетизм.
- •24 Вопрос: Работа по перемещению заряда в электрическом поле. Потенциал
- •26 Вопрос:
- •28 Вопрос: 1.8. Электрический ток. Закон Ома
- •30 Вопрос: Закон Ома для неоднородного участка цепи
- •32 Вопрос: Закон Био - Савара - Лапласа и его применение к расчету магнитного поля
- •34 Вопрос:
- •35 Вопрос: Сила Лоренца
- •36 Вопрос: Закон полного тока
- •Ток смещения
- •37 Вопрос: Основные формулы
- •38 Вопрос: Явление электромагнитной индукции.
- •Закон Фарадея
- •40 Вопрос: Уравнения Максвелла для электромагнитного поля
- •Раздел 3. Оптика и атомная физика
- •45 Вопрос: Дифракция Света
- •47 Вопрос: фракция Фраунгофера на одной щели
- •48 Вопрос: Дифракция Фраунгофера на дифракционной решетке. Условия минимумов и максимумов.
- •Энергетическая светимость тела
- •52 Вопрос: 1.2. Законы Кирхгофа
- •53 Вопрос: Формулы Рэлея - Джинса и Планка
- •54 Вопрос: Модели атома Томсона и Резерфорда
- •55 Вопрос: Формула Бальмера
- •История создания формулы Бальмера и ее значение
- •57 Вопрос: Квантовые числа и их физический смысл
- •58 Вопрос: Состав атомного ядра
- •1919 Г. Э. Резерфорд. Ядерная реакция. 14n(α,p)17o
- •1919 Г. Э. Резерфорд. Ядерная реакция. 14n(α,p)17o
- •1932 Г. Дж. Чедвик. Открытие нейтрона
- •Нейтроны
- •Размер ядра
- •Размер ядра и закон сил
- •Характеристики свободных нейтрона и протона
- •59 Вопрос: Закон радиоактивного распада
12 Вопрос: Изопроцессы
Изопроцессы - это процессы, протекающие при неизменном значении одного из макроскопических параметров (р, V, Т).
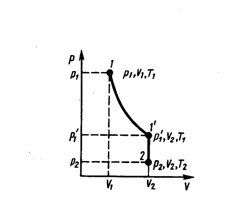
Процесс изменения состояния термодинамической системы макроскопических тел при постоянной температуре называют изотермическим.
Изотермический процесс описывает закон Бойля- Мариотта, открытый в 1861 г. английским ученым Р. Бой-лем (1627-1691) и в 1876 г. французским ученым Э. Мари-оттом (1620-1684). При постоянной массе газа pV = const.
Для газа данной массы произведение давления на его объем постоянно, если температура не меняется.
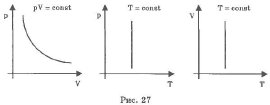
Графики изотермического процесса в координатах р-V; р-Т; V-Т имеют следующий вид (рис. 27):
Процесс изменения состояния термодинамической системы при постоянном давлении называется изобарным. Из уравнения Менделеева-Клапейрона следует, что при
постоянной массе газа
![]()
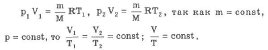
Для данной массы газа отношение объема к температуре постоянно, если давление газа не меняется.
Этот закон был установлен экспериментально в 1802 г. французским ученым Ж. Гей-Люссаком (1778-1850).
Графики изобарического процесса в координатах р-V; V-Т; р-Т имеют следующий вид (рис. 28):
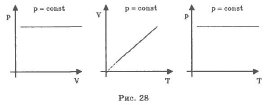
Процесс изменения состояния термодинамической системы при постоянном объеме называется изохорным. Из уравнения Менделеева-Клапейрона можно записать:
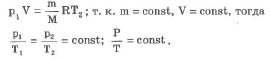

Для данной массы газа отношение давления к температуре постоянно, если его объем не меняется. Графики изохорного процесса в координатах р-V; V-Т; р-Т имеют следующий вид (см. рис. 29). Этот закон был установлен экспериментально в 1787 г. Ж. Шарлем (1746-1823).
13 Вопрос:
Уравнение Менделеева-Клайперона |
Физическое
состояние массы газа определяется
тремя термодинамическими параметрами:
давлением р, объемом V и температурой
Т. Между этими параметрами существует
определенная связь, называемая
уравнением
состояния,
задаваемая в общем виде дается
выражением
Рис.1
В
соответствии с законами Бойля —
Мариотта и Гей-Люссака запишем:
где NA/Vm = n — концентрация молекул (число молекул в единице объема). Таким образом, из уравнения
|
14
вопрос:
![]() ,
где k является постоянной
Больцмана (отношение универсальной
газовой постоянной R к числу
Авогадро NA), i
— число степеней свободы молекул (
,
где k является постоянной
Больцмана (отношение универсальной
газовой постоянной R к числу
Авогадро NA), i
— число степеней свободы молекул (![]() в большинстве задач про идеальные газы,
где молекулы предполагаются сферами
малого радиуса, физическим аналогом
которых могут служить инертные газы),
а T - абсолютная температура.
в большинстве задач про идеальные газы,
где молекулы предполагаются сферами
малого радиуса, физическим аналогом
которых могут служить инертные газы),
а T - абсолютная температура.
Основное уравнение МКТ связывает макроскопические параметры (давление, объём, температура) газовой системы с микроскопическими (масса молекул, средняя скорость их движения).