- •Лекция №15 квантовые свойства атома
- •Опыт Франка и Герца.
- •Квантование энергий и орбит электрона в атоме как проявление волновых свойств электрона
- •Квантовомеханическое описание водородоподобных атомов
- •Лекция №16 квантовые свойства атома
- •Квантовые числа и их физический смысл
- •Опыт Штерна и Герлаха. Гипотеза о спине электрона
- •Атом в магнитном поле
Лекция №16 квантовые свойства атома
Квантовые числа и их физический смысл. Опыт Штерна и Герлаха. Гипотеза о спине электрона. Атом в магнитном поле.
Квантовые числа и их физический смысл
Как следует из решения уравнения Шредингера для атома водорода, квантовое состояние электрона в этом атоме (можно сказать и квантовое состояние атома) полностью определяется заданием трех квантовых чисел. "Задайте значения квантовых чисел, и я полностью опишу свойства атома" - так может современный физик перефразировать известное изречение Архимеда.
Каждое из квантовых чисел принимает только целочисленные значения и определяет, то есть предсказывает результаты измерения основных физических величин в заданном квантовом состоянии атома.
1.
Главное
квантовое число
![]() .
Это квантовое число принимает значения
.
Это квантовое число принимает значения
![]()
и определяет полную энергию электрона в любом квантовом состоянии
|
(16.1) |
В
связанном состоянии электрон в атоме
водорода имеет дискретный энергетический
спектр, лежащий в области отрицательных
значений и имеющий точку сгущения
![]() .
.
2.
Орбитальное (азимутальное) квантовое
число
![]() .
В квантовых состояниях с заданным
значением главного квантового числа
.
В квантовых состояниях с заданным
значением главного квантового числа
![]() азимутальное
квантовое число может иметь следующие
значения:
азимутальное
квантовое число может иметь следующие
значения:
![]() .
.
Из
выводов предыдущего параграфа следует,
что стационарные волновые функции
![]() ,
описывающие различные квантовые
состояния атома, являются собственными
функциями не только оператора полной
энергии
,
описывающие различные квантовые
состояния атома, являются собственными
функциями не только оператора полной
энергии
![]() ,
но и оператора квадрата момента импульса
,
но и оператора квадрата момента импульса
![]() ,
причем
,
причем
![]() .
.
Следовательно, в любом квантовом состоянии атом обладает определенным значением квадрата момента импульса, причем модуль орбитального момента импульса движущегося в атоме электрона однозначно определяется орбитальным квантовым числом:
|
(16.2) |
Проанализируем
эту формулу
квантования момента импульса.
Сравнивая ее с условием квантования
момента импульса движущегося электрона
в теории Бора, можно заметить, что эти
условия не совпадают. И дело не только
в отличии числовых значений, рассчитанных
по этим формулам. Принципиальное отличие
этих соотношений состоит в том, что в
квантовой механике возможны состояния
атома с нулевым моментом импульса. Во
всех
![]() -состояниях
и, частности, в основном
-состояниях
и, частности, в основном
![]() -состоянии,
когда
-состоянии,
когда
![]() ,
по
формуле (16.2)
получаем
,
по
формуле (16.2)
получаем
![]() .
.
При классическом описании движения электрона в атоме по определенной траектории (орбите) в любом состоянии атом должен обладать ненулевым моментом импульса.
Опыт подтверждает существование квантовых состояний атома с нулевыми орбитальными моментами. Следовательно, опыт подтверждает, что только отказ от классического траекторного способа описания движения электрона в атоме позволяет правильно рассчитать и предсказать свойства атома. Вероятностный способ описания движения частиц в квантовой механике является единственно правильным способом описания свойств атомных систем - таков вывод современной физики.
Так
как движущийся вокруг ядра электрон
является заряженной частицей, то такое
движение обуславливает протекание
некоторого замкнутого тока в атоме,
который можно охарактеризовать
орбитальным
магнитным моментом![]() .
.
В
теории Бора, когда с позиции классической
теории рассматривается круговое движение
электрона по орбите радиуса
![]() со
скоростью
со
скоростью
![]() ,
величина орбитального механического
момента равна
,
величина орбитального механического
момента равна
![]() .
Если время полного оборота электрона
.
Если время полного оборота электрона
![]() ,
то такому движению соответствует
замкнутый ток
,
то такому движению соответствует
замкнутый ток
![]() ,
,
который можно охарактеризовать величиной магнитного момента
![]() .
.
Связь механического и магнитного моментов при этом определяется гиромагнитным отношением
|
(16.3) |
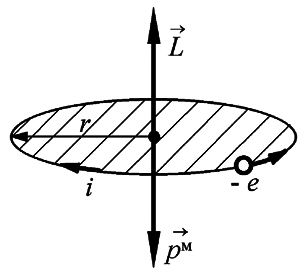
Так
как заряд электрона отрицателен, то для
орбитального движения направление
вектора магнитного момента
![]() противоположно
направлению вектора механического
момента импульса
противоположно
направлению вектора механического
момента импульса
![]() (рис.
16.1).
(рис.
16.1).
Для
расчета орбитального магнитного момента
в квантовой теории следует определить
пространственную плотность электрического
тока
![]() через
плотность потока вероятностей
через
плотность потока вероятностей
![]() по
формуле:
по
формуле:
![]() .
Плотность потока вероятности при этом
можно найти, зная волновую функцию
электрона в заданном квантовом состоянии
атома. Точный квантовомеханический
расчет гиромагнитного отношения также
приводит к формуле (16.3).
.
Плотность потока вероятности при этом
можно найти, зная волновую функцию
электрона в заданном квантовом состоянии
атома. Точный квантовомеханический
расчет гиромагнитного отношения также
приводит к формуле (16.3).
|
Рис. 16.1. |
Итак,
в любом квантовом состоянии атом водорода
обладает не только механическим моментом
![]() ,
величина которого определяется формулой
(16.2),
но
и магнитным моментом.
,
величина которого определяется формулой
(16.2),
но
и магнитным моментом.
|
(16.4) |
Здесь универсальная постоянная
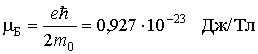
служит единицей измерения магнитных моментов атомов и называется магнетоном Бора.
Если
атом переходит из одного квантового
состояния в другое с испусканием
(поглощением) фотона излучения, то
возможны лишь такие переходы, для которых
орбитальное квантовое число
изменяется
на единицу. Это правило, согласно которому
для оптических переходов
![]() ,
называется правилом
отбора.
Наличие такого правила отбора обусловлено
тем, что электромагнитное излучение
(фотон) уносит или вносит не только квант
энергии, но и вполне определенный момент
импульса, изменяющий орбитальное
квантовое число для электрона всегда
на единицу.
,
называется правилом
отбора.
Наличие такого правила отбора обусловлено
тем, что электромагнитное излучение
(фотон) уносит или вносит не только квант
энергии, но и вполне определенный момент
импульса, изменяющий орбитальное
квантовое число для электрона всегда
на единицу.
3.
Магнитное квантовое число
![]() .
В квантовом состоянии с заданным
значением орбитального квантового
числа
.
В квантовом состоянии с заданным
значением орбитального квантового
числа
![]() ,
магнитное квантовое число может принимать
,
магнитное квантовое число может принимать
![]() различных
значений из ряда
различных
значений из ряда
![]() .
.
Физический
смысл магнитного квантового числа
вытекает из того, что волновая функция
![]() ,
описывающая квантовое состояние
электрона в атоме водорода, является
собственной функцией оператора проекции
момента импульса
,
описывающая квантовое состояние
электрона в атоме водорода, является
собственной функцией оператора проекции
момента импульса
![]() ,
причем
,
причем
![]() .
.
Поэтому,
из общих положений квантовой механики
следует, что проекция момента импульса
электрона на выделенное в пространстве
направление
![]() может
иметь только определенные значения,
равные
может
иметь только определенные значения,
равные
|
(16.5) |
Направление
![]() в
пространстве обычно выделяется внешним
полем (например, магнитным или
электрическим), в котором находится
атом.
в
пространстве обычно выделяется внешним
полем (например, магнитным или
электрическим), в котором находится
атом.
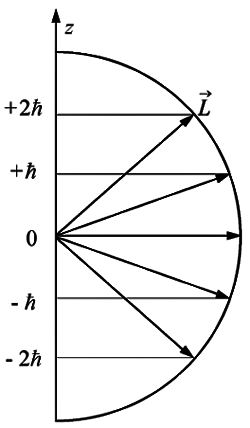
Так как формула (16.5) квантования проекции механического момента соответствует вполне определенным направлениям ориентации в пространстве вектора (рис. 16.2), то эту формулу называют обычно формулой пространственного квантования.
С точки зрения классического представления об электронной орбите, с учетом перпендикулярности вектора к плоскости орбиты, соотношение (16.5) определяет возможные дискретные расположения электронных орбит в пространстве по отношению к направлению внешнего поля.
|
Рис. 16.2. |
Отмеченная выше связь механического и магнитного моментов атома позволяет с учетом (16.5) записать также возможные значения проекции магнитного момента атома на выделенное направление :
|
(16.6) |
зависящие
от значения магнитного квантового числа
![]()

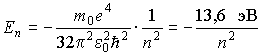 .
. .
.